
【题目】0.5 mol Na2CO3中所含的Na+数约为( )
A.3.01×1023B.6.02×1023C.0.5D.1
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种元素,A的一种同位素可用于考古中测定生物的死亡年代; B与A同周期,其s能级电子数比p能级电子数多;C原子的最外层电子数是次外层的3倍;D与B同主族;E的原子序数为29.回答下列问题:
(1)五种元素中第一电离能最大的是(填元素符号),其中D原子价电子排布图为 .
(2)元素B的简单气态氢化物的沸点填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是; A的简单气态氢化物中心原子的杂化轨道类型为 .
(3)BC3﹣的立体构型为 , 与其互为等电子体的分子是(写化学式).
(4)EC在加热条件下容易转化为E2C,从原子结构的角度解释原因;E原子的外围电子排布式为 , E晶体的堆积方式为(填序号) ①简单立方堆积 ②体心立方堆积
③六方最密堆积 ④面心立方最密堆积
(5)硼与D可形成一种耐磨材料F,其结构与金刚石相似(如图),可由硼的三溴化物和D的三溴化物于高温下在氢气的氛围中合成.写出合成F的化学方程式: . F的晶胞边长为a pm,则该晶体密度的表达式为gcm﹣3 . (用含a、NA的式子表示,不必化简). 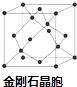
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000molL﹣1的NaOH溶液分别滴定20.00mL浓度均为0.1000molL﹣1的盐酸和醋酸溶液的滴定曲线如图所示(混合溶液体积变化忽略不计).下列说法不正确的是( ) 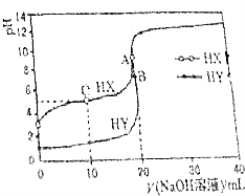
A.根据滴定曲线,可得Ka(CH3COOH)≈10﹣5
B.pH=7时,滴定醋酸溶液消耗的V(NaOH溶液)<20mL
C.C点溶液:c(HX)>c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
D.当V(NaOH溶液)=20mL时,A点水电离出c(H+)大于B点水电离出的c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究碳和硫的化合物的性质,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品.
(1)有科学家提出可利用FeO吸收和利用CO2 , 相关热化学方程式如下: 6FeO(s)+CO2(g)═2Fe3O4(s)+C(s)△H=﹣76.0kJmol﹣1
①上述反应的还原产物为 , 每生成1mol Fe3O4 , 转移电子的物质的量为mol;
②已知:C(s)+2H2O(g)═CO2(g)+2H2(g)△H=+113.4kJmol﹣1 , 则反应:
3FeO(s)+H2O(g)═Fe3O4(s)+H2(g)的△H= .
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2(g)CH4(g)+2H2O(g).向一容积为2L的恒容密闭容器中充入一定量的CO2和H2 , 在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2molL﹣1 , H2 0.8molL﹣1 , CH4 0.8molL﹣1 , H2O 1.6molL﹣1 . 则300℃时上述反应的平衡常数K= . 200℃时该反应的平衡常数K=64.8,则该反应的△H(填“>”或“<”)0.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 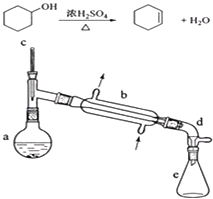
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验中最容易产生的副产物的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用含硫酸铜的工业废液制备硫酸铵,流程如下: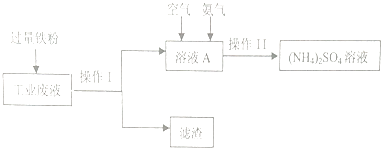
(1)操作Ⅰ的名称为 , 滤渣的成分为 .
(2)工业废液中加入过量铁粉所发生反应的离子方程式为 .
(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要 .
(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓该反应是否为氧化还原反应(填“是”或“否”).
(5)检验(NH4)2SO4溶液中含有SO ![]() 的方法为 .
的方法为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列俗名与物质相匹配的一组是( )
A. 水玻璃——Na2SO4 B. 小苏打——NaHCO3 C. 石膏——CaSiO3 D. 胆矾——FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关碱金性铷(Rb)的叙述中,正确的是( )
A. 灼烧氯化铷时,火焰没有特殊颜色
B. 硝酸铷是离子化合物,易溶于水
C. 在钠、钾、铷三种单质中,铷的熔点最高
D. 氢氧化铷是弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是( )
A.AgCl的溶解度增大
B.AgCl的溶解度、Ksp均不变
C.Ksp(AgCl)增大
D.AgCl的溶解度、Ksp均增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com