
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 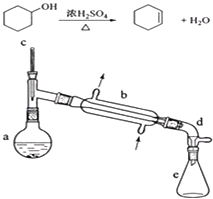
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验中最容易产生的副产物的结构简式为 .
【答案】
(1)蒸馏烧瓶
(2)防止暴沸;B
(3)捡漏;上口倒出
(4)吸收水
(5)ABE
(6)![]()
【解析】解:(1)根据仪器a的构造可知其名称为蒸馏烧瓶,所以答案是:蒸馏烧瓶;
(2.)混合液态在加热时易发生爆沸现象,碎瓷片的存在可以防止在加热过程中产生暴沸现象;如果加热一段时间后发现忘记加瓷片,补加碎瓷片时需要待已加热的试液冷却后再加入,则B正确,所以答案是:防止暴沸;B;
(3.)由于分液漏斗有活塞开关,则使用前需要检查是否漏液;分液过程中,由于环己烯的密度比水的密度小,故应该从分液漏斗的上口倒出,所以答案是:检漏;上口倒出;
(4.)无水氯化钙具有吸水性,分离提纯过程中加入无水氯化钙可吸收产物中少量的水,所以答案是:吸收水;
(5.)利用蒸馏方法分离出环己烯,需要用到的仪器有:圆底烧瓶、温度计、接收器、冷凝管等,不会用到玻璃杯、漏斗,则正确的为ABE,所以答案是:ABE;
(6.)加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应,分子间发生脱水反应生成二环己醚,其结构简式为: ![]() ,所以答案是:
,所以答案是: ![]() .
.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A.H、D、T互为同位素
B.NaHCO3、HCOONa均含有离子键和共价键
C.常温常压下,22.4 L CCl4含有NA个CCl4分子
D.常温下,23 g NO2含有NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于某些氧化物的说法正确的是( )
A. NO2、Na2O2都能与水发生氧化还原反应
B. NO、CO2均可用向上排空气法收集
C. CO2、SO2可用澄清石灰水鉴别
D. CO2、SO3都可由相应单质在O2中燃烧生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.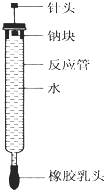
(1)钠与水反应的离子方程式为 .
(2)实验中“钠块熔化为闪亮的小球”说明;向烧杯中的溶液中滴加 , 溶液变红,说明钠与水反应生成碱性物质.
(3)如果实验前加入反应管内水的体积为a mL,欲使水最终全部被排出,则所取金属钠的质量至少为g.(设当时实验条件下气体摩尔体积为V mL/mol,写出简要步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
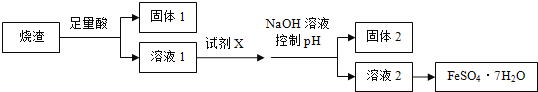
【题目】利用硫铁矿焙烧的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
已知部分阳离子以氢氧化物形式沉淀时溶液的pH 见下表:
沉淀物 | F e(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)试剂X应选用________________。
(2)控制pH 的范用_________________。
(3)从溶液2得到FeSO4·7H2O 产品的过程中,须控制条作防止其氧化和分解,检验FeSO4溶液是否变质的方法是______________。
(4) 利用溶液1还可制备一种新型高效净水剂——聚合硫酸铝铁[Al2Feb(OH)m(SO4)n·xH2O],为了测定某种聚合硫酸铝铁的组成,进行如下实验:
步骤一:准确称取8.810g 样品溶于150mL0.100mol·L-1稀硫酸,恰如完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体10.485g;
步骤二:另取相同质量的样品,溶于过量的氢碘酸,充分搅拌反应后,以0.500mol·L-1 Na2S2O3溶液滴定至浅黄色,滴入几滴淀粉溶液,继续滴定至终点,消耗Na2S2O3溶液20.00mL。
(已知:I2+2Na2S2O3=2NaI+Na2S4O6 )
通过计算确定该聚合硫酸铝铁的化学式______________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示.下列说法错误的是( ) 
A.可利用KSCN溶液检验FeSO4溶液是否变质
B.沉淀过程中有CO2气体放出
C.过滤搡作的常用玻璃仪器有烧杯、漏斗和玻璃棒
D.产品FeCO3在空气中高温分解可得到纯净的FeO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示. 
请回答下列问题:
(1)电极X的材料是;电解质溶液Y是;
(2)银电极为电池的极,发生的电极反应为;X电极上发生的电极反应为;
(3)外电路中的电子是从电极流向电极.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com