
【题目】下列俗名与物质相匹配的一组是( )
A. 水玻璃——Na2SO4 B. 小苏打——NaHCO3 C. 石膏——CaSiO3 D. 胆矾——FeSO4
科目:高中化学 来源: 题型:
【题目】常温下,向20mL的某稀H2S04溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴人氨水体积变化如图.下列分析正确的是( ) 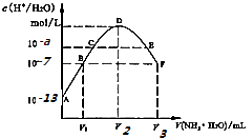
A.稀硫酸的浓度为0.1mol/L
B.C点溶液pH=14﹣a
C.E溶液中存在:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
D.B到D,D到F所加氨水体积一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.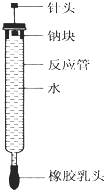
(1)钠与水反应的离子方程式为 .
(2)实验中“钠块熔化为闪亮的小球”说明;向烧杯中的溶液中滴加 , 溶液变红,说明钠与水反应生成碱性物质.
(3)如果实验前加入反应管内水的体积为a mL,欲使水最终全部被排出,则所取金属钠的质量至少为g.(设当时实验条件下气体摩尔体积为V mL/mol,写出简要步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫铁矿焙烧的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
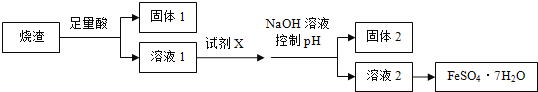
已知部分阳离子以氢氧化物形式沉淀时溶液的pH 见下表:
沉淀物 | F e(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)试剂X应选用________________。
(2)控制pH 的范用_________________。
(3)从溶液2得到FeSO4·7H2O 产品的过程中,须控制条作防止其氧化和分解,检验FeSO4溶液是否变质的方法是______________。
(4) 利用溶液1还可制备一种新型高效净水剂——聚合硫酸铝铁[Al2Feb(OH)m(SO4)n·xH2O],为了测定某种聚合硫酸铝铁的组成,进行如下实验:
步骤一:准确称取8.810g 样品溶于150mL0.100mol·L-1稀硫酸,恰如完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体10.485g;
步骤二:另取相同质量的样品,溶于过量的氢碘酸,充分搅拌反应后,以0.500mol·L-1 Na2S2O3溶液滴定至浅黄色,滴入几滴淀粉溶液,继续滴定至终点,消耗Na2S2O3溶液20.00mL。
(已知:I2+2Na2S2O3=2NaI+Na2S4O6 )
通过计算确定该聚合硫酸铝铁的化学式______________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为28,可以使溴的四氯化碳溶液褪色,F高分子化合物,它有如下转化关系: 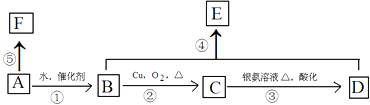
按要求填空:
(1)写出C中所含官能团的名称 , 指出④的反应类型 .
(2)若B转化为A,所需反应条件为: .
(3)写出B和F结构简式:B;F .
(4)写出反应③对应的化学方程式: .
(5)写出反应④对应的化学方程式: .
(6)E的同分异构体有多种,其中能与NaHCO3反应的同分异构体共有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示.下列说法错误的是( ) 
A.可利用KSCN溶液检验FeSO4溶液是否变质
B.沉淀过程中有CO2气体放出
C.过滤搡作的常用玻璃仪器有烧杯、漏斗和玻璃棒
D.产品FeCO3在空气中高温分解可得到纯净的FeO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中所用少量氯气是用下列方法制取的,4HCl(浓)+MnO2 ![]() Cl2↑+MnCl2+2H2O 试回答下列问题:
Cl2↑+MnCl2+2H2O 试回答下列问题:
(1)实验室中可采用溶液来吸收有毒的氯气,写出该反应的离子方程式 .
(2)实验取质量分数为36.5%,密度为1.19gcm﹣3 , 浓盐酸100mL,反应结束后测得盐酸的浓度变为1.9mol/L,(忽略体积的变化)请你计算出实验过程生成标况下的Cl2多少L(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下面叙述正确的是( )
A.标准状况下,11.2L SO3所含分子数为0.5 NA
B.1L 1mol/L的氯化钠溶液中,所含离子数为NA
C.64g二氧化硫含有原子数为3NA
D.在反应中,1mol镁转化为Mg2+后失去的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com