
有关物质间转化关系如下图,试回答:
(1)转化①的反应条件为 .
(2)转化②的化学方程式为 .转化③的离子方程式为 .
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 (填名称).
(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为 mL。
(1)融熔、电解 (各1分,共2分)
(2)2Al+2 NaOH+2H2O=2NaAlO2+3H2↑,MnO2+4 H++2Cl- Mn2++Cl2↑+2 H2O
Mn2++Cl2↑+2 H2O
(3)氨水( 2分) (4)150mL、550mL(各2分,共4分)
解析试题分析:1)工业制备铝,是电解融熔的氧化铝。 (2)反应的化学方程式分别为:2Al+2 NaOH+2H2O=2NaAlO2+3H2↑,MnO2+4 H++2Cl-=Mn2++Cl2↑+2 H2O(3)若转化⑤用于实验室制Al(OH)3,由于氢氧化铝能溶于强碱,所以选择氨水弱碱溶液可以使铝离子尽可能转化为沉淀。(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积有两种情况,一种是铝离子剩余,即NaOH溶液少量,求得NaOH溶液的体积为150mL.。另一种情况是当铝离子先全部转化为沉淀然后再用NaOH溶液溶解氢氧化铝剩下的沉淀刚好,这时求得为550mL。
考点:考查铝离子和偏铝酸根离子的转化计算。


科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F 六种物质有如下图所示转化关系,其中物质D常温下为固体,物质E是淡黄色粉末。(部分反应物、生成物及反应条件已略去)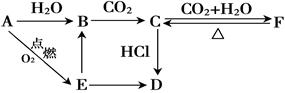
(1)写出物质A、D的化学式:A. ; D. ;
(2)写出下列物质转化反应的离子方程式:
B C: ,
C: ,
E B: ,
B: ,
C F: 。
F: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
我国从澳大利亚进口的某高炉生铁(用A表示)的成分如下(其余是铁):
| C | Si | Mn | P | S |
| 4.070% | 2.900% | 0.495% | 0.165% | 0.010% |
| | FeO | Fe2O3 | CaO |
| 烟尘煅烧前(%) | 86.40 | 4.00 | 9.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提炼Al2O3并制取铝的流程如下: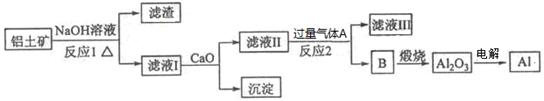
请回答下列问题:
(1)铝与NaOH溶液反应的离子方程式为 。
(2)图中涉及分离溶液与沉淀的玻璃仪器有烧杯、玻璃棒、_________。
(3)反应1涉及的化学方程式有 、 。滤液Ⅰ中加入CaO生成的沉淀是_ (填化学式)。
(4)向滤液Ⅱ中通入气体A为 ,生成沉淀B的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
以下是对金属及其化合物的讨论,根据要求回答问题
(1)写出钠与水反应的离子方程式 。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是 ,
反应的离子方程式为 , 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
常见金属单质A、B和非金属单质C、D以及它们化合物之间的转化关系如下。F、J既能溶于强酸M又能溶于强碱N,Z的摩尔质量为198 g·mol-1,且其中各元素的质量比为:钾:金属B:氧=39:28:32。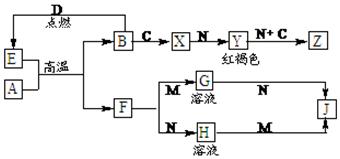
请回答下列问题:
(1)C的化学式为 ,Z的化学式为 。
(2)写出检验X中阳离子的方法 。
(3)写出E和A在高温下反应的化学方程式为 。
(4)写出A和N反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铝是一种应用广泛的金属,工业上用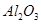 和冰晶石(
和冰晶石(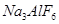 )混合熔融电解制得。
)混合熔融电解制得。
①铝土矿的主要成分是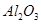 和
和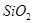 等。从铝土矿中提炼
等。从铝土矿中提炼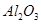 的流程如下:
的流程如下: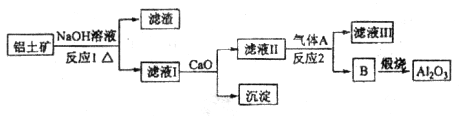
②以萤石(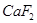 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下: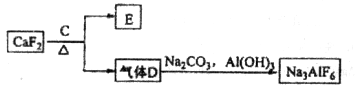
回答下列问题:
(1)写出反应1的化学方程式_________________________、________________________________;
(2)滤液Ⅰ中加入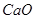 生成的沉淀是___________,反应2的离子方程式为____ ___________________
生成的沉淀是___________,反应2的离子方程式为____ ___________________
(3)E常用作制作豆腐的添加剂,化合物C是____,写出由D制备冰晶石的化学方程式_______________;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁及其化合物之间的相互转化可用下式表示: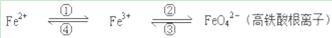
回答下列有关问题:
(1)铁元素在周期表中的位置是___________________________。
(2)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是________(选填序号)。
A.Cl2 B.Fe C.HNO3 D.H2O2
(3)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价),下列说法正确的是________(选填序号)。
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2既作氧化剂又作还原剂
D.当转移1 mol电子时,46 g CuFeS2参加反应
(4)下述反应中,若FeSO4和O2的系数比为2︰1,试配平下列方程式:
FeSO4 + K2O2 → K2FeO4 + K2O + K2SO4 + O2↑
(5)向某稀HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体, 该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如右图所示。则混合溶液中HNO3和Fe(NO3)3的物质的量浓度之比为__________。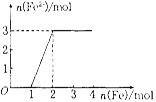
(6)某同学将铁与水蒸气高温反应后的固体物质溶解在过量盐酸中,如何判断所得溶液中是否含有Fe3+? ___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
镁铝尖晶石(MgAl2O4)常做耐火材料。共沉淀制备尖晶石的方法是:用AlCl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。完成下列填空:
(1)为使Mg2+、Al3+同时生成沉淀,应该把 (填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
(用离子符号表示)。
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是 ,属于难溶物的电离方程式 。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________。
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com