
【题目】铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速易行的方法:首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③烧杯中潮湿的铁丝依然光亮。
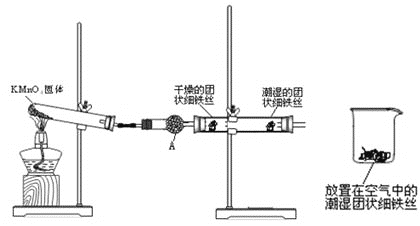
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___,能表示其原理的正极反应式为_________,负极反应式为________;
(2)仪器A的名称为____,其中装的药品可以是____,其作用是_____________;
(3)由实验可知,该类铁生锈的条件为_____。决定铁生锈快慢的一个重要因素是_______。
【答案】吸氧腐蚀 Fe-2e-=Fe2+ 2H2O+O2+4e-=4OH- 球形干燥管 碱石灰(或无水氯化钙) 干燥氧气 与O2接触、与水接触 氧气的浓度
【解析】
(1)在弱酸性或中性条件下,钢铁发生吸氧腐蚀;铁、C和水构成原电池,负极上Fe失电子发生氧化反应,正极上氧气得电子发生还原反应,据此分析解答;
(2)根据A的形状分析判断;A中盛放的物质是固态且具有吸水性,据此分析解答;
(3)根据三团细铁丝生锈程度确定铁生锈的条件,根据不同点确定铁生锈快慢因素。
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中水呈中性,实验中铁的生锈属于吸氧腐蚀,Fe作负极,负极反应式为Fe-2e-=Fe2+,C作正极,正极反应为:2H2O+O2+4e-=4OH-,故答案为:吸氧腐蚀;Fe-2e-=Fe2+;2H2O+O2+4e-=4OH-;
(2)根据图示,仪器A是球形干燥管,本实验中干燥管是用来干燥氧气的,盛放的物质是碱石灰(或无水氯化钙),故答案为:球形干燥管;碱石灰(或无水氯化钙);干燥氧气;
(3)钢铁在潮湿环境下形成原电池,发生电化学腐蚀;根据直形管中的现象说明,潮湿是铁生锈的条件;直形管实验与烧杯实验的对比,则说明O2浓度是影响生锈快慢的一个重要因素,所以铁生锈的条件是与氧气接触、与水接触,故答案为:与O2接触、与水接触;氧气的浓度。


科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g)ΔH<0,在一定条件下达平衡,下列有关叙述正确的是①增加A的量,平衡向正反应方向移动②升高温度,平衡向逆反应方向移动,v正减小③压强增大一倍,平衡不移动,v正、v逆不变④增大B的浓度,v正>v逆⑤加入催化剂,平衡向正反应方向移动
C(g)+2D(g)ΔH<0,在一定条件下达平衡,下列有关叙述正确的是①增加A的量,平衡向正反应方向移动②升高温度,平衡向逆反应方向移动,v正减小③压强增大一倍,平衡不移动,v正、v逆不变④增大B的浓度,v正>v逆⑤加入催化剂,平衡向正反应方向移动
A.①②B.④C.③D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学以一种工业废渣(主要成分为MgCO3和少量C、Al2O3、FeSO4等)为原料制备MgCO3·3H2O,其设计的实验流程如下:
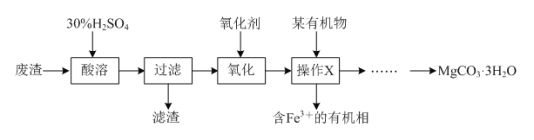
(1)质量分数为30%的稀硫酸(密度是1.176 g·cm-3)的物质的量浓度为__________。
(2)滤渣的化学式为________;操作X的名称为__________,该操作需要的玻璃仪器是___________。
(3)已知:在下列实验中,当溶液中pH=8.5时,Mg(OH)2开始沉淀;pH=5.0时,Al(OH)3沉淀完全。请补充完整由操作X得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水,________,过滤、用水洗涤固体2-3次,在50℃下干燥,得到MgCO3·3H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 =2CO2 +3H2O,电池示意如图,

下列说法不正确的是()
A.a极为电池的负极
B.电池工作时,1mol乙醇被氧化时就有6mol电子转移
C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O
D.电池工作时电流由b极沿导线经灯泡再到a极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的图示与对应的叙述相符的是

A. 图1表示向l00mL0.l mol·L-l的A1Cl3溶液中滴加1 mol·L-1的NaOH溶液时n [Al(OH)3]的变化情况
B. 图2表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点
C. 图3表示某一放热反应,若使用催化剂,E1、E2、△H都会发生改变
D. 图4表示向Na2CO3溶液中滴加稀盐酸时,产生n(CO2)的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将![]() 体积NO和
体积NO和![]() 体积O2同时通入倒立于水中且盛满水的容器中,充分反应后,容器内残留
体积O2同时通入倒立于水中且盛满水的容器中,充分反应后,容器内残留![]() 体积的气体,该气体与空气接触变为红棕色,则
体积的气体,该气体与空气接触变为红棕色,则![]() 为( )
为( )
A. 3:2 B. 2:3 C. 8:3 D. 3:8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.生物质能与氢能均属于一次能源
B.电解熔融MgCl2可以得到单质Mg和氯气,该反应是一个放出能量的反应
C.相同状况下,已知:2SO2+O2![]() 2SO3 ΔH<0,则2SO3
2SO3 ΔH<0,则2SO3![]() 2SO2+O2是一个吸热反应
2SO2+O2是一个吸热反应
D.取一定量的Ba(OH)2·8H2O晶体和NH4Cl晶体于烧杯中搅拌,烧杯壁下部变冷,放出的气体使蓝色石蕊试纸变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲中可能含NO、CO2、NO2、NH3、N2中的几种。将100mL气体甲经过如图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
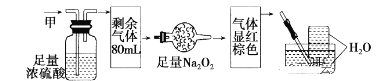
A.NH3、NO2、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法中正确的是
①20 g D2O含有的电子数为10NA
②含有1molFe(OH)3的氢氧化铁胶体中含有胶粒数为NA
③1 L0.1mol/L的NH4NO3溶液中氮原子数为0.2NA
④ 在标准状况下22.4 L SO3的物质的量为1mol
⑤25℃时,pH=12的l.0LNaClO溶液中水电离出的OH-的数目为0.01NA
⑥常温下,5.6 L NO和5.6 LO2的混合气体中含有的分子数为0.5NA
⑦l mol Na2O2与水完全反应时转移电子数为2NA
A. ③⑥⑦ B. ①③⑤ C. ①②④ D. ④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com