
����Ŀ��ij��ѧѧϰС�������ͼʵ��װ�ã��г�װ����ȥ���Ʊ�������̽��������������ʣ�Dװ��Ϊ��Һ©����״���ͽ��߳��� 
��1����Aװ���й���ҩƷΪMnO2 �� д�������ӷ�Ӧ����ʽ����Aװ���й���ҩƷΪKC1O3 �� ��Ӧ��ÿ����1mol Cl2ʱת�Ƶ�����ĿΪ ��
��2��װ��B���������� �� ��C�������˶�������B�е����� ��
��3��װ��C����������֤�����Ƿ����Ư���ԣ�I����ʪ�����ɫ��������II��III��Ӧ��������ʷֱ����� ��
���𰸡�
��1��MnO2+4H++2Cl�� ![]() Mn2++C12��+2H2O��1.67NA��
Mn2++C12��+2H2O��1.67NA�� ![]() NA
NA
��2����ȥHCl���壻��������C12������©���ڵ�Һ��������ƿ��Һ���½�
��3����ˮCaC12������ĺ첼��
���������⣺�ڼ��������£�Ũ����Ͷ���������A�з�Ӧ����������Ũ������лӷ��ԣ��������ɵ������к���HCl���ñ���ʳ��ˮ��ȥ������HCl������û��Ư���Ե�������û��Ư���ԣ��������廯�Ʒ�Ӧ�����壬���ܺ�KI��Ӧ���ɵⵥ�ʣ������ж������ſգ�Ӧ����NaOH��Һ����β������1�����������£�Ũ����Ͷ������̷�Ӧ�������������ӷ���ʽΪMnO2+4H++2Cl�� ![]() Mn2++C12��+2H2O�������ᷴӦ�Ļ�ѧ����ʽΪ��KClO3+6HCl=KCl+3Cl2��+3H2O����Ӧ����3molCl2 �� ת�Ƶ���5mol����Ӧ��ÿ����1mol Cl2ʱת�Ƶ��Ӹ���Ϊ1.67NA��
Mn2++C12��+2H2O�������ᷴӦ�Ļ�ѧ����ʽΪ��KClO3+6HCl=KCl+3Cl2��+3H2O����Ӧ����3molCl2 �� ת�Ƶ���5mol����Ӧ��ÿ����1mol Cl2ʱת�Ƶ��Ӹ���Ϊ1.67NA�� ![]() NA �� ���Դ��ǣ�MnO2+4H++2Cl��
NA �� ���Դ��ǣ�MnO2+4H++2Cl�� ![]() Mn2++C12��+2H2O��1.67NA��
Mn2++C12��+2H2O��1.67NA�� ![]() NA����2������ʳ��ˮ�����������ܽ������ܽ��Ȼ��⣬��װ�û���������������������Bװ�������dz�ȥHCl���塢��������C12�� Cװ�÷��������ᵼ��B��ѹǿ������©���ڵ�Һ��������ƿ��Һ���½������Դ��ǣ���ȥHCl���壻��������C12������©���ڵ�Һ��������ƿ��Һ���½�����3��Ҫ��֤����û��Ư���ԣ�Ӧ���ø������������Ȼ���ø���ĺ�ɫ�������飬��II��III�����������Ϊ��ˮCaC12����ĺ첼����
NA����2������ʳ��ˮ�����������ܽ������ܽ��Ȼ��⣬��װ�û���������������������Bװ�������dz�ȥHCl���塢��������C12�� Cװ�÷��������ᵼ��B��ѹǿ������©���ڵ�Һ��������ƿ��Һ���½������Դ��ǣ���ȥHCl���壻��������C12������©���ڵ�Һ��������ƿ��Һ���½�����3��Ҫ��֤����û��Ư���ԣ�Ӧ���ø������������Ȼ���ø���ĺ�ɫ�������飬��II��III�����������Ϊ��ˮCaC12����ĺ첼����
���Դ��ǣ���ˮCaC12������ĺ첼����
�����㾫�������ڱ��⿼���������ʵ�����Ʒ�����Ҫ�˽�ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O���ܵó���ȷ�𰸣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ����������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ��ǣ� ��
A.SiO2 ![]() SiCl4
SiCl4 ![]() Si
Si
B.FeS2 ![]() SO2
SO2 ![]() H2SO4
H2SO4
C.N2 ![]() NH3
NH3 ![]() NH4Cl��aq��
NH4Cl��aq��
D.MgCO3 ![]() MgCl2��aq��
MgCl2��aq�� ![]() Mg
Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��HCOONa���ȷֽ�ʱ������ʧ�������¶ȵĹ�ϵ��ͼ��ʾ�������ķ�Ӧ�У�
2HCOONa ![]() Na2C2O4+H2�� ��
Na2C2O4+H2�� ��
2HCOONa ![]() Na2CO3+H2��+CO����
Na2CO3+H2��+CO����
Na2C2O4 ![]() Na2CO3+CO�� ��
Na2CO3+CO�� ��
����˵����ȷ���ǣ� ��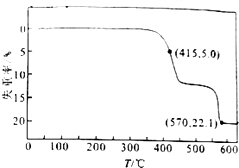
A.T��415�棬ֻ�з�Ӧ�ٷ���
B.��Ӧ�١��ڲ�����ͬʱ����
C.570�棼T��600��ʱ�������������Ҫ�ɷ���Na2CO3
D.���������е�m��Na2C2O4��=m��Na2CO3��ʱ����Ӧ�١��ڵķ�Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2�� H2�ڴ�������ϳɰ��������̼������仯��ʾ��ͼ���£��� ![]() ��
�� ![]() ��
�� ![]() �ֱ��ʾN2��H2��NH3 �� ����˵����ȷ���ǣ� ��
�ֱ��ʾN2��H2��NH3 �� ����˵����ȷ���ǣ� �� 
A.ʹ�ô������ϳɰ���Ӧ�ų�����������
B.�ڸù����У�N2��H2�ϼ��γ�Nԭ�Ӻ�Hԭ��
C.�ڸù����У�Nԭ�Ӻ�Hԭ���γ��˺��зǼ��Լ���NH3
D.�ϳɰ���Ӧ�У���Ӧ��ϼ��������������������γ��¼��ͷŵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D�����ֶ�����Ԫ�أ����ǵ�ԭ����������������֪A��Cԭ�������ֻ��һ�����ӣ�C����ȼ��ʱ����ɫΪ��ɫ��C�����ڼ�����������B�ĵ��ʳ�ַ�Ӧ���Բ�������ɫ���廯���A������D���ʿ��Է������Ϸ�Ӧ���ҷ�Ӧ���������ǵ�ȼ���߹��գ��Ը������������ش�
��1��д��A��B��C��D��Ԫ�ط��ţ�ABCD
��2��д����Ӧ�Ļ�ѧ����ʽ�� ��A������D���ʷ�Ӧ�� ��
��C������B�����ڼ��ȵ������·�Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤����������ֵ������˵����ȷ���ǣ� ��
A.���ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl������ΪNA
B.���³�ѹ�£�1.06gNa2CO3���е�Na+��Ϊ0.02NA
C.ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4L
D.��״���£�22.4LH2O���еķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1mol X��1mol Y�����2L���ܱ������У��������·�Ӧ 2X��g��+Y��g��=nZ��g��+2W��g����2minĩX�����ʵ���Ϊ0.2mol����Z��Ũ�ȱ�ʾ�ķ�Ӧ����Ϊ0.1mol/��Lmin�� ��ش�
��1��ǰ2min��X��Ũ�ȱ�ʾ��ƽ����Ӧ����
��2��nֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4mol A�����2mol B������2L���ܱ������ڻ�ϣ�����һ�������·������·�Ӧ��2A��g��+B��g��2C��g��������2s����C��Ũ��Ϊ0.6molL��1 �� �������м���˵���� ��������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3molL��1s��1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6molL��1s��1
��2sʱ����A��ת����Ϊ70%
��2sʱ����B��Ũ��Ϊ0.7molL��1
������ȷ���ǣ� ��
A.�٢�
B.�٢�
C.�ڢ�
D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��Һ�������һ�����͵���ɫ�������ܵ�أ������ܷ�ӦΪ��
V3++VO2++H2O ![]() VO2++2H++V2+ �� ����˵����ȷ���ǣ� ��
VO2++2H++V2+ �� ����˵����ȷ���ǣ� ��
A.�ŵ�ʱÿת��2mol����ʱ������1mol������
B.�ŵ�ʱ������ӦΪ��VO+2+2H++e��=VO2++H2O
C.�ŵ�����е����ɸ��������·���������������������������Һ����
D.�������У�H+������������������Ǩ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com