
【题目】次硫酸氢钠甲醛(aNaHSO2bHCHOcH2O)俗称吊白块,在印染、医药以及原子能工业中应用广泛。某化学兴趣小组以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛。已知次硫酸氢钠甲醛易溶于水,微溶于乙醇,具有强还原性,且在120℃以上会发生分解。实验装置(如图1所示)及步骤如下:

I.在三颈烧瓶中加入一定量的Na2SO3和水,搅拌溶解后缓慢通入SO2,制得NaHSO3溶液。
II.将装置A中导气管换成橡皮塞。向三颈烧瓶中加入稍过量的锌粉和一定量37%的甲醛溶液,不断搅拌,在80~90℃左右的水浴中反应约3h后趁热过滤,试剂X洗涤。
III.将滤液蒸发浓缩,冷却结晶,过滤;往滤液中加入适量试剂Y,析出晶体,过滤;合并滤渣,试剂Z洗涤,干燥得到产品。
请回答下列问题:
(1)Na2SO3水溶液中,含硫微粒H2SO3、HSO3-、SO32-随pH的分布如图2所示,则步骤I中确定何时停止通SO2的实验操作为___。
(2)下列说法中正确的是___。
A.B中烧杯中盛放的试剂可以是NaOH溶液
B.试剂Y是无水乙醇;试剂X与试剂Z都是乙醇的水溶液
C.冷凝管内冷凝回流的主要物质是HCHO
D.步骤III中所选择的干燥操作应为真空干燥
(3)步骤II中的水浴加热相比于与酒精灯直接加热,除了有使三颈烧瓶受热更均匀、较低温度下减少产物的分解之外,还有___的优点。化学兴趣小组的同学为完成所设计的实验,除图1中装置仪器外,还需要使用到的仪器有___。
(4)步骤III中蒸发浓缩时应注意的问题有___(并简要说明理由)。
(5)AHMT分光光度法常用于测定溶液样本中甲醛的浓度。其原理是:甲醛与AHMT溶液在碱性条件下缩合后,经高碘酸钾氧化成一种紫红色化合物,其对特定波长光的吸收程度(即色泽深浅)与甲醛在一定浓度范围内成正比。现测得该紫红色化合物的吸光度A与HCHO标准溶液的浓度关系如图3所示:

该化学兴趣小组的同学设计了如下实验确定次硫酸氢钠甲醛的组成:
I.准确称取1.5400g样品,完全溶于水配制成100mL溶液
II.取25.00mL所配溶液经AHMT分光光度法测得溶液吸光度A=0.4000
III.另取25.00mL所配溶液,加入过量碘完全反应后,再加入BaCl2溶液充分反应,得到0.5825g白色沉淀。其反应原理为:
aNaHSO2bHCHOcH2O+I2→NaHSO4+HI+HCHO+H2O(未配平)。
①通过计算可知次硫酸氢钠甲醛的化学式为___。
②结合三颈烧瓶内发生的合成反应产物分析,题干的步骤II中,不断搅拌的目的为:___。
③若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物。写出该反应的离子方程式___。
【答案】测量溶液的pH,若溶液的pH约为4,则停止通入SO2 ACD 更易控制反应温度在80℃90℃或更有利于SO2在水中的溶解 温度计 应在真空容器中蒸发浓缩,真空降低水的沸点,防止温度过高产品分解,真空也可防止氧气氧化产物 NaHSO2·HCHO·2H2O 合成反应生成的Zn(OH)2会附着在锌粉表面,阻止反应进一步进行 OH-+2HCHO=HCOO-+CH3OH
【解析】
(1) 根据图象分析溶液的pH和溶液中含硫微粒的主要存在形式,据此回答;
(2) 该步为次硫酸氢钠甲醛的制备,根据它的性质:易溶于水,微溶于乙醇,具有强还原性,且在120℃以上会发生分解,考虑如何洗涤、干燥,B装置为尾气处理装置,甲醛容易挥发,据此回答;
(3)根据水浴加热的特点和二氧化硫的相关性质回答该问;
(4)在蒸发浓缩时特别注意次硫酸氢钠甲醛在120℃以上会发生分解;
(5)根据图象分析甲醛的量,根据硫原子守恒确定NaHSO2的量,再根据质量守恒确定水的量,据此求出次硫酸氢钠甲醛的化学式,其它根据题给信息回答即可。
![]() 由图2可知,当pH约为4时,溶液中含硫的微粒主要是
由图2可知,当pH约为4时,溶液中含硫的微粒主要是![]() ,故可测量溶液的pH,若溶液的pH约为4,则停止通入
,故可测量溶液的pH,若溶液的pH约为4,则停止通入![]() ;
;
![]() 装置B为尾气处理,可用NaOH溶液来吸收
装置B为尾气处理,可用NaOH溶液来吸收![]() 等有毒气体,故A正确;
等有毒气体,故A正确;
B.次硫酸氢钠甲醛易溶于水,微溶于乙醇,故不能用乙醇的水溶液进行洗涤,避免造成产品溶解而损失,故B错误;
C.甲醛易挥发,冷凝回流,提高其利用率,故C正确;
D.次硫酸氢钠甲醛受热易分解,则应选择真空干燥,故D正确;
![]() 水浴加热,除了有使三颈烧瓶受热更均匀、较低温度下减少产物的分解之外,还有更易控制反应温度在
水浴加热,除了有使三颈烧瓶受热更均匀、较低温度下减少产物的分解之外,还有更易控制反应温度在![]() 或更有利于
或更有利于![]() 在水中的溶解;还需要温度计测量温度;
在水中的溶解;还需要温度计测量温度;
![]() 步骤III中蒸发浓缩时应注意的问题有:应在真空容器中蒸发浓缩,真空降低水的沸点,防止温度过高产品分解,真空也可防止氧气氧化产物;
步骤III中蒸发浓缩时应注意的问题有:应在真空容器中蒸发浓缩,真空降低水的沸点,防止温度过高产品分解,真空也可防止氧气氧化产物;
![]() 由图可知
由图可知![]() ,则100mL溶液中
,则100mL溶液中![]() ;
;![]() 白色沉淀为硫酸钡,其物质的量为
白色沉淀为硫酸钡,其物质的量为![]() ,则100mL溶液中
,则100mL溶液中![]() ,则
,则![]() 样品中含
样品中含![]() ,
,![]() ,则
,则![]() 的物质的量为:
的物质的量为:![]() ,则a:b:
,则a:b:![]() :
:![]() :
:![]() :1:2,则次硫酸氢钠甲醛的化学式为
:1:2,则次硫酸氢钠甲醛的化学式为![]() ;
;
![]() 在步骤II中,合成反应生成的
在步骤II中,合成反应生成的![]() 会附着在锌粉表面,阻止反应进一步进行;
会附着在锌粉表面,阻止反应进一步进行;
![]() 加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,可知其反应的离子方程式为
加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,可知其反应的离子方程式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】油脂是油与脂肪的总称,它是多种高级脂肪酸的甘油酯。油脂既是重要食物,又是重要的化工原料。油脂的以下用途与其含有的碳碳不饱和键(![]() )有关的是
)有关的是
A. 衣服上的油脂可用汽油洗去
B. 适量摄入油脂,有利于人体吸收多种脂溶性维生素和胡萝卜素
C. 植物油通过氢化可以制造植物奶油(人造奶油)
D. 脂肪是有机体组织里储存能量的重要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
X | ||
Y | ||
Z | M |
A.电负性:Y>Z>M
B.离子半径:M->Z2->Y-
C.ZM2分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子最外层电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,通常采用电解法处理酸性废水中的![]() ,装置示意图如图所示。下列说法正确的是
,装置示意图如图所示。下列说法正确的是
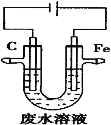
A.石墨极上发生氧化反应
B.阳极的电极反应式为![]()
C.除去![]() 的反应:
的反应:![]()
D.随着电解的进行,石墨极附近电解质溶液的pH会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请阅读下列材料,完成下面小题。
利用Kolbe's电解法制取乙炔的反应原理为: +2H2O
+2H2O 2CO2↑+C2H2↑+H2↑+2KOH
2CO2↑+C2H2↑+H2↑+2KOH
【1】下列表示反应中相关微粒的化学用语错误的是( )
A.中子数为20的钾原子:![]() K
K
B.K+的结构示意图:
C.CO2的电子式:![]()
D.C2H2的结构式:H—C![]() C—H
C—H
【2】有关该反应的下列说法正确的是( )
A.化学能转变为电能
B.电解槽中向阴极迁移的主要是H+
C.电解过程中溶液pH不断减小
D.阴极的电极反应式为2H2O+2e-=2OH-+H2↑
【3】下列羧酸钾盐中,其水溶液电解生成的烃主要是CH2=CH2的是( )
A.CH3COOKB.CH3CH2COOKC.CH2=CHCOOKD.KOOCCH2CH2COOK
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究Mg与NaHCO3溶液反应的机理,做了如下探究。
实验一:
实验A | 实验B | |
操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液。 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水。 |
现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |
(1)实验B的目的是___。
实验二:
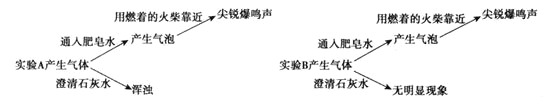
(2)根据实验二,实验A中产生的气体是___。(填分子式)
实验三:分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象。
(3)实验三说明Mg与NaHCO3溶液反应产生了___(填离子符号)。
实验四:该小组同学对实验A中产生的白色沉淀做出如下猜测:并用图所示装置进行实验,进一步确定白色沉淀的成分。

猜测1:白色不溶物可能为Mg(OH)2
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH)2xMgCO3]
(4)若用装置A、B组合进行实验,B中有白色浑浊,则猜想___不正确;将装置按A、C、B的顺序组合进行实验,当出现___现象时,猜想3是正确的。
实验五:用图所示装置测定碱式碳酸镁[yMg(OH)2xMgCO3]的组成:
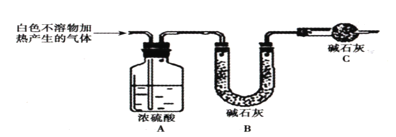
(5)称取干燥、纯净的白色不溶物7.36g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.72g,装置B增重2.64g。装置C的作用是___,白色不溶物的化学式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)为二元弱碱,在水中的电离方式与NH3相似。25℃时,水合肼(N2H4·H2O)的电离常数K1、K2依次为9.55×10-7、1.26×10-15。下列推测或叙述一定错误的是
A.N2H4易溶于水和乙醇
B.N2H4分子中所有原子处于同一平面
C.N2H6Cl2溶液中:2c(N2H![]() )+c(N2H
)+c(N2H![]() )>c(Cl-)+c(OH-)
)>c(Cl-)+c(OH-)
D.25°C时,反应H++N2H4N2H![]() 的平衡常数K=9.55×107
的平衡常数K=9.55×107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某固体有机物![]() 的分子组成,测定装置图所示(夹持仪器、酒精灯等已略去)。
的分子组成,测定装置图所示(夹持仪器、酒精灯等已略去)。

取![]() 放入装置中,通入过量
放入装置中,通入过量![]() 燃烧,生成
燃烧,生成![]() 和
和![]() ,请回答下列有关问题:
,请回答下列有关问题:
(1)通入过量![]() 的目的是_________。
的目的是_________。
(2)![]() 装置的作用是________________,
装置的作用是________________,![]() 装置的作用是___________。
装置的作用是___________。
(3)通过该实验能否确定![]() 中是否含有氧原子________(填“能”或“不能”)。
中是否含有氧原子________(填“能”或“不能”)。
(4)若![]() 的摩尔质量为
的摩尔质量为![]() ,
,![]() 装置增重
装置增重![]() ,
,![]() 装置增重
装置增重![]() ,则
,则![]() 的分子式为________。
的分子式为________。
(5)写出![]() 燃烧的化学方程式:________________。
燃烧的化学方程式:________________。
(6)![]() 可发生水解反应,
可发生水解反应,![]() 可水解生成2种互为同分异构体的产物,且这两种产物均为
可水解生成2种互为同分异构体的产物,且这两种产物均为![]() ,则
,则![]() 在催化剂作用下水解的化学方程式为_____。
在催化剂作用下水解的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将1.0Lcmol/LCH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH 或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是

A. 该温度下,醋酸的电离平衡常数Ka=![]()
B. a点对应的混合溶液中c(CH3COOH)>c(Na+)>c(OH-)
C. 水的电离程度:c>b>a
D. 当混合溶液呈中性时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com