
����Ŀ��ij��ѧ��ȤС��������ͼװ�ý�������ˮ������Ӧ��ʵ�飬�������������ʣ���ش��������⣺

(1)Aװ�õ�������____________����ƿ�ײ������Ƭ��������_________________________��
(2)װ��B�з�����Ӧ�Ļ�ѧ����ʽ��____________________________________���÷�Ӧ����������__________������������__________________��
(3)D��������__________________________________��
(4)E�е�ʵ��������____________________________��
(5)A��B����װ����Ӧ�ȵ�ȼ________________���ľƾ�(��)�ƣ���ȼE���ƾ���֮ǰӦ���еIJ�����________________��
���𰸡�����ˮ���� ��ֹ����ʱҺ�屩�� 3Fe��4H2O(g)![]() Fe3O4��4H2 H2O Fe3O4 ����δ��Ӧ��ˮ�����������H2) ��ɫ�����ɺ�ɫ���������ڱ�����ˮ������ A �ռ�H2�������䴿��
Fe3O4��4H2 H2O Fe3O4 ����δ��Ӧ��ˮ�����������H2) ��ɫ�����ɺ�ɫ���������ڱ�����ˮ������ A �ռ�H2�������䴿��
��������
װ��A��ˮ��������ˮ������B�и�������������ˮ������Ӧ����������������������ˮ�������������������D��������Eװ�ã���CuO��Ӧ����Cu���ʣ�����E֮ǰӦ����ͨ������װ���е������ž�����ֹ������������ϼ��ȷ�����ը���Դ˽����⡣
��1������ˮ������Ӧ�������Ǹ��£�ˮ��״̬�����壬����Aװ�õ������Dz���ˮ��������Ӧ�ڸ��������½��У���ƿ�ײ������Ƭ�����÷�ֹ����ʱҺ�屩�У�
��2��װ��B��������ˮ������Ӧ������������������������Ӧ�ķ���ʽΪ3Fe+4H2O(g)![]() Fe3O4+4H2����Ԫ�ػ��ϼ۽��ͣ��õ����ӣ�ˮ������������Ӧ����Ԫ�ػ��ϼ����ߣ����ǻ�ԭ�����������������������
Fe3O4+4H2����Ԫ�ػ��ϼ۽��ͣ��õ����ӣ�ˮ������������Ӧ����Ԫ�ػ��ϼ����ߣ����ǻ�ԭ�����������������������
��3��E��������ԭ����ͭ��ʵ�飬�������Eװ��ǰҪ����������Σ�գ�Ӳ�ʲ����ܿ���ը�ѣ����D������������δ��Ӧ��ˮ�����������H2)��
��4��������ԭ����ͭ�õ�ͭ��ˮ����H2+CuO![]() Cu+H2O������E�е�ʵ��������Ӳ�ʲ������к�ɫ�����Ϊ��ɫ��Ӳ�ʲ������Ҷ˹ܱ���Һ������
Cu+H2O������E�е�ʵ��������Ӳ�ʲ������к�ɫ�����Ϊ��ɫ��Ӳ�ʲ������Ҷ˹ܱ���Һ������
��5�����ȵ�ȼB���������������ȷ�����Ӧ���������ȵ�ȼA���������ǿ�ȼ��������п����ᷢ����ը�����Ե�ȼE���ƾ���֮ǰӦ���еIJ�������֤�����Ĵ��ȣ������ǣ��ռ�һ�Թ����壬���Թܿڿ����ƾ��ƻ��棬�������۵�������˵�����崿��������������������˵�����岻����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�м�����Ƭ�������������������������ڸ���Һ�п϶��ܴ���������ǣ�������
A.Na+
B.Mg2+
C.CO32��
D.MnO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������¿���ˮ��Ӧ�ƺϳ���(CO��H2)�����Ƴɼ״�����ȼ�͡�
��1��CH4��H2O����������Ԫ�ص縺�Դ�С�����˳��Ϊ________��
��2��CH4��CO2������̼ԭ�ӵ��ӻ����ͷֱ���_____��_______��
��3����̬Niԭ�ӵĵ����Ų�ʽΪ______����Ԫ��λ��Ԫ�����ڱ��ĵ�_____�塣
��4������������CO�����������ȣ�������ɫ�ӷ���Һ̬Ni(CO)4���÷��ӳ��������幹�͡���1molNi(CO)4�к���____mol������Ni(CO)4�ľ�������Ϊ_____��Ni(CO)4����������___(��ѡ����ĸ)�С�
a.ˮ b.������̼ C.�� d.��������Һ
��5����ͼ��һ������Ͻ����ľ����ṹʾ��ͼ���úϽ���ԭ�Ӹ�����La:Ni=_____�������1molLa�ĺϽ������H2����ĿΪ______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ��P4(s)��3NaOH(aq)��3H2O(l)��3NaH2PO2(aq)��PH3(g) ��H��0���Ƶõ�NaH2PO2�����ڻ�ѧ����������˵����ȷ����

A. P4������Pԭ�Ӿ�����8�����ȶ��ṹ
B. ��Ӧ��NaOH����ԭ��
C. �÷�Ӧ���Է����У���S<0
D. ��Ӧ������1 mol NaH2PO2��ת�Ƶ�����ĿΪ3��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1molCH4���������������ܱ������е�ȼ����ַ�Ӧ�������������ʣ�࣬�Ҳ����Ϊ����(101kPa��120��)����������Ϊ72g�������й���������ȷ����
A. ��������ͨ����ʯ�ң����ȫ�����գ���ͨ��Ũ���ᣬ���ܱ���ȫ����
B. �����ƽ��Ħ������Ϊ24g/mol
C. ��������ͨ��Ũ���������պ�ָ���(101kPa��120��)����ѹǿ��Ϊԭ����1/3
D. ��Ӧ�����ĵ�����Ϊ56g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3�������Ϊ1 L�ĺ����ܱ������з�����Ӧ��SO2(g)��2NO(g)![]() 2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶���ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶���ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
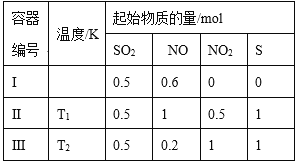
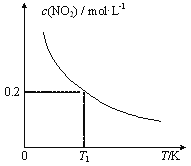
A. �÷�Ӧ����H<0
B. T1ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ![]()
C. ������������������T1ʱ�ﵽƽ�⣬��ѹǿ֮��С��1:2
D. ��T2<T1���ﵽƽ��ʱ����������NO���������С��40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú�ҵ��ۺ����������ڽ�Լ��Դ�������ڱ���������ij��ú�ң���Ҫ��Al2O3��Fe2O3��CaCO3�ȣ������������빤���������£�
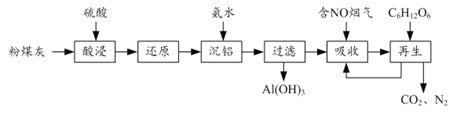
��1���١������ʱAl2O3������Ӧ�����ӷ���ʽΪ______��
�ڵ�����������������50%����������������������½�����ԭ����______��
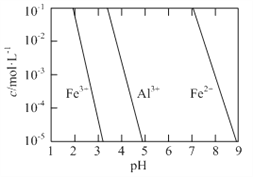
��2���йؽ��������������������ʱ����Ũ����pH�仯��ͼ��ʾ��������Һ������ԭֱ���백ˮ��ϣ�������Ԫ�ط���Ч���ϲ��ԭ����______��
��3������������FeSO4��Һ������������NO���գ���ԭ��ΪFe2++2NO![]() [Fe(NO)2]2+��������O2�����������NO�����ʵ�Ӱ����ͼ��ʾ��
[Fe(NO)2]2+��������O2�����������NO�����ʵ�Ӱ����ͼ��ʾ��
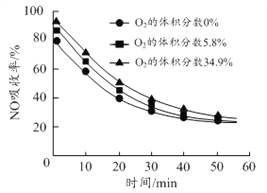
��Ϊ���������NO �������ʣ��ɲ�ȡ�Ĵ�ʩ��______����һ������˵�����ɣ���
�ڡ������������У�[Fe(NO)2]2+���������������C6H12O6������Ӧ�����ӷ���ʽΪ______��
��4��Al(OH)3����һϵ�з�Ӧ�ɻ�ô�������������״̬�������ܶȲ�ͬ��ͨ������Һ��⾫�������ɴ�����øߴ�����װ����ͼ��ʾ����

�ٸ�װ�ù���ʱ���缫A��______����
�����ڴ���ʱ����ͭ��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С������BaS�Ļ�ԭ���ᴿHBr��Һ������ȡ�廯þ�ķ���������
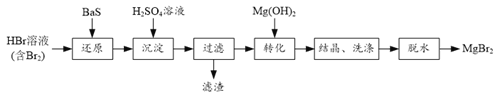
��1�� ����ԭ��������BaS���˹���̫���ԭ����______��
��2�������ijɷ���______��
��3���ᾧ��õ�MgBr2��6H2O���Ҵ�ϴ�ӣ���ϴ��Һ�л����Ҵ���ʵ�鷽����______��
��4��������ͼװ�ý�MgBr2��6H2O��ˮ�õ�MgBr2��
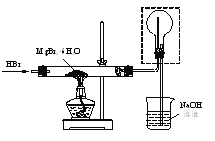
��ͨ��HBr��Ŀ����______��
��ͼ�п���װ�õ�������______��
��5����֪��BaS+H2O2��Ba(OH)2+S�����벹������ʵ������BaS��ȡ�ߴ�BaSO3��ʵ�鷽����ȡBaS��ˮ�������߽�����ڽ���Һ�м������H2O2�����ˣ�______����ʵ������ʹ�����Լ��У�SO2���壬����SO2��ˮ����������������ʹ���������У���ո����䡢pH�ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ�����о�DZˮͧ�й�����ϵ��Ӧ������װ��ͼ(�г�������)��
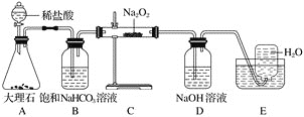
��1��Aװ��ΪCO2�ķ���װ�ã���Ӧ�����ӷ���ʽΪ____________________��
��2��Bװ�ÿɳ�ȥAװ���п��ܻӷ�����___________����Ӧ�����ӷ���ʽΪ_______________��
��3��Cװ��ΪO2�ķ���װ�ã���Ӧ�Ļ�ѧ����ʽΪ__________________��________________��
��4��Dװ�ÿɳ�ȥCװ����δ��Ӧ��__________����Ӧ�����ӷ���ʽΪ____________________��
��5��Eװ��Ϊ��ˮ���ռ�O2��װ�ã��������ռ�������ΪO2�ķ���Ϊ_____________________��
��6��Cװ���й����ɵ���ɫ��ȫ��Ϊ��ɫ���������ɷֵ�ʵ�鷽��Ϊȡ����Cװ���з�Ӧ��Ĺ�������ˮ������Һ�е������___��Һ�����а�ɫ�������ɣ���֤�������к���___�����ˣ�����Һ�е��뼸�η�̪��Һ����__�Ҳ���ɫ����֤�������к���__��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com