
����Ŀ��ij�¶��£���4.0 L�����ܱ������г���2.0 mol PCl5����ӦPCl5(g) ��PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
ʱ��/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
����˵����ȷ����
A����Ӧ��ǰ50 s��ƽ������Ϊv(PCl3)��0.0064 mol/(L��s)
B�������������������䣬�����¶ȣ�ƽ��ʱc(PCl3)��0.11 mol��L��1������Ӧ�ġ�H��0
C����ͬ�¶��£���ʼʱ��������г��� 4.0 mol PCl3��4.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת����С�� 80%
D����ͬ�¶��£���ʼʱ��������г���2.0 mol PCl5��0.40 mol PCl3��0.40 mol Cl2���ﵽƽ��ǰv(��)��v(��)
���𰸡�D
��������
���������A���ɱ������ݿ�֪50s�ڣ���n(PCl3)=0.32mol��v(PCl3)= 0.0016 mol/(L��s)����A����B���ɱ������ݿ�֪��ƽ��ʱn(PCl3)=0.4mol�����������������䣬�����¶ȣ�ƽ��ʱ��c(PCl3)=0.11 mol/L����n��(PCl3)=0.11 mol/L��4L=0.44mol��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ������H��0����B����C��ԭƽ��ʱPCl5ת����Ϊ20%����ЧΪ2.0 mol PCl3��2.0 mol Cl2����ʱPCl3��ת����Ϊ80%��������ʼʱ���� 4.0 mol PCl3��4.0 mol Cl2����ԭƽ����ȣ�ѹǿ����ƽ�����淴Ӧ�����ƶ���ƽ��ʱ��PCl3ת���ʸ���80%����C����
D�����ڿ��淴Ӧ�� PCl5(g)![]() PCl3(g) + Cl2(g)��
PCl3(g) + Cl2(g)��
��ʼ��mol/L����0.5 0 0
�仯��mol/L����0.1 0.1 0.1
ƽ�⣨mol/L����0.4 0.1 0.1
����ƽ�ⳣ��k=![]() =0.025��
=0.025��
��ʼʱ�������г���2.0 mol PCl5��0.40 molPCl3��0.40 molCl2����ʼʱPCl5��Ũ��Ϊ0.5mol/L��PCl3��Ũ��Ϊ0.1mol/L��Cl2��Ũ��Ϊ0.1mol/L��Ũ����Qc=![]() =0.02��K��Qc��˵��ƽ��������Ӧ�����ƶ�����Ӧ��ƽ��ǰv��������v���棩����D��ȷ����ѡD��
=0.02��K��Qc��˵��ƽ��������Ӧ�����ƶ�����Ӧ��ƽ��ǰv��������v���棩����D��ȷ����ѡD��


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼʾΪһ����Ȼ�������һ���ij��ݹ�Ч�������йظû������˵��������ǣ� ��

A.�����к������ֺ���������
B.1mol�û������������6molNaOH��Ӧ
C.�ȿ��Է���ȡ����Ӧ�����ܹ������ӳɷ�Ӧ
D.����FeCl3������ɫ��Ӧ�����ܺ�NaHCO3��Ӧ�ų�CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
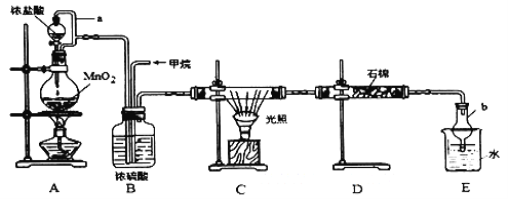
����Ŀ�����ü�������������ȡ����Ӧ��ͬʱ��ø���Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС������ʵ������ģ���������̣�����Ƶ�ģ��װ�����£�
����Ҫ����գ�
����Ҫ����գ�
��1��Aװ�÷�����Ӧ�����ӷ���ʽ��_________________________________��Cװ����CH4��Cl2����һ�ȴ���Ļ�ѧ��Ӧ����ʽ��___________________________ ��
��2������a��������____________������b��������____________��
��3��Dװ���е�ʯ���Ͼ��ȸ��ų�ʪ��KI����������______________ ��
��4��Eװ�õ�������____________��������ţ���
A���ռ����� B���������� C����ֹ���� D�������Ȼ���
��5����װ�õ�ȱ����û�н���β����������β������Ҫ�ɷ���_______.
A��CH4 B��CH3Cl C��CH2Cl2 D��CHCl3 E.CCl4
��6����V(Cl2)/V(CH4)=x,������������������Ȼ���,��xֵӦ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��ʵ��ȼú��������Ļ��գ�SO2(g)��2CO(g) ![]() 2CO2(g)��S(l)����H��0������Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ����(����)
2CO2(g)��S(l)����H��0������Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ����(����)
A.ƽ��ʱ�������������䣬�����¶ȿ���� SO2 ��ת����
B.�����������䣬��С���������ƽ������Ӧ�����ƶ����÷�Ӧ��ƽ�ⳣ������
C.ƽ��ǰ�����������������ѹǿ����Ӧ���ʼӿ�
D.ƽ��ʱ�������������䣬��������淴Ӧ���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5��������Ӧ��PCl5(g)![]() PCl3(g)��Cl2(g)����H=a kJ��mol��1(a��0)��0��10 min���������¶Ȳ��䣬10 minʱ�ı�һ������������������PCl5��PCl3��Cl2�����ʵ�����ʱ��ı仯��ͼ��ʾ��
PCl3(g)��Cl2(g)����H=a kJ��mol��1(a��0)��0��10 min���������¶Ȳ��䣬10 minʱ�ı�һ������������������PCl5��PCl3��Cl2�����ʵ�����ʱ��ı仯��ͼ��ʾ��

����˵����ȷ����
A.0��4 min��ƽ������v(PCl3)=0.025 mol��L��1��min��1
B.10 minʱ�ı��������������һ������PCl5
C.����ʼʱ��������г���2.0 mol PCl3��2.0 mol Cl2�������¶�ΪT����Ӧ��ƽ��ʱ�ų�������С��1.6a kJ
D.�¶�ΪT����ʼʱ��������г���1.0 mol PCl5��0.10 mol PCl3��0.10 mol Cl2����Ӧ�ﵽƽ��ǰv����v��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ���Ȼ����ڶ���A�Ļ����Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��B��C���γ����������εķ��ӣ�D�Ļ�̬ԭ�ӵ������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ���ش��������⣺
��������Ԫ���е縺������Ԫ�صĻ�̬ԭ�ӵļ۵����Ų�ͼΪ______��
����A��B����Ԫ���γɵĻ������У�����Bԭ�Ӳ���sp�ӻ��������������У����е�������������Ŀ֮��Ϊ______��
��DԪ�صij������ӵ�ˮ��Һ��ɫ��ԭ����______���������д��ڵĻ�ѧ����______(a.���Ӽ�b.���ۼ�c.��λ��d.���e.���»���f.������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ�õ�����Ҫ����Դ��
(1)��25����101kPa�£�16g�ļ״�(CH3OH)��ȫȼ������CO2��Һ̬ˮʱ�ų�352kJ�����������ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ______��
(2)��ѧ��Ӧ�зų�������(�ʱ䣬��H)�뷴Ӧ���������ļ���(E)�йء���֪��H2(g)+Cl2(g)=2HCl(g) ��H=��185kJ/mol��E(H��Cl)=432kJ/mol��E(Cl��Cl)=243kJ/mol��E(H��H)=_____��
(3)����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע����֪��2Cu(s)+ ![]() O2(g)�TCu2O(s)��H=��169kJmol��1��C(s)+
O2(g)�TCu2O(s)��H=��169kJmol��1��C(s)+ ![]() O2(g)�TCO(g)��H=��110.5kJmol��1��2Cu(s)+O2(g)�T2CuO(s)��H=��314kJmol��1����ҵ����̿���ڸ��������»�ԭCuO��ȡCu2O��CO���Ȼ�ѧ����ʽ_____��
O2(g)�TCO(g)��H=��110.5kJmol��1��2Cu(s)+O2(g)�T2CuO(s)��H=��314kJmol��1����ҵ����̿���ڸ��������»�ԭCuO��ȡCu2O��CO���Ȼ�ѧ����ʽ_____��
(4)��ͼ��N2(g)��H2(g)��Ӧ����2molNH3(g)�����������仯ʾ��ͼ��
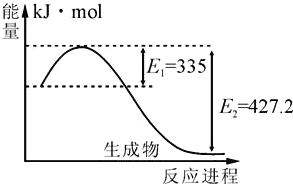
�������ÿ����1molNH3�ų�����Ϊ��______��
������ʼʱ�������ڳ���1molN2��3molH2��ƽ���N2��ת����Ϊ20%����Ӧ�ų�������ΪQ1kJ����Q1����ֵΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�ķ�Ӧ����ʽ����ȷ���ǣ� ��
A. ��̼������Һ�еμӷ�̪��Һ����Һ��죺CO32��+2H2O![]() H2CO3+ 2OH��
H2CO3+ 2OH��
B. ��Na2SΪ����������ȥ��Һ�е�Cu2+��Cu2+ + S2��===CuS��
C. ��AgCl�����еμ�Na2S��Һ����ɫ������ɺ�ɫ��2AgCl+S2��![]() Ag2S+2Cl��
Ag2S+2Cl��
D. ��KI��Һ�еμ�ϡ����͵�����Һ�������ڿ�������Һ������4H++4I��+O2=== 2I2 + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���һͭ����ȼ�ϵ�������ߡ��ɱ��ͣ����й����ķ�չǰ�����õ��ͨ��һ�ָ��ӵ�ͭ��ʴ�����������������зŵ����Ϊ2Li+Cu2O+H2O==2Cu+2Li��+2OH��������˵������ȷ����

A. �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e��=2OH��+2Cu
B. �ŵ�ʱ������������������Li���ƶ�
C. ͨ����ʱ��ͭ�缫����ʴ���������Cu2O
D. ������Ӧ�����У�������ΪO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com