
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,是因为生成了_________气体,继续滴加至液溴滴完。装置d的作用是_________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是_________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是_________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_________,要进一步提纯,下列操作中必须的是____________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是_____________(填入正确选项前的字母):
A.25mL B.50mL C.250mL D.500mL
【答案】(1)HBr;吸收HBr和Br2;(2)除去HBr和未反应的Br2;干燥;(3)苯;C;(4)b。
【解析】试题分析:(1)苯与液溴反应生成HBr,HBr遇水蒸气形成白雾;苯的卤代反应是放热反应,液溴易挥发,所以尾气中有HBr及挥发出的Br2,用氢氧化钠溶液吸收,防止污染大气;(2)制取得到的溴苯中含有未反应的Br2和苯,利用Br2与NaOH可以发生反应:Br2+2NaOH=NaBr+NaBrO+H2O,产生的物质容易溶于水,所以滤液用8mL10%的NaOH溶液洗涤,就是把未反应的Br2变成NaBr和NaBrO洗到水中,除去;向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是干燥溴苯;(3)由于制取得到的粗溴苯中的溴单质被除去,所以经以上分离干燥操作后,粗溴苯中还含有的主要杂质为苯;苯与溴苯是互溶的、沸点不同的液态混合物,分离二者的方法可根据他们沸点的不同,用蒸馏的方法,选项C正确;(4)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴也要进入仪器a中,还向a中加入10mL此时液态物质的体积是15mL+4mL+10mL=29mL,根据液态物质反应时不能超出容器容积的2/3,仪器的规格是50mL烧瓶,选项b正确。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法中正确的是
①常温下,0.1molCl2与足量NaOH溶液反应,转移的电子数目为0.2NA
②常温常压下,18gH2O中含有的电子总数为10NA
③将100 mL 0.1 mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
④在反应KIO3+6HI==KI+3I2+3H2O中,每生成3 mol I2转移的电子数为5NA
⑤常温常压下,14g的C2H4和C4H8混合气体中含有的原子数为3NA
⑥在标准状况下,0.5molNO与0.5molO2混合后气体分子数为0.75 NA
⑦1.0L 1.0 mol·L-1 Na2SiO3水溶液中含有的氧原子数为3NA
A.①⑤⑦ B.③④⑥
C.②④⑤ D.②③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐中含有杂质CaCl2,一学生设计了如下实验方法分离NaCl和CaCl2:

填空和回答下列问题:
(1)写出生成B物质的化学方程式 。
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 (填字母或化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种新型净水剂,制取Na2FeO4的离子方程式为:Fe3+ + OH—+ Cl2 → FeO42—+ Cl— + H2O,该反应配平的离子方程式中H2O的系数是
A.4 B.6 C.8 D.10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.

(1)写出下列仪器的名称:① ②
(2)仪器①~④中,使用时必须检查是否漏水的有 .(填序号)
(3)若利用装置I分离丙三醇(能跟水、酒精以任意比互溶,沸点290℃)和酒精(沸点78.2℃)的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为; .进水方向是 (填g或f),还需加入少量碎瓷片,其作用是 .
(4)如图所示装置Ⅱ是转移操作,请指出该操作错误之处:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内含量极少,但必不可少的化学元素有( )
A. Fe Mn Zn Mg
B. Zn Cu Mn Ca
C. H 0 Na Mg
D. Zn Cu B Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(g)![]() 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等②单位时间生成amolA,同时消耗1.5molB;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2: 3: 2.
A. ⑤⑥⑧ B. ②⑤⑧ C. ①③④ D. ②④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别取40mL的0.50mol/L盐酸与40mL0.55mol/L氢氧化钠溶液进行中和热的测定.下列说法错误的是( )

A.稍过量的氢氧化钠是确保盐酸完全反应
B.仪器A的名称是环形玻璃搅拌棒
C.在实验过程中,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度
D.用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,结果也是正确的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol/Ls溶液的pH为12。上述物质的转化关系如图所示。下列说法正确的是
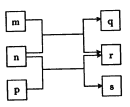
A. 离子半径:X>Y>Z
B. 氧化性:r>m
C. p和q中均含有离子键
D. 等体积等浓度的q溶液与s溶液反应后,溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com