
【题目】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大.A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒.
(1)A元素的第一电离能 B元素的第一电离能(填“<”“>”或“=”),A、B、C三种元素电负性由小到大的顺序为 (用元素符号表示).
(2)D元素原子的价电子排布式是 .
(3)C元素的电子排布图为 ;E3+的离子符号为 .
(4)F元素位于元素周期表的 区,其基态原子的电子排布式为 .
(5)G元素可能的性质 .
A.其单质可作为半导体材料
B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸.
【答案】(1)>; N<O<F;
(2)3s2;
(3)![]() ; Fe3+;
; Fe3+;
(4)ds; 1s22s22p63s23p63d104s1或[Ar]3d104s1;
(5)A.
【解析】试题分析:A元素的价电子构型为nsnnpn+1,n=2,A为N元素,C元素为最活泼的非金属元素,C为F元素,则B为O元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,应为Mg元素,E元素正三价离子的3d轨道为半充满状态,则原子序数为26,为Fe元素,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,为Cu元素,G元素与A元素位于同一主族,其某种氧化物有剧毒,为As元素,以此解答该题.
解:A元素的价电子构型为nsnnpn+1,n=2,A为N元素,C元素为最活泼的非金属元素,C为F元素,则B为O元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,应为Mg元素,E元素正三价离子的3d轨道为半充满状态,则原子序数为26,为Fe元素,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,为Cu元素,G元素与A元素位于同一主族,其某种氧化物有剧毒,为As元素,
(1)N原子最外层为半充满状态,性质稳定,难以失去电子,第一电离能大于O元素,同周期元素从左到右元素的电负性逐渐增强,即 N<O<F,
故答案为:>; N<O<F;
(2)D为Mg元素,最外层电子数为2,价电子排布式为3s2,故答案为:3s2;
(3)C为F元素,电子排布图为![]() ,E3+的离子符号为 Fe3+,
,E3+的离子符号为 Fe3+,
故答案为:![]() ; Fe3+;
; Fe3+;
(4)F为Cu,位于周期表ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,故答案为:ds; 1s22s22p63s23p63d104s1或[Ar]3d104s1;
(5)G为As元素,与Si位于周期表对角线位置,其单质可作为半导体材料,电负性比P小,因磷酸为中强酸,则As的最高价氧化物对应的水化物是弱酸,
故答案为:A.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
![]()
下列说法中不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg﹣AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是
A.负极反应式为Mg﹣2e﹣=Mg2+
B.正极反应式为Ag++e﹣=Ag
C.电池放电时Cl﹣由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与材料、生活和环境密切相关。下列有关说法中错误的是( )
A.某新型航天服材料主要成分是由碳化硅、陶瓷和碳纤维复合而成,它是一种新型无机非金属材料
B.玛瑙饰品的主要成分与建筑材料砂子相同
C.明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒的作用
D.医用酒精是利用了乙醇的氧化性来杀菌消毒的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某混合物的无色透明溶液,可能含有以下离子中的若干种:
Na+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:
①第一份加入足量AgNO3溶液有沉淀产生,加足量稀硝酸后沉淀部分溶解;
②第二份加足量NaOH溶液充分加热后,收集到气体0.896L(标准状况);
③第三份加足量BaCl2溶液后,过滤后充分干燥得到沉淀6.27g,再经足量稀硝酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验现象和有关数据,回答下列问题:
(1)原溶液中一定存在的阴离子是 ,一定不存在的离子是 ,可能存在的离子是 。
(2)②中发生化学反应的离子方程式为 。
(3)③中生成可溶于稀硝酸的沉淀化学式为 ,物质的量为 mol,该沉淀溶于稀硝酸的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 向鸡蛋清的溶液中加入饱和硫酸钠溶液,鸡蛋清因发生变性而沉淀析出
B. 溶液和胶体的鉴别可利用丁达尔效应
C. 进行焰色反应时,铂丝需用稀硫酸洗净,并在火焰上灼烧至无色
D. 水晶和陶瓷的主要成分都是硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线画出.
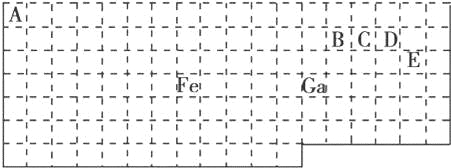
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为
(2)铁元素位于元素周期表的 区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为 .
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征.与CO互为等电子体的分子和离子分别为 和 (填化学式).
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 .
(5)根据VSEPR模型预测ED4﹣的空间构型为 .B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子为 (写2种).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
①铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
②往FeCl3溶液中加入Fe粉:2Fe3++Fe =3Fe2+
③氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O
④氯化铁水解:Fe3+ +3H2O = Fe(OH)3↓+ 3H+
⑤氯化亚铁溶液中加入氯水:Fe2++C12=Fe3++2C1-
⑥钾投入水中:2K+2H2O = 2K++2OH-+H2↑
⑦Na2CO3溶液中通入过量CO2:CO![]() +CO2+H2O = 2HCO
+CO2+H2O = 2HCO![]()
⑧NaHCO3溶液显碱性:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
⑨硫酸铝溶液中加入过量氨水: Al3++3OH—═Al(OH)3↓
⑩烧碱溶液中加入铝片:2Al+2OH-+2H2O=2AlO2-+3H2↑
A.①③⑤⑦ B.②④⑥⑧ C.②④⑤⑨ D.②⑥⑦⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题8分)
(1)化合物A的结构简式为: ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_________;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_________;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为________。
(2)篮烷分子的键线式如图所示,试回答:

①写出篮烷分子的化学式____________
②篮烷分子的一氯取代物是种数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com