
【题目】在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)![]() 2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )
2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )
A.等于5sB.等于10sC.小于10sD.大于10s
 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】如图为向25mL 0.1mol·L1NaOH溶液中逐滴滴加0.2mol·L1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
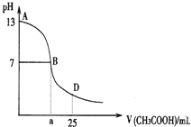
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?(选填“是”或“否”)_________.若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?__________________(若正确,此问不答)
(2)AB区间,c(OH)>c(H+),则c(OH)与c(CH3COO)大小关系是_______________
A.c(OH)一定大于c(CH3COO) B.c(OH)一定小于c(CH3COO)
C.c(OH)一定等于c(CH3COO) D.c(OH)大于、小于或等于c(CH3COO)
(3)在D点时,溶液中c(CH3COO)+c(CH3COOH)_________2c(Na+)(“>”、“<”或“=”)
(4)常温下,将VmL、0.1000mol·L1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L1醋酸溶液中,充分反应。回答下列问题.(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值____________20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO)、c(H+)、c(OH)的大小关系为________________________.
②如果V=40.00,则此时溶液中c(OH)c(H+)c(CH3COOH)=__________________mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极 上析出6.4g某金属,下列说法正确的是
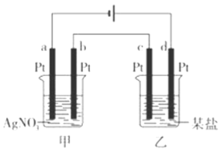
A.甲池是b极上析出金属银,乙池是c极上析出某金属
B.甲池是a极上析出金属银,乙池是d极上析出某金属
C.某盐溶液可能是CuSO4溶液
D.某盐溶液可能是Mg(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是()
实验目的 | 实验操作 | |
A | 除去MgCl2溶液中的少量FeCl3 | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后,过滤 |
B | 验证乙醇和浓硫酸可以制备乙烯 | 乙醇和浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 |
C | 比较HClO和CH3COOH酸性 | 用pH试纸测定浓度均为0.1mol/L的HClO溶液和CH3COOH溶液的pH |
D | Mg(OH)2可溶解于饱和NH4Cl溶液 | 将NH4Cl固体与Mg(OH)2混合 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照要求填写下列内容 :
(1)1molH2的质量是_________。
(2)已知0.5mol某气体分子的质量为16 g,则该气体的摩尔质量是_________。
(3)NA个氨气分子(NH3)中含_________mol原子。
(4)等质量的氧气和臭氧,它们原子的个数之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1
B. 由图甲推断,A点对应温度下该反应的平衡常数为800(L·mol-1)
C. 达平衡后,若增大容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
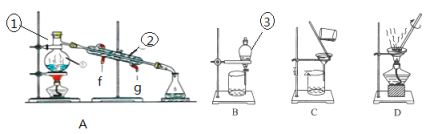
(1)写出下列仪器的名称:① __________②____________。
(2)仪器③中使用前必须检查是否_________________。
(3)若利用装置A分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的一种仪器名称为__________。冷凝管中冷凝水应从____(填“f”或“g”)口进,在①中注入液体混合物后,加几片碎瓷片的目的是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或模型正确的是
A. 苯分子的比例模型:
B. CO2的电子式:![]()
C. Cl-离子的结构示意图:
D. 乙烯的结构式:CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们的物质生活水平的不断提高和工业化快速发展,环境污染也日益加重,空气中有毒气体主要包括SO2、CO、NOx、烃类等等。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和水。已知CH4和S的燃烧热ΔH分别为-890 kJ/mol和-297kJ/mol,则CH4和SO2反应的热化学方程式为_______________。
(2)在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH。测得CO的转化率随温度及不同压强的变化如图所示,P2和195 ℃时n(H2)随时间的变化结果如表所示。
CH3OH(g) ΔH。测得CO的转化率随温度及不同压强的变化如图所示,P2和195 ℃时n(H2)随时间的变化结果如表所示。
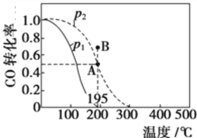
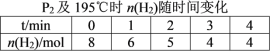
①P2及195℃下,在B点时,v(正)_____v(逆)(填“>”、“<”或“=”)。
②该反应的ΔH_________0(填“>”、“<”或“=”),原因是______________________________。
③在0~2 min,平均反应速率v(H2)=______________________。(数值用小数形式表示)
④在P2及195 ℃时,该反应的平衡常数Kp=__________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果用含P2的分式表示)。
(3)某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见图所示。
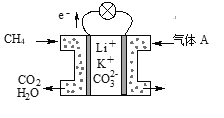
①气体A中除了O2外,一定还含有的气体是________。
②该电池的负极反应式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com