
【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。
(1)已知25℃时,存在以下反应:
①N2(g)+O2(g) ![]() 2NO(g) △H1=+183 kJ·mol-1
2NO(g) △H1=+183 kJ·mol-1
②2H2(g)+O2(g)=2H2O(1) △H2=-571. 6 kJ·mol-1
③4NH3(g)+5O2(g) =4NO(g)+6H2O(1) △H3=-1164.4 kJ·mol-1
则合成氨的反应N2(g)+3H2(g)![]() 2NH3(g) △H=____________kJ·mol-1。
2NH3(g) △H=____________kJ·mol-1。
(2)在恒温恒容容积为1 L的密闭容器中进行合成氨的反应,起始加入N2:1.0 mol、H2:3.0 mol。
①该温度下合成氨反应的平衡常数表达式为__________________。
②若其它条件不变增大压强,则合成氨反应的化学平衡常数_____________(填“变大”、“变小”或“不变”);
③经过2min达到化学平衡状态时测得H2的浓度为1.8mol/L,则平均化学反应速率v(NH3)_____________,氢气的转化率为________________。
④下图表示合成氨反应中H2 (g)的平衡转化率随温度的变化关系,判断P1_____P2(填“>”“ <”或“ = ”),并简述理由:__________________。

【答案】 -92.2 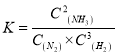 不变 0.4 mol·L-1·min-1 40% < 当温度一定时,压强越大,平衡正向移动,氢气转化率越大
不变 0.4 mol·L-1·min-1 40% < 当温度一定时,压强越大,平衡正向移动,氢气转化率越大
【解析】(1)已知反应①N2(g)+O2(g) ![]() 2NO(g) △H1=+183 kJ·mol-1;②2H2(g)+O2(g)=2H2O(1)△H2=-571. 6 kJ·mol-1;③4NH3(g)+5O2(g) =4NO(g)+6H2O(1) △H3=-1164.4 kJ·mol-1。由①+②
2NO(g) △H1=+183 kJ·mol-1;②2H2(g)+O2(g)=2H2O(1)△H2=-571. 6 kJ·mol-1;③4NH3(g)+5O2(g) =4NO(g)+6H2O(1) △H3=-1164.4 kJ·mol-1。由①+②![]() -③
-③![]() 得,N2(g)+3H2(g)
得,N2(g)+3H2(g)![]() 2NH3(g),则合成氨的反应的△H=(+183 kJ·mol-1)+
2NH3(g),则合成氨的反应的△H=(+183 kJ·mol-1)+ ![]() (-571. 6 kJ·mol-1)-
(-571. 6 kJ·mol-1)- ![]() (-1164.4 kJ·mol-1)= -92.2 kJ·mol-1。
(-1164.4 kJ·mol-1)= -92.2 kJ·mol-1。
(2)在恒温恒容容积为1 L的密闭容器中进行合成氨的反应,起始加入1.0 mol N2和3.0 mol H2,则N2和H2的起始浓度分别为1.0 mol/L和3.0 mol/L。
①该温度下合成氨反应的平衡常数表达式为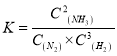 。
。
②化学平衡常数只与温度有关,若其它条件不变增大压强,则合成氨反应的化学平衡常数不变;
③经过2min达到化学平衡状态时测得H2的浓度为1.8mol/L,则平均化学反应速率v(NH3)=![]() v(H2)=
v(H2)=![]() mol·L-1·min-1 =0.4 mol·L-1·min-1 ,氢气的转化率为
mol·L-1·min-1 =0.4 mol·L-1·min-1 ,氢气的转化率为![]() 。
。
④合成氨反应是一个气体分子数减少的反应,在相同温度下,压强越大,反应物的转化率越大。由图可知,在相同温度下,压强为P2对应的氢气的转化率较大,因此可以判断P1 < P2。


科目:高中化学 来源: 题型:
【题目】某超市中一种电池外壳的纸层包装上印有如图所示的文字,根据要求回答:
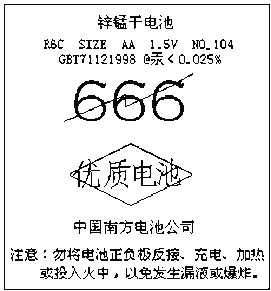
(1)该电池的种类是______(填序号).
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是______(写元素符号).
(3)该电池的使用和性能,下列说法中不正确的是______
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极___________________________________
正极___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B和C为短周期元素,原子序数依次减小,A的最低负化合价为﹣2,无最高正价,B是空气中含量最高的元素,C最外层电子数与电子层数相等.回答下列问题:
(1)A、B和C分别为、、(用元素名称表示).
(2)由以上元素组成的化合物中,属于离子化合物的是 , 属于共价化合物的是 . (各写一种即可)
(3)B的常见气态氢化物的电子式为 , B的常见气态氢化物与其最高价氧化物对应的水化物反应产物的阳离子含有(填化学键的种类),该离子氯化物的水溶液呈性,用离子方程式表示为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对危险化学品要在包装标签上印有警示性标志。下列化学药品名称与警示标志名称对应正确的是( )
A.浓硫酸——腐蚀品B.酒精——剧毒品
C.汽油——爆炸品D.烧碱——剧毒品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益,其分子结构如图所示.下列说法不正确的是 ( ) 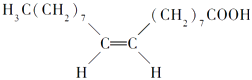
A.油酸的分子式为C18H34O2
B.油酸可与氢氧化钠溶液发生中和反应
C.1mol油酸可与2molH2发生加成反应
D.1mol甘油可与3mol油酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各电离方程式中,书写正确的是( )
A.H2S2H++S2﹣
B.KHSO4K++H++SO42﹣
C.Al(OH)3Al3++3OH﹣
D.HClO═H++ClO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 某实验小组对H2O2的分解做了如下探究。下表是研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 mL5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮,但木条未复燃 | 30min |
(1)该反应是_________反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与_____________________有关。
Ⅱ.某可逆反应在体积为5L的密闭容器中进行,在从0—3分钟各物质的物质的量变化情况如图所示(A、B、C均为气体)。

(3)该反应的的化学方程式为_____________。
(4)反应开始至2分钟时,B的平均反应速率为__________。
(5)能说明该反应已达到平衡状态的是_________。
A.v(A)= 2v(B) B.容器内压强保持不变
C.v逆(A)= v正(C) D.容器内混合气体的密度保持不变
(6)由图求得A的平衡时的转化率为__________。
Ⅲ.已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如下表:
共价键 | H—H | N—H | N≡N |
能量变化/kJ·mol-1 | 436 | 390.8 | 946 |
则合成氨反应:N2(g) + 3H2(g)= 2NH3(g) ![]() H = ____________kJ·mol-1。
H = ____________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T3℃时,将A、B、C三种物质分别溶于100克水中,制成饱和溶液.这三种物质的溶解度随温度而变化的曲线如图.从T3降至T1 , 下列有关说法正确的是( ) 
A.T3℃时,由A物质所形成的溶液的物质的量浓度最大
B.T2℃时,由A、C两物质形成的溶液质量分数相等
C.T1℃时,由B物质所形成的溶液质量分数最大,C的最小
D.从溶解度曲线可知分离A、C的混合溶液得到A可采用蒸发结晶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com