
【题目】在日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为( )
A. 元素 B. 单质 C. 分子 D. 氧化物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列反应中说明NH3既有还原性,又有碱性的是( )
A. 4NH3+5O2![]() 4NO+6H2O B. NH3+HNO3=NH4NO3
4NO+6H2O B. NH3+HNO3=NH4NO3
C. 8NH3+3Cl2=N2+6NH4Cl D. 2NH3+3CuO![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 用硝酸银溶液检验自来水中的氯离子:Ag++Cl-=AgCl↓
B. 实验室用碳酸钙与稀盐酸反应制备二氧化碳:CO32-+2H+=H2O+CO2↑
C. 用稀硫酸清洗铁锈(氧化铁):Fe2O3+6H+=2Fe3++3H2O
D. 用MnO2和浓盐酸反应制备Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需配制500mL 0.2mol/L Na2SO4溶液,实验操作步骤为:
A.把制得的溶液小心地转移至容量瓶中。
B.在天平上称取14.2g 硫酸钠固体,把它放在烧杯中,用适量的蒸馏水将它完全溶解并冷却至室温。
C.继续向容量瓶中加蒸馏水至液面距刻度1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
⑴操作步骤的正确顺序为___________(填序号)。
⑵本实验用到的基本仪器除烧杯、天平(砝码、镊子)、玻璃棒外,还有___________。
⑶下列情况中,会使所配溶液浓度偏低的是___________。
A.某同学观察液面时仰视 B.没有进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线 D.容量瓶使用前内壁沾有水珠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,下列各组气体既能大量共存又能用浓硫酸干燥的是
A.NO、O2、N2B.HCl、H2、O2
C.NH3、O2、CO2D.CO2、H2S、SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水
利用下图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的主要玻璃仪器有烧杯、玻璃棒、________________________。
(2)若对调B和C装置的位置,________(填“能”或 “不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20 mol·L-1 KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol·L-1 H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是__________________________________________。
②若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案:使用下图装置,加热15.0 mL 饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是______________________________________。
(不考虑实验装置及操作失误导致不可行的原因)

(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节): ______________。
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯气可被SO2、H2O2、FeCl2等物质还原成Cl-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,相关物质间的关系如下图所示。

(1)H的化学式是______________。
(2)反应①的化学方程式是____________________________。
(3)反应②的离子方程式是____________________________。
(4)检验F溶液中金属阳离子的操作和现象是____________________________。
(5)H转化为G的实验现象是__________________________________________。
(6)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是_______(填下图字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是
A. 常温下溶解度:Na2CO3<NaHCO3
B. 热稳定性:Na2CO3<NaHCO3
C. 与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D. 与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() ,有机玻璃可按下列路线合成:
,有机玻璃可按下列路线合成:
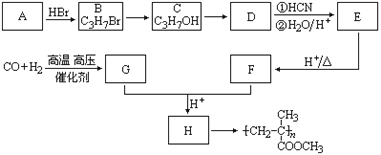
试写出:
(1)A、E的结构简式分别为:___________________、______________________。
(2)B→C、E→F的反应类型分别为:________________、________________。
(3)写出下列转化的化学方程式:C→D___________________________________________;G+F→H___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com