
【题目】A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,相关物质间的关系如下图所示。

(1)H的化学式是______________。
(2)反应①的化学方程式是____________________________。
(3)反应②的离子方程式是____________________________。
(4)检验F溶液中金属阳离子的操作和现象是____________________________。
(5)H转化为G的实验现象是__________________________________________。
(6)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是_______(填下图字母)

【答案】Fe(OH)2 Fe2O3+2Al ![]() Al2O3+2Fe Fe+2Fe3+=3Fe2+ 取2mL F溶液于试管中,加入K3Fe(CN)6溶液,生成特征的蓝色沉淀,则F溶液中金属阳离子为Fe2+ 白色沉淀迅速变成灰绿色,最终变成红褐色 B
Al2O3+2Fe Fe+2Fe3+=3Fe2+ 取2mL F溶液于试管中,加入K3Fe(CN)6溶液,生成特征的蓝色沉淀,则F溶液中金属阳离子为Fe2+ 白色沉淀迅速变成灰绿色,最终变成红褐色 B
【解析】
A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,则反应①为铝热反应,所以A为Al,D为Fe,C为Al2O3,B为铁的氧化物,D与硫酸反应生成F为FeSO4,F与氢氧化钠反应生成H为Fe(OH)2,H氧化得G为Fe(OH)3,所以E为Fe2(SO4)3,则B为Fe2O3,据此答题。
据上所述可知:A是Al,B Fe2O3,C是Al2O3,D是Fe;E是Fe2(SO4)3,F是FeSO4,G是Fe(OH)3,H是Fe(OH)2。
(1)根据上面的分析可知,H的化学式是Fe(OH)2;
(2)反应①的化学方程式是 Fe2O3+2Al![]() Al2O3+2Fe;
Al2O3+2Fe;
(3)反应②为硫酸铁与铁反应生成硫酸亚铁,该反应的离子方程式是Fe+2Fe3+=3Fe2+;
(4)F是FeSO4,检验F溶液中金属阳离子Fe2+的方法是取2mL F溶液于试管中,加入K3Fe(CN)6溶液,若生成特征的蓝色沉淀,则证明F溶液中金属阳离子为Fe2+;
的操作和现象是
(5)H是Fe(OH)2,G是Fe(OH)3,Fe(OH)2不稳定,容易被空气中的氧气氧化产生Fe(OH)3,该反应的化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3,看到的现象是产生的沉淀由白色迅速变成灰绿色,最终变成红褐色;
(6)为了更清楚地观察到生成Fe(OH)2的现象,使FeSO4的溶液与NaOH溶液反应的正确操作是在FeSO4溶液的液面上覆盖一层煤油,以隔绝空气,然后将吸有NaOH溶液的长胶头滴管伸到液面以下再滴加NaOH溶液,这样就可以减少与氧气接触,从而可防止Fe(OH)2被氧化产Fe(OH)3,因此合理选项是B。


科目:高中化学 来源: 题型:
【题目】在日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为( )
A. 元素 B. 单质 C. 分子 D. 氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
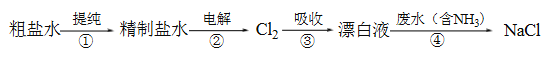
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中:①饱和食盐水 ②CaCO3 ③酒精 ④NH3 ⑤Al ⑥KOH ⑦液态HCl,能导电的有______,属于电解质的有______(填编号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙_________,F__________。
(2)写出下列反应的离子方程式:
①金属A和水反应_______________。②红褐色沉淀C与物质E反应__________。
③F与黄绿色气体乙反应____________。
④实验室常用氢氧化钠吸收实验过程中的黄绿色气体乙,写出用氢氧化钠溶液吸收该气体的离子方程式___。
(3)将G溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在______之间,验证的简单方法是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A标准状况下的密度为1.16 g·Lˉ1,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。F为有浓郁香味,不易溶于水的油状液体。

请回答:
(1)A的结构简式________________。
(2)D+E→F的反应类型是__________。
(3)有机物A转化为B的化学方程式是___________________________________。
(4)下列说法正确的是_________。
A.有机物E与金属钠反应比水与金属钠反应要剧烈。
B.有机物E与金属钠反应的产物可以与水反应重新生成E。
C.有机物D、E、F可用饱和Na2CO3溶液鉴别。
D.上述转化关系图中共涉及3次加成反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com