
����Ŀ��ij�¶��£�H2��g��+CO2 ��g��H2O��g��+CO��g����ƽ�ⳣ��K= ![]() �����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2 ��g����CO2 ��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ�������
�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2 ��g����CO2 ��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ�������
��ʼŨ�� | �� | �� | �� |
c��H2��/molL��1 | 0.010 | 0.020 | 0.020 |
c��CO2��/molL��1 | 0.010 | 0.010 | 0.020 |
A.ƽ��ʱ������CO2��ת���ʴ���60%
B.ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C.ƽ��ʱ������c��CO2���Ǽ��е�2������0.008 molL��1
D.��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
���𰸡�D
�����������ڼ�������
H2��g��+ | CO2��g�� | H2O��g��+ | CO��g�� | |
��ʼ��mol/L�� | 0.01 | 0.01 | 0 | 0 |
ת����mol/L�� | x | x | x | x |
ƽ�⣨mol/L�� | 0.01-x | 0.01-x | x | x |
���� ![]() =
= ![]() �����x=0.006��
�����x=0.006��
A�������������֪���������ڶ�����̼��ת����Ϊ ![]() ��100%=60%�����º����£�������������ʼŨ�ȱȼ�����������ʼŨ�ȴ����ж�����̼��ת���ʱȼ��иߣ���ƽ��ʱ������CO2��ת���ʴ���60%����A���������⣻
��100%=60%�����º����£�������������ʼŨ�ȱȼ�����������ʼŨ�ȴ����ж�����̼��ת���ʱȼ��иߣ���ƽ��ʱ������CO2��ת���ʴ���60%����A���������⣻
B���ס�������������ʼŨ��n��H2����n��CO2��=1��1����ӦH2��g��+CO2��g��H2O��g��+CO��g��ǰ�������������䣬���º����£��ס���Ϊ��Чƽ�⣬ƽ��ʱ�ס�����H2��ת���ʾ���ȣ������������֪����������������ת����Ϊ ![]() ��100%=60%����B���������⣻
��100%=60%����B���������⣻
C�������������֪��ƽ��ʱ��������c��CO2��=��0.01��x ��mol/L=0.004mol/L���ס���Ϊ��Чƽ�⣬ƽ��ʱ���ס�����CO2��ת������ȣ���A�м����֪Ϊ60%����ƽ��ʱ��������c��CO2��=0.02mol/L����1��60%��=0.008mol/L������c��CO2���Ǽ��е�2������C���������⣻
D��Ũ��Խ��Ӧ����Խ�죬�ɱ������ݿ�֪���ס��������ڣ���ʼCO2Ũ����ȣ�����H2Ũ�ȱȼ���Ũ�ȴ����������ң��ף��ҡ��������ڣ���ʼH2Ũ����ȣ�����CO2Ũ�ȱ�����Ũ�ȴ��������ʱ����ң������ʱ����ң��ף���D�������⣬
���Դ��ǣ�D��
�����㾫����������Ĺؼ��������⻯ѧƽ��ļ�������֪ʶ�����շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������SO42��ʱ��ѡ�õ��Լ���˳�����������( )
A.ϡ���ᡢBaCl2��ҺB.ϡ���ᡢBaCl2��Һ
C.Ba(NO3)2��Һ��ϡ����D.BaCl2��Һ��ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B����ԭ�ӣ�A��M���Ӳ��B��M���Ӳ���3�����ӣ�B��L���Ӳ������ǡΪA��L���Ӳ��������2����A��B�ֱ��� (����)��
A. ��ԭ�Ӻ���ԭ��B. ��ԭ�Ӻͺ�ԭ��
C. ��ԭ�Ӻ�̼ԭ��D. ̼ԭ�Ӻ���ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ��������������ʵ�ֵ���
A.H2O2��O2 B.HCl��Cl2C.H2SO4 ��BaSO4D.CuO��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������ȷ�Ӧʵ��չ���о������и��л�ѧ�̲��ж������ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â������ֽ©�����²����մ���������������ɳ���������ġ���ѧ�ֲᡷ֪��Al��Al2O3��Fe��Fe2O3�۵㡢�е��������£�
���� | Al | Al2O3 | Fe | Fe2O3 |
�۵�/�� | 660 | 2054 | 1535 | 1462 |
�е�/�� | 2467 | 2980 | 2750 | -- |
������1��ijͬѧ�Ʋ⣬���ȷ�Ӧ���õ���������Ӧ�������Ͻ������ǣ��÷�Ӧ�ų�������ʹ���ۻ����������۵�����ͣ���ʱҺ̬���������ۺ��γ������Ͻ�����Ϊ���Ľ����Ƿ��������_____ ��������������������������
��2�����һ����ʵ�鷽����֤���������õĿ�״�������к��н���������ʵ�������Լ���_____ ����Ӧ�����ӷ���ʽΪ____ __��
��3��ʵ�����ܽ������������Լ�����õ���___ ___������ţ���
A��Ũ���� B��ϡ���� C��ϡ���� D������������Һ
����ʵ���о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������������������һ������ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���4molL-1������������Һ����������������Һ�������mL��������ij��������ʵ�����mol���Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
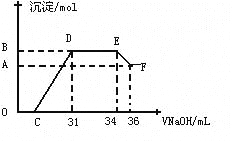
��4��ͼ��OC��û�г������ɣ��˽η�����Ӧ�����ӷ���ʽΪ____ __
��5����DE�Σ����������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ____ _ ����������˵����Һ��_____ _���OH����������___ ___ǿ�������ӷ��ţ���
��6��B���Ӧ�ij��������ʵ���Ϊ____ __mol��C���Ӧ������������Һ�����Ϊ____ __mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ����������ϵ���

A. ͼ�ױ�ʾȼ��ȼ�շ�Ӧ�������仯
B. ͼ�ұ�ʾø����Ӧ�ķ�Ӧ�����淴Ӧ�¶ȵı仯
C. ͼ����ʾ���淴Ӧ�Ӽ��뷴Ӧ�↑ʼ������ѧƽ��Ĺ���
D. ͼ����ʾ��NH3ͨ�������Һ�Ĺ����У���Һ�����Եı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���л���A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������AΪ��Ҫԭ�Ϻϳ�������������ϳ�·����ͼ��ʾ��

��1��B�еĺ�������������Ϊ______��
��2����Ӧ�ٵķ�Ӧ������______��
��3����Ӧ�ڵĻ�ѧ����ʽ��______��
��4��ijѧ����ͼ��ʾ��ʵ��װ����ȡ��������������ʵ��������Թܼ����ϲ�Ϊ���ġ�������ˮ����״Һ�塣

���Թܼ��еĵ��ܲ����뱥��Na2CO3��Һ��Һ�����µ�ԭ����______��
����������Թܼ��е���״Һ�壬����ʹ�õIJ���������______��
��5������������˵���Ҵ��������������Ӧ�Ѵﵽ��ѧƽ��״̬����______������ţ���
a��������и����ʵ�Ũ�Ȳ��ٱ仯
b����λʱ�������1mol�Ҵ���ͬʱ����1mol����
c����λʱ�������1mol����������ͬʱ����1mol�Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������ͬλ�ص���
A.16O��18OB.H2O��D2OC.H2��D2D.24Mg��24Na
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ոմ�ũҵѧԺ��ҵ��С������������ѧ��֪ʶ��ũ������������������Ƶ�����Һ�к���Mg2+��K+��Ca2+��Zn2+����Ũ�ȶ���0��1molL��1������һ��ʱ�������Һ��ʣ�������� �� ��
A��Ca2+ B��Mg2+ C��Cu2+ D��K+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com