
【题目】工业上常用绿柱石(主要成分3BeOAl2O36SiO2,还含有铁元素)冶炼铍,其简化的工艺流程如图所示:
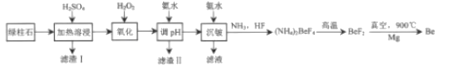
已知:Be和Al性质相似:几种金属阳离子的氢氧化物沉淀时的pH如表:
Be2+ | Al3+ | Fe3+ | Fe2+ | |
开始沉淀时 | 5.2 | 3.3 | 1.5 | 6.5 |
沉淀完全时 | 8.8 | 5.0 | 3.7 | 9.7 |
回答下列问题:
(1)滤渣Ⅰ的主要成分是______,加入H2O2的作用是______。
(2)得到滤渣Ⅱ的合理pH范围是______。
(3)用化学方程式解释不宜使用NaOH溶液来沉铍的原因是______。
(4)得到(NH4)2BeF4的化学方程式为______。
(5)由Mg还原BeF2得到Be需要真空的环境,其原因是______。
(6)若绿柱石中BeO的含量为a%,1吨绿柱石能生产含铍2%的合金b吨,则Be的利用率为______。(用含a、b的表达式表示)
【答案】H2SiO3或SiO2 将Fe2+氧化成Fe3+ 5.0≤pH<5.2或5.0~5.2 Be(OH)2+2NaOH=Na2BeO2+2H2O Be(OH)2+2NH3+4HF=(NH4)2BeF4+2H2O 防止Mg、Be高温下与N2、O2等气体发生反应 ![]()
【解析】
绿柱石中加入稀硫酸,得到滤液中含有Be2+、Al3+、SO42-、含铁元素的离子,SiO2不与稀硫酸反应,且不溶于稀硫酸,或者绿柱石中SiO32-与H+反应生成H2SiO3沉淀,即滤渣1主要成分是H2SiO3或SiO2,向滤液中加入H2O2,利用H2O2的氧化性,将Fe2+转化成Fe3+,便于后续操作除去,根据流程,加入氨水调节pH,除去Al3+、Fe3+,过滤后加入氨水,使Be元素转化成Be(OH)2沉淀,然后让Be(OH)2、NH3、HF反应生成(NH4)2BeF4,据此分析;
绿柱石中加入稀硫酸,得到滤液中含有Be2+、Al3+、SO42-、含铁元素的离子,SiO2不与稀硫酸反应,且不溶于稀硫酸,或者绿柱石中SiO32-与H+反应生成H2SiO3沉淀,即滤渣1主要成分是H2SiO3或SiO2,向滤液中加入H2O2,利用H2O2的氧化性,将Fe2+转化成Fe3+,便于后续操作除去,根据流程,加入氨水调节pH,除去Al3+、Fe3+,过滤后加入氨水,使Be元素转化成Be(OH)2沉淀,然后让Be(OH)2、NH3、HF反应生成(NH4)2BeF4,
(1)滤渣1为H2SiO3或SiO2;加入H2O2的目的是将Fe2+氧化成Fe3+;
(2)得到滤渣II为Fe(OH)3、Al(OH)3,Be元素不能转化成沉淀,根据表中数据,控制的pH范围是5.0≤pH<5.2或5.0~5.2;
(3)Be和Al的性质相似,氢氧化铝表现两性,能与NaOH溶液反应,Be(OH)2也能与NaOH反应,反应方程式为Be(OH)2+2NaOH=Na2BeO2+2H2O;
(4)沉铍中Be元素以Be(OH)2形式存在,根据流程发生Be(OH)2+2NH3+4HF=(NH4)2BeF4+2H2O;
(5)Mg、Be是活泼金属,能与氧气、氮气发生反应,因此需要真空的环境其原因是防止Mg、Be高温下与N2、O2等气体发生反应;
(6)令Be的利用率为x,因此有![]() ,推出Be的利用率为
,推出Be的利用率为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】建设“美丽中国”首先要做好环境保护与治理。氮氧化物(NOx)是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物(NOX)能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
(1)方案Ⅰ:利用甲烷在催化剂条件下还原NOx,相关反应如下:
①N2(g)+O2(g)=2NO(g) H1=+180.5kJ/mol
②CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) H2=-574kJ/mol
③CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(l) H3=-1160kJ/mol
则表示甲烷燃烧热的热化学反应方程式是 ___ 。
(2)方案Ⅱ:利用CO在催化剂条件下还原NOx:2NOx(g)+2CO(g)N2(g)+2CO2(g) H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2 mol NO2(g)和3 mol CO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
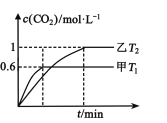
①甲容器中,平衡时NO2的转化率为____;
②T1___T2(填“>”或“<”);△H___0(填“>”或“<”),判定的依据是____;
③T2温度时,该反应的平衡常数K=____;
④乙容器达到平衡后,再充入3 mol NO2和2 molCO2,此时v(正)___v(逆)(填“>”“<”或“=”)。
(3)方案3:可以利用原电池原理处理氮氧化合物,原理如图。则其正极的电极反应式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是一种储氢材料,遇水反应生成氢氧化钙和氢气,是登山运动员常用的能源提供剂。某化学兴趣小组设计制取氢化钙的装置如下(固定装置已略去)。下列说法不正确的是
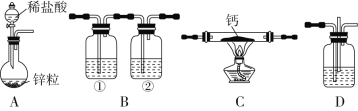
A.装置A:制取H2,离子方程式为Zn+2H+=Zn2++H2↑
B.装置B:用于除去H2中杂质,①中盛有NaOH溶液,②中盛有浓硫酸
C.装置C:制取CaH2,先点燃C处酒精灯,后打开A中分液漏斗的活塞
D.装置D:竖直导管的作用是平衡压强,观察H2流速以调节反应的进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜品油烯(D)可用作香料的原料,它可由A合成得到如下所示,下列说法正确的是 ( )
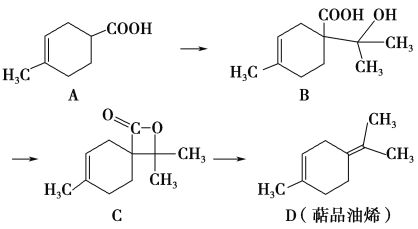
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 1 mol有机物A中含有1.204×1024个双键
D. 有机物C的同分异构体中不可能有芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下:
主反应 2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
副反应CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
(乙醚的制备)
实验装置如图所示(夹持装置和加热装置略)

(1)仪器a是_____(写名称);仪器b应更换为下列的 ___(填字母)。
A.干燥器
B.直形冷凝管
C.玻璃管
D.安全瓶
(2)实验操作的正确排序为_____(填字母),取出乙醚后立即密闭保存。
a.组装实验仪器
b.加入12mL浓硫酸和少量乙醇的混合物
c.检查装置气密性
d.熄灭酒精灯
e.点燃酒精灯
f.通冷却水
g.控制滴加乙醇的速率与产物馏出的速率相等
h.弃去前馏分
i.拆除装置
(3)加热后发现仪器a中没有添加碎瓷片,处理方法是_____;若滴入乙醇的速率显著超过产物馏出的速率,则反应速率会降低,可能的原因是 ____。
(乙醚的提纯)
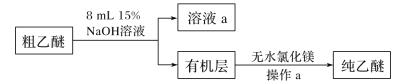
(4)用15%NaOH溶液洗涤粗乙醚的原因是____________;无水氯化镁的作用是_____。
(5)操作a的名称是____;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管接室外相同,均为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述中正确的是( )
A.物质的摩尔质量就是其相对分子(原子)质量
B.“摩尔”是国际单位制中的一个物理量
C.0.012 kg 12C中所含的碳原子数为NA
D.1 mol任何物质都含有约6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,其常见的化合物有钙钛矿、硫酸氧钛(TiOSO4)、钛酸(H2TiO3)、二氧化钛(TiO2)、四氯化钛(TiCl4)等,回答下列问题:
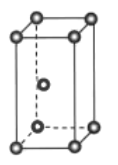
(1)基态钛原子的价层电子排布式为______,金属钛晶体的晶胞结构如图所示,其堆积方式名称为______。
(2)硫酸氧钛的阳离子为TiO2+,其阴离子的VSEPR模型名称为______。TiOSO4在水溶液中不稳定,易生成钛酸沉淀,该反应化学方程式为______。
(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图:
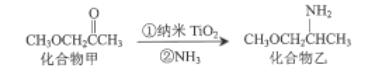
化合物乙种C、N、O元素的第一电离能由大到小的顺序为______。化合物甲的沸点低于化合物乙的沸点,主要原因是______。
(4)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,由此可知TiCl4为______晶体。将TiCl4加入盐酸中,经处理可得到一种配位数为6的绿色晶体TiCl36H2O,1mol该晶体恰好与含2molAgNO3的溶液反应得到白色沉淀,则该绿色晶体中配离子的化学式为______。
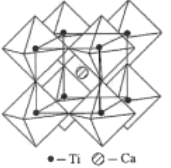
(5)钙钛矿的一种晶体结构如图所示。Ti位于立方晶胞的顶点,每个Ti被6个O包围成配位八面体,Ca位于立方晶胞的体心,与Ca距离最近的O有______个;若Ca与Ti的最近核间距为apm,阿伏伽德罗常数为NA,则此钙钛矿的密度为______gcm-3.(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法测得其中含C 72.0%、H 6.67%,其余为氧;质谱法分析得知A的相对分子质量为150。现代仪器分析有机化合物的分子结构有以下两种方法。
方法一:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1∶2∶2∶2∶3。
方法二:利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如图:
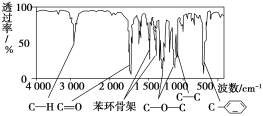
已知:A分子中只含一个苯环,且苯环上只有一个取代基。试回答下列问题。
(1)A的分子式为________。
(2)A的结构简式为_______________________________________________(写一种即可)。
(3)A的芳香化合物类同分异构体有多种,其中分子中不含甲基的芳香酸为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com