
| A、原子的最外层均有5个电子,最高价均为+5价 |
| B、非金属性比同周期的氧族元素和卤族元素弱 |
| C、原子半径比同周期的氧族元素、卤族元素小 |
| D、稳定性:NH3>PH3 |


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第IA族的元素都是金属元素 |
| B、L层电子数为奇数的所有主族元素,所在族的序数与元素原子的L层电子数相等 |
| C、主族元素的化合价绝对值与它的族序数一定相等 |
| D、同一主族元素的原子,最外层电子数相同,化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率可用同一原理来解释 |
| B、已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1:6,则该反应的还原产物是NO |
| C、已知14 mol/L的H2SO4溶液的溶质质量分数为80%,那么7 mol/L的H2SO4溶液的溶质质量分数将大于40% |
| D、铁在少量氯气或过量的氯气中点燃所得产物不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
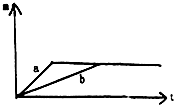 一定质量的钾、钠投入一定量的稀盐酸中,产生的气体的质量(纵轴m)随时间(横轴t)变化曲线如图:则下列说法正确的是(已知钾的还原性比钠强)( )
一定质量的钾、钠投入一定量的稀盐酸中,产生的气体的质量(纵轴m)随时间(横轴t)变化曲线如图:则下列说法正确的是(已知钾的还原性比钠强)( )| A、曲线a为钠,曲线b为钾 |
| B、投入的Na的质量小于K的质量 |
| C、投入的Na、K的质量一定相等 |
| D、两个反应的盐酸中HCl必须足量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com