
����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�����ȷ������ָ�����ϳɰ���ӦN2+3H2![]() 2NH3��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
2NH3��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�¶�/�� | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1�����ɱ������ݿ�֪�÷�ӦΪ______��Ӧ������������������������
�������ϣ�Ϊ������ƽ��ʱH2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______________������ĸ�������
a������ѹǿ b��ʹ�ú��ʵĴ���
c�������¶� d����ʱ����������е�NH3
��2��ԭ����H2��ͨ����ӦCH4��g��+H2O��g�� ![]() CO��g��+3H2��g����ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO��g��+3H2��g����ȡ����֪�÷�Ӧ�У�����ʼ������е�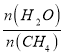 �㶨ʱ���¶ȡ�ѹǿ��ƽ��������CH4������Ӱ����ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ��������CH4������Ӱ����ͼ��ʾ��

��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ��p1________p2������>��������������<������
�ڸ÷�ӦΪ________��Ӧ��������������������������
��3��ԭ����H2����ͨ����ӦCO��g��+H2O��g�� ![]() CO2��g��+H2��g����ȡ��T ��ʱ�����ݻ��̶�Ϊ2 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO2��Ũ��Ϊ0.3 mol��L��1����ƽ��ʱCO��ת����Ϊ________
CO2��g��+H2��g����ȡ��T ��ʱ�����ݻ��̶�Ϊ2 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO2��Ũ��Ϊ0.3 mol��L��1����ƽ��ʱCO��ת����Ϊ________
���𰸡� ���� ad < ���� 0.6
����������1�����ɱ������ݿ�֪�����¶����ߣ���Ӧ��ƽ�ⳣ����С��˵�������¶�ƽ�������ƶ����������¶�ƽ�������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ���ʴ�Ϊ��������
��a������ѹǿ��ƽ�������ƶ���H2ת��������a��ȷ��b��ʹ�ô�����ƽ�ⲻ�ƶ���H2ת���ʲ��䣬��b������c������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���H2ת���ʼ�С����c������d����ʱ����������е�NH3��ƽ�������ƶ���H2ת��������d��ȷ��
�ʴ�Ϊ��ad��
��2��������ӦΪ��������ķ�Ӧ������ѹǿƽ�������ƶ������麬������������P2>P1��
�ʴ�Ϊ��<��
����ͼ��֪�����¶�������ĺ�����С��˵�������¶�ƽ�������ƶ����������¶�ƽ�������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��3����T��ʱ�����ݻ��̶�Ϊ2 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO2��Ũ��Ϊ0.3 mol��L��1����
CO(g) + H2O(g)CO2(g)+H2(g)
��ʼŨ��(mol/L):0.5 0.5 0 0
�仯Ũ��(mol/L):0.3 0.3 0.3 0.3
ƽ��Ũ��(mol/L):0.2 0.2 0.3 0.3
ƽ��ʱCO��ת����=![]() =60%��
=60%��
�ʴ�Ϊ��60%��0.6


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��Һ�к�������8�������е�5�֣�����ˮ�ĵ��뼰���ӵ�ˮ�⣩��K+��Cu2+��Al3+��Fe2+��Cl����CO32����NO3����SO42�� �� ��5�����ӵ����ʵ���Ũ����ȣ�Ϊ�˽�һ��̽����ˮ��Һ����ɣ�ijͬ ѧ����������ʵ�飺
���ò�˿պȡ������Һ���ڻ��������գ�����ɫ�ܲ����۲�����ɫ���森
����ȡ��Һ�����������ᣬ����ɫ�������ɣ�����ɫ������������ɺ���ɫ��
����ȡ��Һ����BaCl2��Һ���а�ɫ�������ɣ�
��������ʵ�飬�����Ʋ���ȷ���ǣ� ��
A.��ȷ����Һ���Ƿ����Cu2+����
B.ԭ��Һ�в���K+��Al3+��CO![]() ������
������
C.���ݲ����ֻ��ȷ����Һ��һ������NO3������
D.��������õ��İ�ɫ��������2�ֱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A.�����ʯ��ˮ�м�������ʵ�����NaHCO3��Һ��Ca2++2OH��+2HCO ![]() �TCaCO3��+CO
�TCaCO3��+CO ![]() +2H2O
+2H2O
B.��NH4HSO4ϡ��Һ�м���NaOHϡ��Һ������OH��+NH ![]() �TNH3?H2O
�TNH3?H2O
C.�������������������Fe��OH��3+3H+�TFe3++3H2O
D.�����KI��Һ�еμ�����H2O2��Һ����Һ����ɫ��H2O2+2I��+2H+�TI2+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���M�Ľṹ��ʽ���£� ![]() �����й�M����������ȷ���ǣ� ��
�����й�M����������ȷ���ǣ� ��
A.M�ķ���ʽΪ��C12H15O5N2
B.M���Է���ˮ�ⷴӦ���кͷ�Ӧ���ӳɷ�Ӧ����ȥ��Ӧ
C.M��ˮ�������һ�����д���
D.1 molM��������1L4mol/L��NaOH��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g����5O2��g�� ![]() 4NO��g����6H2O��g��������������ȷ����
4NO��g����6H2O��g��������������ȷ����
A. �ﵽ��ѧƽ��ʱ4v����O2����5v����NO��
B. ����λʱ��������x mol NO��ͬʱ������x mol NH3,��Ӧ�ﵽƽ��״̬
C. �ﵽ��ѧƽ��ʱ�������������ݻ���������Ӧ���ʼ�С���淴Ӧ��������
D. ��ѧ��Ӧ���ʹ�ϵ��2v����NH3����3v����H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2 L���ܱ������з������·�Ӧ��A(s)��2B(g)![]() 2C(g) ��H<0����Ӧ������B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����Ӧ��ƽ�����t1��t2��t3��t4ʱ�ֱ�ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2.�����й�˵����ȷ����
2C(g) ��H<0����Ӧ������B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����Ӧ��ƽ�����t1��t2��t3��t4ʱ�ֱ�ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2.�����й�˵����ȷ����

A. ��Ӧ��ʼ2 min�ڣ�v(B)��0.1 mol/(L��min)
B. t1ʱ�ı�����������������¶�
C. t3ʱ�ı�����������Ǽ�ѹ����ʱc(B)����
D. t4ʱ������ʹ���˴�������ʱc(B)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷���������Ҫ�ɷ�ΪAl��������Fe��Si�ȣ��ȿ���ȡ�л��ϳɴ���AlBr3�ֿ���ȡ��ˮ������������[Al2��SO4��318H2O]��
I��ʵ������ȡ��ɫ����ˮAlBr3���۵㣺97.5�棬�е㣺263.3��265�棩������ͼ��ʾװ�ã���Ҫʵ�鲽�����£�
����1�����������飬��CCl4����Ƭ�̣����Ȼ��Ͷ�뵽��ƿ6�У�
����2���ӵ��ܿ�7�������ĵ�����ͬʱ���ܿ�l��4�ſգ�һ��
ʱ���رյ��ܿ�7��1�����ܿ�4��װ��P2O5�ĸ���ܣ�
����3���ӵ�Һ©������һ������Һ������ƿ6�У�����֤��ƿ6
������ʣ��
����4��������ƿ6������һ��ʱ�䣮
����5�������������������Ϊ�ӵ��ܿ�4�����ܿ�1����װ��
P2O5�ĸ�����뵼�ܿ�1���ӣ�����ƿ6������270�����ң�ʹ�廯��
��������ռ���2��
����6���������ʱ���ڼ���ͨ�뵪��������£����ռ���2��3��
���£����������3����
��1������1�У�������CCl4���ݵ�Ŀ���� ��
��2������2�����У�ͨ������Ŀ���� ��
��3������3�У���ʵ��Ҫ��֤��ƿ��������ʣ����Ŀ���� ��
��4������4���ݺ��������жϿ���ֹͣ�������� ��
��5������5����ܿ�1��4������4ͨ��N2��Ŀ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܹ���������������Ԫ�صĴ��ڵIJ�����(����)
A.����������ֱ�Ӽ���AgNO3��Һ
B.������ˮ����ֽ������AgNO3��Һ
C.����ϡ�����ữ��Ȼ�����AgNO3��Һ
D.����NaOH���Ҵ���Һ�����Ⱥ����ϡ�����ữ��Ȼ�����AgNO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʰ��ᡢ����������е���
A. ���ᡢ̼���ơ������� B. ���ᡢ�ռ����
C. �������ơ���ʯ�ҡ������� D. ���ᡢ��ʯ�ҡ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com