
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij�Ͼ���ͭԪ��(��BeO:25%��CuS:71%������FeS��SiO2)�л������ͭ���ֽ����Ĺ�����������:

��֪:I.�롢��Ԫ�ػ�ѧ��������
II.������:Ksp[Cu(OH)2]=2.2��10-20��Ksp[Fe(OH)3]=4.0��10-38��Ksp[Mn(OH)2]=-2.1��10-13
(1)��ҺA����Ҫ�ɷֳ�NaOH�⣬����_____ (�ѧʽ)��д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ_____________��
(2)����ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2��ѡ�����������˳��______��
a.���������NaOH b.ͨ�������CO2 c.��������İ�ˮ
d.����������HC1 e.���� f.ϴ��
�ڴ�BeCl2��Һ�еõ�BeCl2����IJ�����________________��
(3)��MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����ӦII��CuS ������Ӧ�Ļ�ѧ����ʽ______________��
������ŨHNO3�ܽ�������ȱ����____________(��дһ��)��
(4)��ҺD�к�c(Cu2+)=2.2mol/L��c(Fe3+)=0.008mol/L c(Mn2+)=0.01mol/L����μ���ϡ��ˮ����pH�����η��룬���ȳ�������___ (�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pHֵ����____��
���𰸡� Na2SiO3��Na2BeO2 BeO22-+4H+=Be2++2H2O cefd ���Ȼ��������������ᾧ���������ᾧʱ����Һ�г���ͨ���Ȼ������壩 MnO2+CuS+2H2SO4=S+MnSO4+CuSO4+2H2O ������Ⱦ���������� Fe3+ 4
�����������黯ѧ�������̣���1������ͭԭ���ijɷ�BeO��CuS��FeS��SiO2��������ϢI��BeO�������������CuS��������������Һ��Ӧ��FeS�����������Ʒ�Ӧ��SiO2���������������������������Һ��Ӧ�������ҺA����Ҫ�ɷ���NaOH��Na2SiO3��Na2BeO2��������ϢI��BeO2����������ᷴӦ�����Ȼ����ˮ�������ӷ���ʽΪBeO22��+4H��=Be2��+2H2O���𰸣�Na2SiO3��Na2BeO2��BeO22-+4H+=Be2++2H2O��
��2��������BeԪ�ء���Ԫ�ػ�ѧ�������ƣ�����ҺC���ȼ�������İ�ˮ������Be(OH)2������Ȼ����ˡ�ϴ�ӣ��ټ���������HCl������BeCl2������������cefd��
��Ϊ������Be2����ˮ�⣬�����Ҫ��HCl�ķ�Χ�ж�BeCl2��Һ�����ᾧ��
��3���ٸ�����Ϣ��CuS��Sת��ΪS���ʣ�MnO2��Mn����ԭΪMn2�������ݻ��ϼ�������������ƽ���仯ѧ��Ӧ����ʽΪMnO2+CuS+2H2SO4=S��+MnSO4+CuSO4+2H2O������Ũ��������������ŨHNO3����ԭ��NO2��NO2�ж���Ⱦ������
��4�����ֽ��������ӳ��ֳ���������Ũ������Ksp�Ĺ�ϵ��Cu2��ת���ɳ�����c(OH��)= mol��L��1��Fe3��ת���ɳ�����c(OH��)=
mol��L��1��Fe3��ת���ɳ�����c(OH��)= mol��L��1��Mn2��ת���ɳ�����c(OH��)=
mol��L��1��Mn2��ת���ɳ�����c(OH��)= mol��L��1��������ȳ�������Fe3����ΪʹCu2����������ʱc(OH��)=1��10��10mol��L��1��c(H��)=10��14/10��10=10��4mol��L��1����pH=4����pH>4ʱ��Cu2�����ֳ�����
mol��L��1��������ȳ�������Fe3����ΪʹCu2����������ʱc(OH��)=1��10��10mol��L��1��c(H��)=10��14/10��10=10��4mol��L��1����pH=4����pH>4ʱ��Cu2�����ֳ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�������F(![]() )����Ҫ�Ļ���ԭ�ϣ���һ�ֺϳ�·�����£�
)����Ҫ�Ļ���ԭ�ϣ���һ�ֺϳ�·�����£�

��֪

��1��д��B�Ĺ���������___________��
��2�������й�����C��˵����ȷ����________��
A��C�ķ���ʽ��C9H12O3 B��C�ĺ˴Ź���������4�����շ�
C��1mlC�������1mol����Na D��C���Է���ȡ�����ӳɺ���ȥ��Ӧ
��3��д���ٵĻ�ѧ����ʽ��____________________________________��
��4��E�Ľṹ��ʽΪ________________________________________________��
��5�� �ж���ͬ���칹�壬�ܷ���������Ӧ�ķ����廯������____________�֣�������������������ͬ���칹��Ľṹ��ʽΪ____________
�ж���ͬ���칹�壬�ܷ���������Ӧ�ķ����廯������____________�֣�������������������ͬ���칹��Ľṹ��ʽΪ____________
��1mol�������������3 mol NaOH�� �ڱ�����һ�ȴ���ֻ�����֡�
��6�����������ϳ�·�ߣ��������ϩ�ϳ�2-�����ĺϳ�·�ߡ�(�úϳ�·������ͼ��ʾ����ע����Ӧ�������Ϲ�����ֻ�����Լ�����ѡ) ____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͼ��˵������ȷ����

A. ͼ�٣����Ũ�ȵĵ⻯�ƺ��Ȼ��ƵĻ����Һ�м�����������Һ
B. ͼ�ڣ���pH���������ͬ������ʹ���������Һ�зֱ��ˮϡ��
C. ͼ�ۣ���Ca��OH��2��Һ��ͨ��CO2
D. ͼ�ܣ���Ba��OH��2��Һ�м���ϡH2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˹�ģ�������ã���Ƶĵ绯ѧʵ��װ����ͼ��ʾ����װ���ܽ�H2O��CO2ת��ΪO2��ȼ��(C3H8O)������˵����ȷ����

A. ��װ�ý���ѧ��ת��Ϊ���ܺ͵���
B. ��װ�ù���ʱ��H+��a����b��Ǩ��
C. ��ת�������У�ˮ�õ�����
D. ��װ���з������ܷ�ӦΪ6CO2+8H2O![]() 2C3H8O+9O2
2C3H8O+9O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ��������������A��B��C��D��E��������Ԫ����ɵ���ѧ��ѧ���������ʣ�����A�ǵ��ʣ�C�����������A��ˮ��Һ��C������Ư���ԣ�B����Ȼ�������Һ�壬E����Ԫ��̨�����֮�����������ͼ��ʾ�Ĺ�ϵ������˵������ȷ����

A. YX2������ɫʯ����Һ�ȱ�����ɫ B. ���Ӱ뾶��С��ϵ��Y>Z>X>W
C. �������ӵĻ�ԭ�ԣ�Y>Z D. Y��Z����ͬһ���ڣ���X����ͬһ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��

��ش��������⣺
��1��ʵ����ֻ��100 mL��250 mL��500 mL���ֹ�������ƿ����Ҫ����480 mL 0.50 mol/L��ϡ���ᣬ��ȡ��Ũ���� mL��
��2����������ɴ�ʵ���㽫�õ���������20 mL��Ͳ���ձ�����������____________��
��3��Ҫ��������Һ��ȡ��50 mLʢװ���Լ�ƿ�У��������ϱ�ǩ�����ǩ��������________________�����ٴ���ȡ��10 mL��Һϡ����20 mL����ϡ�ͺ���Һ�����ʵ���Ũ��Ϊ__________��
��4�����в�����ʹ������ҺŨ��ƫ�͵��� ��
A������Ͳ��ȡŨ���ᣬ����ʱ���ӿ̶��� |
B��ת����Һʱδϴ���ձ� |
C������ƿ������ˮϴ�����Բ���������ˮ |
D������ʱ��������ƿ�Ŀ̶��� |
E������ҡ�Ⱥ���Һ����ڿ̶��ߣ��ټ�ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������к�������[KAl(SO4)2��12H2O]��Al2O3��Fe2O3����һ���������ɼ�ʵ����ͼ��ʾ������֮���ת����
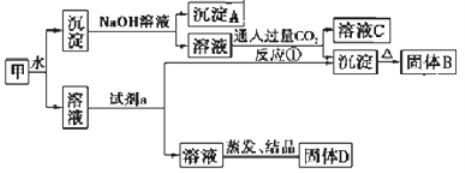
��ش��������⣺
��1��д��A��B�Ļ�ѧʽ��A__________��B__________��
��2���Լ�a���ѡ�������Լ��е�______________��
A��NaOH��Һ B��ϡ���� C��������̼ D����ˮ
д����Ӧ�����ӷ���ʽ_____________________________________��
��3��д����Ӧ�٣�������ҺC�ͳ����������ӷ���ʽ______________��
��4������D������Ϊ�����ԵĻ�ѧ���ϣ�D���������ʵĻ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ұ�����ͼ��ʾ�IJ������������ᴿij�����ʣ����з���һ����ȷ����

A. �ò������̿����ڷ���ˮ�����Ȼ�̼
B. ����I-���ǹ��ˣ�Ŀ���ǽ���Һ����
C. �������ڴ����Ȼ�̼����ȡ�ⵥ��
D. �����ᴿ������BaSO4��NaCI��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˹�������ü�ӵ绯ѧ������ȥ��л�����е�����CO(NH2)2��ԭ����ͼ�������й�˵����ȷ����(����)
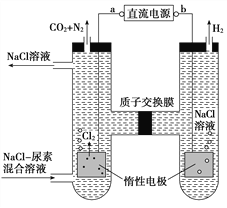
A. aΪ��Դ�ĸ���
B. ����������������Һ��pH����ǰ��Ƚ�����
C. �������з����ĵ缫��ӦΪ2H����2e��=H2��
D. ���������ռ��������Ʒ13.44 L(��״��)�����ȥ������Ϊ7.2 g(����������ܽ�)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com