
【题目】某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 1 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.2 |
丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
A.平衡常数:K甲>K乙
B.a=0.4
C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005molL-1min-1
D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2
【答案】A
【解析】
A.正反应为吸热反应则温度越高平衡常数越大,甲中反应正向或逆向移动程度都较小,则温度变化较小,乙中反应正向移动,正反应为吸热反应,温度较低,所以T:甲>乙,则平衡常数:K甲>K乙,故A正确;
B.若甲中生成物完全转化为反应物,则甲中反应物是乙的二倍,反应前后气体计量数不变,则增大压强平衡不移动,恒温恒容条件下二者为等效平衡,平衡时c(CO):甲是乙的2倍,但实际上是恒容绝热条件,随着反应的进行温度逐渐降低,甲中温度较低,反应物转化率:甲<乙,则甲中c(CO)小于乙中2倍,所以a<0.4,故B错误;
C.v(CO)= =0.03mol/(L·min),相同条件下相同时间内v(S)=
=0.03mol/(L·min),相同条件下相同时间内v(S)=![]() v(CO)=
v(CO)=![]() ×0.03mol/(L·min)=0.015mol/(L·min),故C错误;
×0.03mol/(L·min)=0.015mol/(L·min),故C错误;
D.如果将丙中生成物完全转化为反应物时,反应物物质的量:丙是乙的二倍,丙中开始压强是乙的二倍,增大压强平衡不移动,恒温条件下则有c丙(CO)= 2c乙(CO),但实际为绝热条件下丙逆向移动放热,丙的温度大于乙的温度,温度升高平衡正移,所以平衡时c(CO):b大于乙中c(CO)的二倍,则b>0.4,故D错误;
故选:A。


科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
A.已知C(s)+O2(g)=CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则2ΔH1<ΔH2
B.已知2H2(g)+O2(g)=2H2O(g) ΔH= -483.6kJ·mol-1,则氢气燃烧热为241.8kJ·mol-1
C.已知2SO2(g)+O2(g)![]() 2SO3(g) ΔH= -Q kJ·mol-1(Q>0),则将16g SO2(g)和足量O2置于一密闭容器中,充分反应后放出0.25Q kJ的热量
2SO3(g) ΔH= -Q kJ·mol-1(Q>0),则将16g SO2(g)和足量O2置于一密闭容器中,充分反应后放出0.25Q kJ的热量
D.已知:C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.铅蓄电池放电时,负极质量减轻,正极增重
B.升高CH3COONa溶液的温度,其水的离子积常数和pH均增大
C.CH3CH=CHCH3分子中的四个碳原子都在一条直线上
D.常温下Ksp(AgBr)=5.0×10-13,Ksp(AgCl)=1.8×10-10,则S(AgBr)>S(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学知识,解决下列问题。
(1)AlCl3溶液呈___(填“酸”“中”或“碱”)性,原因是___(用离子方程式表示)。实验室配制AlCl3溶液时,常将AlCl3固体先溶于较浓的盐酸中,再用蒸熘水稀释到所需的浓度,目的是___。
(2)今有常温下五种溶液:CH3COONa溶液、NH4Cl溶液、NaOH溶液、氨水、NH4HSO4溶液。
①CH3COONa溶液pH___(填“>”“=”或“<” )7,若要使溶液的pH增大,可采取的措施是___。
②pH相等的NaOH溶液和CH3COONa溶液,分别稀释相同倍数后,NaOH溶液的pH___(填“>”“=”“<”)CH3COONa溶液。
③物质的量浓度均为0.1mol·L-1的三种溶液:A.NH4Cl溶液 B.NH4HSO4溶液 C.氨水,c(NH4+)由大到小的顺序为___(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D-Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D-Zn-NiOOH二次电池,结构如图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。下列说法错误的是( )
ZnO(s)+2Ni(OH)2(s)。下列说法错误的是( )
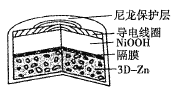
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.放电时正极反应为NiOOH(s)+H2O(l)+e-=Ni(OH)2(s)+OH-(aq)
C.放电时负极反应为Zn(s)+2OH-(aq)-2e-=ZnO(s)+H2O(l)
D.放电过程中OH-通过隔膜从负极区移向正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸厂的烟气中含有一定量的氮氧化物(NOx),通常要将烟气中的氮氧化物转化为无毒无害的物质即脱硝。
(1)用空气-水脱硝的方法是最经济的方法。
已知:①2NO(g)+O2(g)=2NO2(g)△H1=-123.4kJ·mol-1
②3NO2(g)+H2O(1)=2HNO3(aq)+NO(g)△H2=-73.6kJ·mol-1
写出NO(g)、O2(g)和液体水反应生成HNO3(aq)的热化学方程式______。
(2)吸收电解法是脱硝的种重要方法。先用稀硝酸吸收NOx、反应生成HNO2(一元弱酸),再将吸收液加入电解槽中进行电解,使之转化为硝酸,其电解装置如下图所示。

①图中a应连接电源的________(正极或负极),其电极反应式为_____。
②电解过程中总反应的化学方程式是_____。有10 mol HNO2参加反应.氧化产物的物质的量是_____。
③阴极区产生1mol氮气时,理论上阳极区减少H+的物质的量约为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由几种离子化合物组成的混合物中含有以下离子中的若干种:K+、Cl-、NH![]() 、Mg2+、Ba2+、CO
、Mg2+、Ba2+、CO![]() 、SO
、SO![]() 。将该混合物溶于水后得澄清溶液,现取三份100 mL该溶液分别进行如下实验。
。将该混合物溶于水后得澄清溶液,现取三份100 mL该溶液分别进行如下实验。
实验序号 | 实验内容 | 实验结果 |
1 | 加入AgNO3溶液 | 有白色沉淀生成 |
2 | 加入足量NaOH溶液并加热 | 收集到气体1.12 L(标准状况下) |
3 | 加入足量BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加入足量稀盐酸,然后过滤、洗涤、干燥、称量 | 第一次称量读数为6.27 g,第二次称量读数为2.33 g |
请回答下列问题:
(1)根据实验1对Cl-是否存在的判断是________(填“一定存在”“一定不存在”或“不能确定”);根据实验1~3判断原混合物中一定不存在的离子是________。
(2)试确定100 mL溶液中一定存在的阴离子及其物质的量浓度(可不填满)。
阴离子符号 | 物质的量浓度(mol·L-1) |
_______ | ___________ |
______ | _______________ |
(3)K+是否存在?________(填“存在”或“不存在”),判断的理由是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.![]() 属于醛类,官能团为—CHO
属于醛类,官能团为—CHO
B.分子式为C5H10O2的有机物中能与NaOH溶液反应的有4种
C.立方烷( )的六氨基(-NH2)取代物有3种
)的六氨基(-NH2)取代物有3种
D.烷烃 的正确命名是2-甲基-3-丙基戊烷
的正确命名是2-甲基-3-丙基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PMMA. 也叫亚克力或者亚加力[其分子式是(C5H8O2)n].其实就是有机玻璃,化学名称为聚甲基丙烯酸甲酯.某同学从提供的原料库中选择一种原料 x. 设计合成高分子亚克力的路线如图所示:
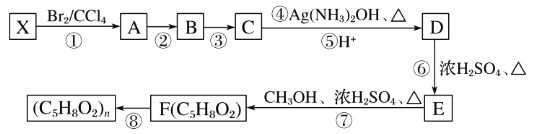
原料库:a.CH2=CHCH3 b. CH2=CHCH2CH3 c. CH2=C(CH3)2 d.CH(CH3)2
已知: 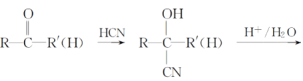
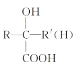 (R、R'、R〃表示烃基)
(R、R'、R〃表示烃基)
请回答;
(1)原料X是 _________________ (填序号字母)。
(2)②的反应条件是 ______________;D中含有的官能团的名称是_____________。
(3)反应⑦的化学方程式是__________________________。
(4)C有多种同分异构体,其中分子中含“![]() ” 结构的共有_______ 种。
” 结构的共有_______ 种。
(5)某同学以丙烯为原料设计了合成中间体D的路线: 丙烯![]() ......→D,得到D的同时也得到了另一种有机副产物M. 请你预测 M 可能的结构简式是__________。
......→D,得到D的同时也得到了另一种有机副产物M. 请你预测 M 可能的结构简式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com