
【题目】硝酸厂的烟气中含有一定量的氮氧化物(NOx),通常要将烟气中的氮氧化物转化为无毒无害的物质即脱硝。
(1)用空气-水脱硝的方法是最经济的方法。
已知:①2NO(g)+O2(g)=2NO2(g)△H1=-123.4kJ·mol-1
②3NO2(g)+H2O(1)=2HNO3(aq)+NO(g)△H2=-73.6kJ·mol-1
写出NO(g)、O2(g)和液体水反应生成HNO3(aq)的热化学方程式______。
(2)吸收电解法是脱硝的种重要方法。先用稀硝酸吸收NOx、反应生成HNO2(一元弱酸),再将吸收液加入电解槽中进行电解,使之转化为硝酸,其电解装置如下图所示。

①图中a应连接电源的________(正极或负极),其电极反应式为_____。
②电解过程中总反应的化学方程式是_____。有10 mol HNO2参加反应.氧化产物的物质的量是_____。
③阴极区产生1mol氮气时,理论上阳极区减少H+的物质的量约为_____。
【答案】4NO(g)+3O2(g)+2H2O(l)=4HNO3(aq) △H=-517.4kJ/mol 正极 HNO2+H2O-2e-=NO3-+3H+ 5HNO2![]() 3HNO3+N2↑+H2O 6mol 10mol
3HNO3+N2↑+H2O 6mol 10mol
【解析】
(1)已知:①2NO(g)+O2(g)=2NO2(g)△H1=-123.4kJ·mol-1
②3NO2(g)+H2O(1)=2HNO3(aq)+NO(g)△H2=-73.6kJ·mol-1
根据盖斯定律可知,将2×②+①×3,可得4NO2(g)+3O2(g)+2H2O(l)=4HNO3(aq),△H=2×△H2+△H1×3=(-73.6 kJmol-1)×2+(-123.4 kJmol-1)×3=-517.4kJmol-1;
(2)①a电极上亚硝酸失电子生成硝酸,所以a为阳极,b为阴极,则a与电源的正极相连;阳极上亚硝酸失电子生成硝酸,其电极方程式为:H2O+HNO2-2e-=NO3-+3H+;
②阳极上亚硝酸失电子生成硝酸,其电极方程式为:5H2O+5HNO2-10e-=5NO3-+15H+;阴极生成氮气,反应式为2NO3-+10e-+12H+= N2↑+6H2O,两式相加得电解过程中总反应的化学方程式为:5HNO2 3HNO3+N2↑+H2O,化合价升高的产物为氧化产物,即硝酸,根据总反应的化学方程式的比列关系可知有10 mol HNO2参加反应,氧化产物的物质的量是6 mol;
3HNO3+N2↑+H2O,化合价升高的产物为氧化产物,即硝酸,根据总反应的化学方程式的比列关系可知有10 mol HNO2参加反应,氧化产物的物质的量是6 mol;
③阴极反应式为2NO3-+10e-+12H+=N2↑+6H2O,所以阴极区产生1mol氮气时,转移电子为10mol,则有10molH+从阳极室进入阴极室,即理论上阳极区减少H+的物质的量约为10mol。


科目:高中化学 来源: 题型:
【题目】在20mL0.1mol·L-1 HCl溶液中加入同体积、同物质的量浓度的NH3·H2O溶液,反应后溶液中各粒子浓度的关系错误的是
A.c(H+)+c(![]() )=c(OH-)+c(Cl-)B.c(H+)+c(Cl-)=c(OH-)+c(NH3·H2O)
)=c(OH-)+c(Cl-)B.c(H+)+c(Cl-)=c(OH-)+c(NH3·H2O)
C.c(Cl-)>c(![]() )>c(H+)>c(OH-)D.c(Cl-)=c(
)>c(H+)>c(OH-)D.c(Cl-)=c(![]() )+c(NH3·H2O)
)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥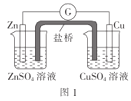
B.图2:可根据该实验验证铁的吸氧腐蚀
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应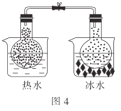
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由多元素组成的化合物Fe-Sm-As-F-O是一种重要的铁系超导材料。下列说法正确的是
A.F的核外电子排布式1s22s22p7
B.Fe3+的轨道表示式![]() 违背了泡利不相容原理
违背了泡利不相容原理
C.N、As同主族,第一电离能N<As
D.电负性F>O>As
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 1 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.2 |
丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
A.平衡常数:K甲>K乙
B.a=0.4
C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005molL-1min-1
D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.钠与水反应:Na+2H2O===Na++2OH-+H2↑
B.电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O ![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-===BaSO4↓+H2O
D.向澄清石灰水中加入少量的NaHCO3溶液:Ca2++2OH-+2HCO3-===CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.4 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。
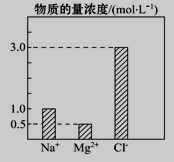
(1)该混合液中,NaCl的物质的量为________mol,含溶质MgCl2的质量为________g。
(2)该混合液中CaCl2的物质的量为_________mol,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为___________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型冠状病毒肺炎疫情发生以来,科学和医学界积极寻找能够治疗病毒的药物。4-去甲基表鬼臼毒素具有抗肿瘤、抗菌、抗病毒等作用,分子结构如图所示,下列说法错误的是

A.该有机物中有三种含氧官能团
B.该有机物有4个手性碳原子,且遇FeCl3溶液显紫色
C.该有机物分子中所有碳原子不可能共平面
D.1mol该有机物最多可以和2molNaOH、7molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为2L的密闭容器中,2mol X和3mol Y进行反应:X(g)+Y(g)![]() Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
A. 以X浓度变化表示的反应速率为0.05 mol/(Ls)
B. 其他条件不变,增大X的浓度,平衡右移,X的转化率增大
C. 其他条件不变,12s后将容器体积扩大为10L,Z的平衡浓度变为0.06mol/L
D. 其他条件不变,若移走1molX和1.5molY,再达平衡时Z的物质的量小于0.3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com