

 ��д�ṹ��ʽ����
��д�ṹ��ʽ���� ��һ�������¿�ˮ��Ϊ
��һ�������¿�ˮ��Ϊ ��R1-NH2����F��ǿ��ͳ�ʱ����������·���ˮ�ⷴӦ�Ļ�ѧ����ʽ��
��R1-NH2����F��ǿ��ͳ�ʱ����������·���ˮ�ⷴӦ�Ļ�ѧ����ʽ�� ��
�� ���� C��״���Ӧ����D����D�Ľṹ��֪CΪ ��B��Ũ���ᷢ��ȡ��������C����BΪ
��B��Ũ���ᷢ��ȡ��������C����BΪ ��A����������Ӧ����B��D����������ԭΪ��������E��E��CH3CH2CH2COCl����ȡ����Ӧ����F�������Ŀ�������
��A����������Ӧ����B��D����������ԭΪ��������E��E��CH3CH2CH2COCl����ȡ����Ӧ����F�������Ŀ�������
��� �⣺C��״���Ӧ����D����D�Ľṹ��֪CΪ ��B��Ũ���ᷢ��ȡ��������C����BΪ
��B��Ũ���ᷢ��ȡ��������C����BΪ ��A����������Ӧ����B��D����������ԭΪ��������E��E��CH3CH2CH2COCl����ȡ����Ӧ����F��
��A����������Ӧ����B��D����������ԭΪ��������E��E��CH3CH2CH2COCl����ȡ����Ӧ����F��
��1��A����������Ӧ����B��D������ԭ��Ӧ����E���ʴ�Ϊ��������Ӧ����ԭ��Ӧ��
��2��BΪ ��B��ͬ���칹����������������ٺ��б������ں�������������������Cu��OH��2��Ӧ��˵������ȩ��������������ͬ���칹�����ڼ����ᱽ����������ᱽ�����Լ����ᱽ�������ᱽ��������4�֣��ʴ�Ϊ��4��
��B��ͬ���칹����������������ٺ��б������ں�������������������Cu��OH��2��Ӧ��˵������ȩ��������������ͬ���칹�����ڼ����ᱽ����������ᱽ�����Լ����ᱽ�������ᱽ��������4�֣��ʴ�Ϊ��4��
��3��CΪ ��C�й������������������Ȼ���
��C�й������������������Ȼ���
a��ʹ�ù����ļ״����ܴٽ���Ӧ������Ӧ������У��������D�IJ��ʣ�����ȷ��
b��Ũ�������ˮ�Կ��ܻᵼ����Һ��ڣ��ʴ���
c�����ڸ÷�Ӧ�м״����Ƿ�Ӧ������ܼ�������ȷ��
d�����ݽṹ��ʽ֪��D�Ļ�ѧʽΪC9H9NO4������ȷ��
�ʴ�Ϊ���������Ȼ���acd��
��4��E��ͬ���칹�屽�����ᾭ�ۺϷ�Ӧ�γɵĸ߾����� ��
��
�ʴ�Ϊ�� ��
��
��5��Fˮ������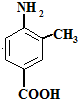 ��CH3CH2CH2COOH��CH3OH����Ӧ����ʽΪ
��CH3CH2CH2COOH��CH3OH����Ӧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬����D�ṹ��ʽ��Ϸ�Ӧ���������ƶϣ����ؿ���ѧ�������ƶϼ�֪ʶǨ����������ȷ�ж������ǽⱾ��ؼ����ѵ���ͬ���칹�������жϣ�ע�⣨5����ˮ�ⷴӦ�ϼ��ͳɼ�λ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��100�桢101 kPa�����£�1 molҺ̬ˮ����ʱ��Ҫ����40.69 kJ����������H2O��g���TH2O��l���ġ�H=+40.69 kJ•mol-1 | |
| B�� | ��֪CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-802.33 kJ•mol-1����CH4��ȼ����Ϊ802.33 kJ | |
| C�� | ϡ������0.1 mol•L-1NaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��H+��aq��+OH-��aq��=H2O��l����H=-57.3 kJ•mol-1 | |
| D�� | ��֪S��g��+O2��g���TSO2��s����H1��S��g��+O2��g���TSO2��g����H2�����H2����H1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƾ���ȼ����ΪQ3 kJ | |
| B�� | ��ʹ46 g�ƾ�Һ����ȫȼ�գ����ָ������£��ͷų�������Ϊ��3Q1-Q2+Q3��kJ | |
| C�� | H2O��g����H2O��l���ͷų������������Ըù���Ϊ��ѧ�仯 | |
| D�� | �ӷ�Ӧ�ۿ�֪1mol C2H5OH��g����������2 mol CO2��g����3 mol H2O��g���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HI���������ʵ�����ֽ����� | |
| B�� | HI����������С����ֽ����� | |
| C�� | HI���������ʴ�����ֽ����� | |
| D�� | ���ж�HI���������ʺͷֽ����ʵ���Դ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��a=1ʱ����ϩ����������ʵ���֮��Ϊ1��1 | |
| B�� | ��a=1ʱ���ҷ�Ӧ��CO��CO2�Ļ����������ʵ���Ϊ��Ӧǰ������$\frac{2}{3}$ʱ����b=3 | |
| C�� | ��a=1ʱ���ҷ�Ӧ��CO��CO2�Ļ����������ʵ���Ϊ��Ӧǰ������$\frac{2}{3}$ʱ����CO��CO2�����ʵ���֮��Ϊ3��1 | |
| D�� | a��ȡֵ��ΧΪ$\frac{5}{6}$��a��$\frac{5}{4}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��д��E��G��Ӧ����H�Ľṹ��ʽ��
��д��E��G��Ӧ����H�Ľṹ��ʽ�� ��
�� +2Cu��OH��2$\stackrel{��}{��}$
+2Cu��OH��2$\stackrel{��}{��}$ +Cu2O��+2H2O��
+Cu2O��+2H2O���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com