
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应是C2H5OH+HCl→C2H5Cl+H2O。某探兖小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。回答下列问题:

(1)仪器a的名称是______________。
(2)装置A中发生反应的离子方程式为____________________________________。
(3)仪器b中冷凝水从______(填“p”或“q”,下同)口进,___________口出。
(4)若撤去装置B,对实验的影响是__________________________________________________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是______________________。
(6)已知:CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2-=H++2I-+CO2↑;I2+2S2O32-=2I-+S4O62-。称取0.40g产品,配成待测溶液,加入20.00mL0.100mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。滴定时所用指示剂是__________________________,达到滴定终点的现象是_____________________________________________________,测得产品的纯度为___________。
【答案】 (恒压)分液漏斗 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O p q 会有氯化氢杂质与乙醇反应,生成氯乙烷。导致三氯乙醛的纯度降低 停止对A加热或控制滴加盐酸的量 淀粉溶液 蓝色变为无色,且半分钟内不变色 66.4%(或66.375%)
Mn2++Cl2↑+2H2O p q 会有氯化氢杂质与乙醇反应,生成氯乙烷。导致三氯乙醛的纯度降低 停止对A加热或控制滴加盐酸的量 淀粉溶液 蓝色变为无色,且半分钟内不变色 66.4%(或66.375%)
【解析】A装置利用二氧化锰与浓盐酸制备氯气,反应的方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,B装置用饱和食盐水除去HCl,C装置盛放浓硫酸干燥氯气,D中反应制备CCl3CHO,E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气。
MnCl2+Cl2↑+2H2O,B装置用饱和食盐水除去HCl,C装置盛放浓硫酸干燥氯气,D中反应制备CCl3CHO,E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气。
(1)由仪器a的结构可知,该分液漏斗能平衡压强,使漏斗内液体顺利滴下,为恒压分液漏斗,故答案为:恒压分液漏斗;
(2)装置A中浓盐酸与二氧化锰在加热时反应放出氯气,反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)冷凝管水流遵循下口进上口出,即p口进,q口出,故答案为:p;q;
(4)装置B中的饱和食盐水可以除去氯气中的杂质氯化氢,若撤去装置B,氯化氢杂质会与乙醇反应,生成氯乙烷,导致三氯乙醛的纯度降低,故答案为:会有氯化氢杂质与乙醇反应,生成氯乙烷,导致三氯乙醛的纯度降低;
(5)实验时发现D中导管口处气泡速率过快,可以停止对A加热或控制滴加盐酸的量,适当降低生成氯气的速率,故答案为:停止对A加热或控制滴加盐酸的量;
(6)根据CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2-=H++2I-+CO2↑;I2+2S2O32-=2I-+S4O62-,反应过程中涉及碘单质,可以选用淀粉作指示剂;滴定终点的现象为蓝色变为无色,且半分钟内不变色;根据消耗的Na2S2O3计算剩余I2的物质的量0.02000molL-1×0.02L×![]() =2×10-4mol,与HCOO-反应的I2的物质的量为0.1000molL-1×0.02L-2×10-4mol=1.8×10-3mol,由CCl3CHO~HCOO-~I2可知,CCl3CHO的物质的量为1.8×10-3mol,则产品的纯度为
=2×10-4mol,与HCOO-反应的I2的物质的量为0.1000molL-1×0.02L-2×10-4mol=1.8×10-3mol,由CCl3CHO~HCOO-~I2可知,CCl3CHO的物质的量为1.8×10-3mol,则产品的纯度为![]() ×100%=66.4%,故答案为:淀粉溶液;蓝色变为无色,且半分钟内不变色;66.4%。
×100%=66.4%,故答案为:淀粉溶液;蓝色变为无色,且半分钟内不变色;66.4%。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:

回答下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)________(填“相同”或“不同”)。
(2)对实验3完成下列填空:
①铝为________极,电极反应式为___________________________。
②石墨为________极,电极反应式为__________________________。
③电池总反应式为________________________________。
(3)实验4中铝作________极(填“负”或“正”),理由是_________________________。此电池反应的离子方程式为_________________________。
(4)根据实验结果总结出影响铝在原电池中作正极或负极的因素为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在强酸性透明溶液中大量共存的是( )
A.Na+、K+、SO42-、OH-B.Na+、K+、Cl-、HCO3-
C.Na+、Cu2+、Cl-、SO42-D.NH4+、Ca2+、NO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是( )
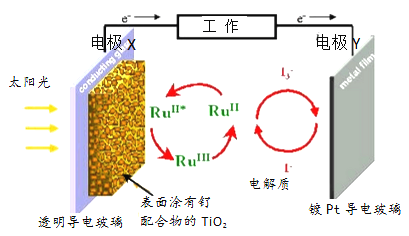
A. 镀铂导电玻璃的作用是传递I-
B. 电池工作时,光能转变为电能,X 为电池的正极
C. 电解质溶液中发生反应:2Ru3++3I-=2Ru2++I3-
D. 电池的电解质溶液中I-和I3-的浓度均不断减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________;K、F、Zn的电负性从大到小的顺序为___________。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________。
(3)OF2分子的几何构型为___________,中心原子的杂化类型为___________。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为___________个。
②晶胞中紧邻的两个F-间的距离为_______________________(列出算式即可)nm。
③该晶体的密度为___________(列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知环己烯可以通过丁二烯与乙烯发生环化加成反应得到. 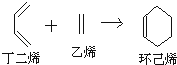 ,已知B、C、D、E、F五种烃有如下转化关系,B为苯的同系物,最多只有13个原子处于同一平面上,D中所有的原子一定在同一平面上.
,已知B、C、D、E、F五种烃有如下转化关系,B为苯的同系物,最多只有13个原子处于同一平面上,D中所有的原子一定在同一平面上.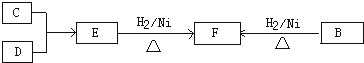
(1)写出B→F的化学方程式:
(2)满足条件的E的结构简式可能为 或
(3)满足条件的C的名称可能为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠广泛应用于染料工业。请完成下列各题:
(1)![]() 的核外电子排布式_______________,其核外有_______种不同运动状态的电子。写出Na2O的电子式___________,比较Na2O和Na2S的熔点高低:Na2O______Na2S。
的核外电子排布式_______________,其核外有_______种不同运动状态的电子。写出Na2O的电子式___________,比较Na2O和Na2S的熔点高低:Na2O______Na2S。
(2)O、S属于同主族元素,其单质的氧化性不同,用一反应的化学方程式表示:_____________,O、S、![]() 半径从大到小的顺序是_________________。
半径从大到小的顺序是_________________。
II.1100℃时,在体积固定且为5L的密闭容器中,发生可逆反应: ![]() 并达到平衡。
并达到平衡。
(1)上述平衡的平衡常数表达式![]() _____________。欲使
_____________。欲使![]() 值变大,可采取的措施是__________________________。平衡后,向容器中充入1mol H2,平衡向__________(填“正反应方向”、“逆反应方向”或“不移动”),重新达到平衡后,与原平衡相比,逆反应速率______(填“增大”、“减小”或“不变”)。
值变大,可采取的措施是__________________________。平衡后,向容器中充入1mol H2,平衡向__________(填“正反应方向”、“逆反应方向”或“不移动”),重新达到平衡后,与原平衡相比,逆反应速率______(填“增大”、“减小”或“不变”)。
(2)若混合气体的密度不变,(填“能”或“不能”)_________判断该反应已经达到平衡状态。若初始时加入的Na2SO4为2.84g,10分钟后达到平衡时Na2SO4的转化率为45%, ![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用化学方程式解释现行高中化学教材中的下列事实:
(1)用FeCl3溶液制作印刷电路板:_________________________________
(2)工业制漂白粉:______________________________________________
(3)由石英砂制粗硅:_____________________________________________
(4)玻璃刻花的反应原理:_____________________________________________
(5)盛放NaOH溶液的试剂瓶不能用玻璃塞:_______________________________
(6)氢氧化钠溶液腐蚀金属铝:_____________________________________________
(7)单质硅与氢氧化钠溶液的反应:__________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com