
【题目】下列依据热化学方程式得出的结论正确的是
A.已知NaOH(aq)+HCl(aq)=![]()
![]() H=-57.3
H=-57.3![]() 则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
B.已知2H2(g)+O2(g)=2H2O(g) ![]() H=-483.6
H=-483.6![]()
![]() 则氢气的燃烧热为241.8
则氢气的燃烧热为241.8![]()
C.已知![]() =
=![]()
![]() H=a
H=a![]()
![]() ===2CO(g)
===2CO(g)![]() H=b
H=b![]() 则a>b
则a>b
D.已知P(白磷,s)=P(红磷,s)![]() H<0,则白磷比红磷稳定
H<0,则白磷比红磷稳定
科目:高中化学 来源: 题型:
【题目】次氯酸钠是常见的消毒剂,实验室可用以下两种方法来制取次氯酸钠溶液:
方法一:向装有NaOH的溶液中通入氯气(装置如图所示);

方法二:向Na2CO3溶液中加入Ca(ClO)2,反应后过滤。
(1)写出方法一所发生反应的离子方程式___。
(2)NaOH溶液和氯气的反应为放热反应,随着温度的升高,会有副反应发生。为防止副反应的发生,可以采取的方法是___。
(3)方法二与方法一相比,优点除无副反应发生外,还有___、___。
(4)某次氯酸钠粗产品中混有的杂质为NaClO3,为测定粗产品中NaClO的质量分数,现进行如下实验:称取0.6173g样品于锥形瓶中,加水使样品完全溶解,向溶液中加入适量硫酸酸化,接着加入40mL0.5000mol·L-1的FeSO4溶液(过量),充分反应。再向锥形瓶中滴加0.0200mol·L-1的KMnO4溶液,恰好完全反应时消耗KMnO4溶液体积28.00mL。请计算样品中NaClO的质量分数(写出计算过程)。___
已知实验过程中发生的反应如下:
H++ClO-+Fe2+→Cl-+Fe3++H2O
H++ClO3-+Fe2+→Cl-+Fe3++H2O
H++MnO4-+Fe2+→Mn2++Fe3++H2O(以上反应均未配平)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式(或离子方程式)的类推正确的是( )
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中: Fe + Cu2+ = Cu + Fe2+ | 将Na加入到CuSO4溶液中: 2Na + Cu2+ = Cu + 2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性: 2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性: 2H++SO42﹣+Ba++2OH﹣=BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2: Ca2++2ClO﹣+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2: Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2mol![]() 和2mol
和2mol![]() 气体,充入固定体积的密闭容器,在一定条件下发生下列反应:
气体,充入固定体积的密闭容器,在一定条件下发生下列反应:![]() ,平衡时
,平衡时![]() 为nmol,相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,到达平衡时
为nmol,相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,到达平衡时![]() 的物质的量一定大于nmol的是
的物质的量一定大于nmol的是![]()
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
容器编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为![]()
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断开1molCl(g)中Cl-Cl键需要吸收243kJ能量,根据能量变化示意图,下列说法或热化学方程式正确的是( )

A.生成lmolH2(g)中的H-H键吸收436kJ能量B.H2(g)+Cl2(g)=2HCl(g) △H=-864kJ·mol-1
C.图示此反应为吸热反应D.HCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) △H=92.5kJ·mol-1
Cl2(g) △H=92.5kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容条件下,反应:2SO2 (g) + O2 (g) ![]() 2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
容器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是( )
A. 在上述条件下反应生成lmol SO3固体放热Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,在工农业生产生活中有着重要的应用。某化学兴趣小组同学利用以下装置制备氯气并对氯气的性质进行探究:
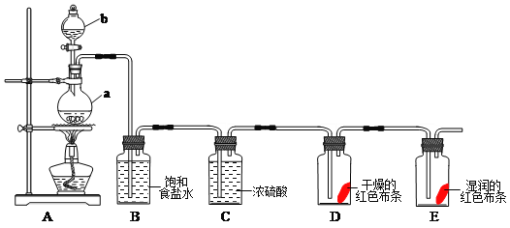
(1)有关氯气、氯水和氯离子的性质,下列说法正确的是_____________
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.Cl-和Cl2都具有很强的氧化性
C.新制氯水可以用来杀菌消毒是因为生成强酸 次氯酸
D.将新制氯水滴入AgNO3溶液,会出现白色沉淀
(2)仪器a的名称为___________,装置B中饱和食盐水的作用是_______________。
(3)装置A中发生反应的离子方程式为:____________________________________。
(4)装置D中的实验现象为__________________,装置E中的实验现象为________
(5)整套实验装置存在着明显缺陷,你的改进措施是__________________________。
(6)8.7gMnO2固体与足量浓盐酸充分反应,在标准状况下产生Cl2的体积为_____L;其中被氧化的HCl的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素A是一类重要的维生素,又称视黄醇.如果人体缺少维生素A,人易患夜盲症、干眼症等眼症.食用胡萝卜等蔬菜和鱼肝油,可以补充维生素![]() 维生素C是另一种重要的维生素,它能防治坏血病.维生素C与补铁剂同服,可以防止补铁剂中的
维生素C是另一种重要的维生素,它能防治坏血病.维生素C与补铁剂同服,可以防止补铁剂中的![]() 被氧化.下图分别是维生素
被氧化.下图分别是维生素![]() 和维生素C的结构简式,以下说法不正确的是
和维生素C的结构简式,以下说法不正确的是
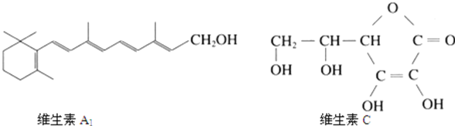
A.维生素![]() 的分子式为
的分子式为![]()
B.1mol维生素![]() 最多可以与5mol
最多可以与5mol![]() 发生加成反应
发生加成反应
C.维生素C有还原性
D.维生素C在碱性溶液中不易变质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com