
【题目】化学平衡研究的对象是
A. 中和反应 B. 离子反应 C. 可逆反应 D. 氧化反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-= Cl-+ ClO-+ H2O
B. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2 ↑+ H2O
C. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+ CH3COO—
D. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0 mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66 g,并有气体放出。试计算:
(1)写出Na2SO4的电离方程式;
(2)原混合溶液中Na2CO3和Na2SO4的物质的量浓度;
(3)产生的气体在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是

A. a点对应溶液的导电性比d点强
B. 氢硫酸的酸性比亚硫酸的酸性强
C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀
D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图中A~I均为中学化学中常见物质.其中A、B、 C、D为单质,通常情况下A为黄绿色气体,B为固体,C、D为无色气体:其余为化合物,其中常温下E是无色气体.其水溶液为强酸,G是具有磁性的物质,常温下I为液体。
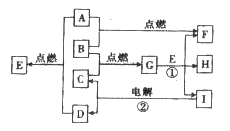
(1)写出下列物质的化学式:A________;F______;G_________。
(2)反应①的离子方程式为______________________________________。
(3)实验室要除去A气体中少量E,将混和气体通过盛有__________的洗气瓶洗气。
(4)F、 H可相互转化,写出一种F转化为H的化学方程式:__________________。
(5)请设计一组实验方案检验F中阳离子:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. HCl溶液中无OH- B. NaOH溶液中无H+
C. KCl溶液中既无H+也无OH- D. 常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com