
【题目】甲醇既是重要的化工原料,又是电动公交车的清洁能源,利用水煤气在一定条件下含成甲醇,发生的反应为:CO (g) +2H2(g)![]() CH3OH(l) △H=?
CH3OH(l) △H=?
(1)己知CO、H2、CH3OH的燃烧热分别为283.0kJ/mol,285.8kJ/mol,726.5kJ/mol 则△H=______。
(2)在一容积为2L的恒容密闭容器中加入0.2mol CO和0.4mol H2,发生如下反应:CO (g) +2H2(g)![]() CH3OH(g),实验测得T1℃和T2℃下,甲醇的物质的量随时间的变化如下表所示,下列说法正确的是
CH3OH(g),实验测得T1℃和T2℃下,甲醇的物质的量随时间的变化如下表所示,下列说法正确的是
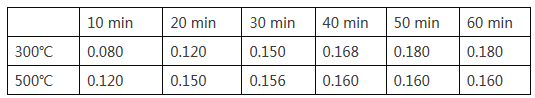
①由上述数据可以判断:T1℃_____T2℃
②T1℃时,0~20minH2的平均反应速率v(H2)=_________。
③该反应T1℃达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是_____(选填编号)。
A.改用高效催化剂 B.升高温度 C.缩小容器体积 D.分离出甲醇 E.增加CO的浓度
(3)若保持T1℃不变,起始时加入CO、H2、CH3OH的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,则a、b、c应该满足的条件___________。
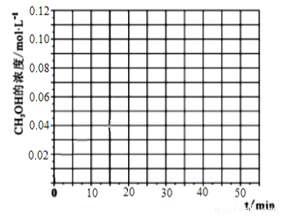
(4)当反应在T1℃达到20min时,控制体积不变,迅速将0.02molCO,0.04molH2,0.18molCH3OH同时投入体系中,后在恒压条件下,反应在40min时达到平衡,请在图中画出2040min内容器中 H2浓度的变化趋势曲线:___________
(5)在以CH3OH(l)为燃料的燃料电池中,电解质溶液为酸性,则负极的电极反应式为__________;理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,则该燃料电池的理论效率为______。(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)
【答案】 -128.1kJ/mol < 0.006mol/(L·min) C、E a+c=0.2,b+c/2=0.4 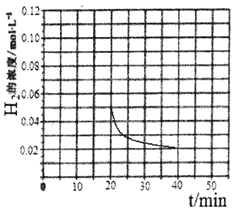 CH3OH-6e-+H2O=CO2+6H+ 80%
CH3OH-6e-+H2O=CO2+6H+ 80%
【解析】本题考查盖斯定律的应用、化学反应速率的计算和影响因素,等效平衡以及影响平衡的因素,化学图像和燃料电池等知识,利用基础知识解答。
(1)因为CO、H2、CH3OH的燃烧热分别为283.0kJ/mol,285.8kJ/mol,726.5kJ/mol,所以①CO(g)+ ![]() O2(g)=CO2(g) △H=-283.0kJ/mol、②H2(g)+
O2(g)=CO2(g) △H=-283.0kJ/mol、②H2(g)+ ![]() O2(g)=H2O(l)△H=-285.8kJ/mol、③CH3OH(l)+
O2(g)=H2O(l)△H=-285.8kJ/mol、③CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l) △H=-726.5kJ/mol,根据盖斯定律,①+2×②-③得CO (g) +2H2(g)
O2(g)=CO2(g)+2H2O(l) △H=-726.5kJ/mol,根据盖斯定律,①+2×②-③得CO (g) +2H2(g)![]() CH3OH(l)的△H=-283.0kJ/mol-285.8kJ/mol×2+726.5kJ/mol=-128.1kJ/mol。
CH3OH(l)的△H=-283.0kJ/mol-285.8kJ/mol×2+726.5kJ/mol=-128.1kJ/mol。
(2)①根据上述分析,CO和氢气反应生成甲醇的反应是放热反应,升高温度,平衡逆向移动,达平衡时甲醇的物质的量减少,再根据表格提供的数据可判断,T1℃<T2℃;②T1℃时,0~20min时生成甲醇0.120mol,则反应掉氢气0.240mol,所以H2的平均反应速率v(H2)=0.240mol÷(2L×20min)=0.006mol/(L·min);③A.改用高效催化剂只能加快反应速率,不能改变平衡,故A错误;B.升高温度,平衡逆向移动,甲醇的生成量减少,故B错误;C.缩小容器体积 ,增大压强,平衡正向移动,反应速率加快且甲醇的生成量增加,故C正确;D.分离出甲醇导致化学反应速率减慢,故D错误; E.增加CO的浓度,平衡正向移动,反应速率加快且甲醇的生成量增加,故E正确;故选CE。
(3)在一容积为2L的恒容密闭容器中,原平衡起始加入0.2mol CO和0.4mol H2,根据等效平衡理论,将生成物全部转移到左边,使得左边反应物CO为0.2mol,氢气为0.4mol,就能得到等效平衡,所以保持T1℃不变,起始时加入CO、H2、CH3OH的物质的量分别为amol、bmol、cmol,达到平衡时,仍与原平衡等效,a、b、c满足的条件为a+c=0.2,b+c/2=0.4。
(4)根据题给数据,20min时氢气的浓度为0.5mol/L,起始加入0.2mol CO和0.4mol H2,20min时再加入0.02molCO,0.04molH2,0.18molCH3OH,相当于加入0.2molCO和0.4mol氢气,在恒压条件下,反应在40min时达到平衡,与原平衡是等效平衡,平衡时氢气的浓度为0.02mol/L,所以2040min内容器中 H2浓度的变化趋势曲线为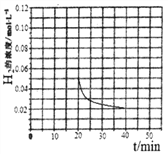 。
。
(5)酸性条件下甲醇燃料电池的总反应式为:CH3OH+![]() O2═CO2+2H2①,酸性条件下该燃料电池的正极反应式为
O2═CO2+2H2①,酸性条件下该燃料电池的正极反应式为![]() O2+6H++6e-═3H2②,①-②得电池负极反应式为:CH3OH-6e-+H2O=CO2+6H+ ;该燃料电池的理论效率为1162.4÷(726.5×2)×100%=80%。
O2+6H++6e-═3H2②,①-②得电池负极反应式为:CH3OH-6e-+H2O=CO2+6H+ ;该燃料电池的理论效率为1162.4÷(726.5×2)×100%=80%。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】下列关于化学键说法正确的是( )
A.构成单质分子的微粒中不一定含有化学键
B.只含有共价键的物质一定是共价化合物
C.NaCl溶于水破坏了离子键,乙醇溶于水破坏了共价键
D.CaCl2 中既有共价键又有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A. 升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B. 0.l0mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C. CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D. 室温下,欲使0.1mol/L醋酸溶液的pH,电离度a都减小,可加入少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用一固体废渣(主要成份为Al2O3·Cr2O3,还含有FeO、SiO2)为主要原料回收利用,生产红矾钠晶体(Na2Cr2O7·2H2O),同时制备明矾(KAl(SO4)2·12H2O)。其主要工艺流程如下:
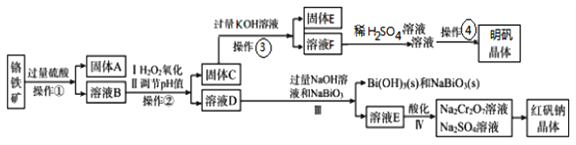
己知:NaBiO3不溶于冷水,在碱性条件下能将Cr3+氧化为CrO42-
(1)I、II目的是___________。
(2)实验室中操作④的名称为_______________。
(3)己知:Ksp[Fe(OH)3]=3.0×10-39,Ksp[Al(OH)3]=3×10-33。当pH=5.6时Cr(OH)3开始沉淀。室温下,II中需调节溶液pH范围为___________(杂质离子浓度小于1×10-6mol/L视为沉淀完全)。
(4)写出Ⅲ中发生反应的离子方程式_____________。
(5)IV中酸化是用硫酸而不用盐酸酸化,理由是_____________(结合化学方程式回答)。
(6)写出溶液F和硫酸溶液反应的离子方程式_________,若用足量二氧化碳通入F中,则生成的溶液中离子浓度关系为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3S+6KOH=2K2S+K2SO3+3H2O中,被还原的硫与被氧化的硫的质量比为( )
A.2:1 B.1:2 C.3:1 D.1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g),下列叙述中不正确的是( )

A. Zn和H2SO4的总能量大于ZnSO4和H2的总能量
B. 反应过程中能量关系可用上图表示
C. 若将该反应设计成原电池,则Zn为负极
D. 若将该反应设计成原电池,当有32.5g锌溶解时正极放出11.2 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作正确的是
A. 用pH试纸测得某新制氯水的pH值为3.5
B. 用酸式滴定管量取酸性高锰酸钾溶液5.10mL
C. 用标准盐酸溶液滴定一定体积的待测NaOH溶液时,用待测溶液润洗锥形瓶
D. 用l0 mL的量简量取8.05mL浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应可用于合成CH3OH:
![]()
(1)Mn2+基态核外电子排布式为____________。
(2)与NO3-互为等电子体的分子为_______(写化学式)。
(3)CO32-的空间构型是________(用文字描述)。
(4)1molCH3OH中含有σ键的数目为______mol。CH3OH与H2O可以任意比互溶,除因为它们都是极性分子外,还因为________。
(5)锰元素的一种硫化物晶体的晶胞结构如图所示,该硫化物的化学式为________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com