
����Ŀ�������£������� NaOH ��Һ��ζ��ĵζ�������ͼ��ʾ�������й���������ȷ�� �ǣ� ��

A.���� a ���� NaOH ��Һ�ζ�����ĵζ�����
B.���� a ������ b �ζ������о����ڣ�c(H+)+c(Na+)=c(OH-)+2c(SO42-)
C.�� NaOH ��Һ�ζ�������Һʱ���÷�̪��ָʾ��
D.������������� NaOH ��Һ�ֱ�����������۷� Ӧ���� H2 ��������һ��Ϊ 1:3
���𰸡�D
��������
A������ a ��pH���������Ա�ʾNaOH ��Һ�ζ���������ߣ���A��ȷ��
B�����ݵ���غ㣬�ζ����̵��κ�ʱ�̶����ڵ���غ㣺c(H+)+c(Na+)=c(OH-)+2c(SO42-)����B��ȷ��
C��ǿ�ᡢǿ����ζ������ü��Ȼ��̪��ָʾ������C��ȷ��
D����ͼ���֪�������Ũ����0.05mol/L���������Ƶ�Ũ����0.1mol/L�������۲��㣬��������ȫ��Ӧ���ų�������һ���࣬��D����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ��ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ� ��
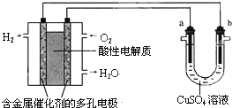
A.ȼ�ϵ�ع���ʱ��������ӦΪO2+4H++4e����2H2O
B.a����ͭ��b������ʱ����ʵ�����϶�ͭ
C.a���Ǻ�п�����Ĵ�ͭ��b���Ǵ�ͭ��a���ܽ�ͭ��������b��������ͭ�������
D.��a��b������Ϊʯīʱ������ͬ�����£�a���������������������ĵ�H2�������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ռ���Ʒ���������������õ����ʣ�Ϊ�ⶨ���ȣ��������µζ�������
A.�� 250 mL ������ƿ�ж������ 250 mL �ռ���Һ
B.����Һ����ȡ 25 mL �ռ���Һ����ƿ�в��μ���ָʾ������
C.����ƽ��ȷ��ȡ�ռ���Ʒ Wg�����ձ���������ˮ�ܽ�
D.�����ʵ���Ũ��Ϊ c �ı�������Һװ����ʽ�ζ��ܣ�����Һ�棬�ǿ�ʼ����Ϊ V1 E������ƿ�µ�һ�Ű�ֽ���ζ����յ㣬�Ƕ��� V2
�ش����и����⣺
(1)��ȷ���������˳���ǣ�����ĸ��д�� _______�� ________�� ________��D�� ______��
(2)D ������Һ��Ӧ���ڵ� ______�����첿��Ӧ ______��
(3)�ζ��յ�ʱ��ƿ����ɫ�仯�� ______��
(4)����ʽ�ζ��ܲ��ñ�������ϴ����������������ȷ��ǰ���£���Բⶨ�����ָ�ռ�Ĵ��ȣ��к�Ӱ�죿______������ƫ������������������������
(5)���ռ���Ʒ���ȵļ���ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������̼���ɼ���Ĺ�����ͼ��ʾ������˵����ȷ���ǣ�NAΪ�����ӵ�������ֵ��
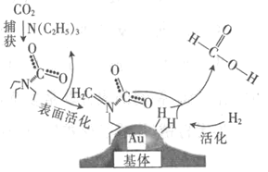
A.��״���£�22.4 L CO2�������ĵ�����ĿΪ16NA
B.10.1 g N��C2H5��3�������ļ��Թ��ۼ���ĿΪ2.1NA
C.2 mol Au��2 mol H2�������ķ�����Ŀ��Ϊ2NA
D.100 g 46%�ļ���ˮ��Һ����������ԭ����ĿΪ5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ���ʾ�����л��
(1)��ϵͳ�����������л���![]() �������� _________��
�������� _________��
(2) 4��4��5-����-2-��Ȳ(д���ṹ��ʽ)_________________
(3) ����������ϩ(д��������ʽ)__________________
(4) 2��2-����-3-�һ�-4-���������(д���ṹ��ʽ)___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2 mol��L��1��KOH��Һ��0.1 mol��L��1��H2SO3��Һ�������Ϻ���Һ�и�����Ũ�ȴ�С��ϵ��ȷ����(����)
A.c(K��)��c(H��)��c(OH��)��c(![]() )��c(
)��c(![]() )
)
B.2c(K��)��c(![]() )��c(
)��c(![]() )��c(H2SO3)
)��c(H2SO3)
C.c(K��)��c(![]() )>c(
)>c(![]() )��c(H2SO3)
)��c(H2SO3)
D.c(![]() )��c(
)��c(![]() )��c(H2SO3)��0.1 mol��L��1
)��c(H2SO3)��0.1 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Լ��������Թ��е����������������ʵ��Ŀ�������ǣ� ��
ʵ��Ŀ�� | �Լ� | �Թ��е����� | |
A | �ǻ��Ա����Ļ�����Ӱ�� | ������ˮ | �ٱ� �ڱ�����Һ |
B | ���Ա����Ļ�����Ӱ�� | ����KMnO4��Һ | �ٱ� �ڼױ� |
C | ��������û��̼̼˫�� | Br2��CCl4��Һ | �ٱ� �ڼ�ϩ |
D | ̼������Աȱ���ǿ | ʯ����Һ | �ٱ�����Һ ��̼����Һ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����˽̰�̲�ʵ�顰��200mL�ձ��з���20g���ǣ�C12H22O11������������ˮ��������ȣ�Ȼ���ټ���15mL��������Ϊ98%Ũ���ᣬѸ�ٽ��衱��������̽����
��1���۲����������ȱ�ƣ�����ڣ�������ͣ��γ����ɶ�ĺ���״��ɫ���ʣ�ͬʱ�ŵ��̼�����ζ����ѹ�˺�ɫ����ʱ���о���Ӳ������ˮ�г�Ư��״̬��ͬѧ�������������Ʋ�����н��ۣ�
��Ũ�������ǿ������ ��Ũ���������ˮ�� ��Ũ���������ˮ�Ԣ�Ũ����������� �ݺ�ɫ���ʾ���ǿ������
�������ݲ���ֵ���_________������ţ���
��2��Ϊ����֤������Ũ���ᷴӦ���ɵ���̬���ͬѧ�����������װ�ã�

�Իش��������⣺
��ͼ1��A�����ѡ������װ��_________�����ţ���
��ͼ1�� Bװ����װ�Լ���_________��Dװ�����Լ���������_________��Eװ���з�����������_________��
��ͼ1��Aװ����ʹ�����ȱ�ڵĻ�ѧ��Ӧ����ʽΪ_________����������͵Ļ�ѧ����ʽΪ��_________��
��ijѧ����ͼ2����ʵ��ʱ������DƿƷ�첻��ɫ��Eװ�����������ݳ���Fװ�������Ը��������Һ��ɫ��dz���Ʋ�Fװ�������Ը��������Һ��ɫ��dz��ԭ��_________���䷴Ӧ�����ӷ���ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵������ȷ����
A.1 L 0.1 mol��L��1 AlCl3��Һ����������Ϊ0.4NA
B.����ͭ����������������32 g�����·��һ��ͨ��NA������
C.N2(g) + 3H2(g)![]() 2NH3(g) ��H����92.4 kJ��mol��1 ���ų�46.2 kJ��������Ӧ����N2������Ϊ0.5NA
2NH3(g) ��H����92.4 kJ��mol��1 ���ų�46.2 kJ��������Ӧ����N2������Ϊ0.5NA
D.1 mol FeCl3��ȫˮ�����ɵ�Fe(OH)3������ĿС��NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com