
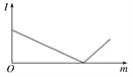
【题目】下列各组溶液,当后一种溶液逐滴加入到一定量的前一种溶液中并稍过量,其溶液的导电性(I表示导电能力)与后一种溶液的质量(m)的函数关系符合下图的是
A. 澄清石灰水、碳酸钠溶液
B. 硝酸银溶液、氯化钠溶液
C. 盐酸、氢氧化钠溶液
D. 稀硫酸、氢氧化钡溶液
【答案】D
【解析】
溶液的导电性与单位体积内离子的数目、离子所带电荷多少有关,单位体积内离子数目越多,导电性越强;离子所带电荷越多,导电性越强(如两个氯离子和一个硫酸根离子导电性相当)进行分析作答。
A. 澄清石灰水和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故A项错误;
B. 硝酸银溶液和氯化钠溶液反应生成氯化银沉淀和硝酸钠,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故B项错误;
C. 盐酸和氢氧化钠溶液反应生成氯化钠和水,溶液中的离子数目没有明显减少,所以导电性不会明显减弱至接近零,故C项错误;
D. 稀硫酸和氢氧化钡溶液反应硫酸钡沉淀和水,水难电离,硫酸钡难溶于水,所以溶液的导电性不断减弱,当氢氧化钡溶液和硫酸恰好反应,导电性最弱接近零,当氢氧化钡溶液过量时,溶液中的离子数目又增多,导电性增强,符合题意,故D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】研究NO、NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)与氮氧化物有关的全球或区域性大气环境问题有_______(填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为___________。若该反应有0.6NA个电子转移,则参加反应的NO2的物质的量为___________。
(3)NH3也是重要的含氮化合物,实验室用NH4Cl和Ca(OH)2制取NH3。
①写出反应的化学方程式_________________
②若用下图所示装置收集氨气,气体由_____口进入。

(4)硝酸可与不活泼金属铜发生反应。将过量的铜置入一定量的浓硝酸中,微热,充分反应后,待反应停止,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式解释)_____________________
(5)若将12.8 g铜跟一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则整个反应过程中,被还原的HNO3总的物质的量是___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某酸H3A水溶液中含A的各种粒子的分布分数(平衡时某种粒子的浓度占各粒子浓度之和的分数)与pH关系图如下所示,下列说法正确的是
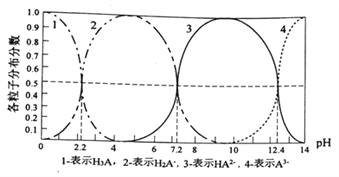
A. NaH2A水溶液呈碱性
B. H3A溶液中存在:c(H+)=c(OH-)+c(H2A-)+![]() c(HA2-)+
c(HA2-)+![]() c(A3-)
c(A3-)
C. 向H3A溶液中加入一定量的NaOH溶液至pH=5时,![]()
D. 向H3A溶液中加入氨水使PH从5→9发生的主要离子反应是:H2A-+OH-=HA2-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图是研究甲烷与氯气反应的实验装置图。
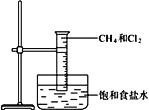
(1)CCl4的电子式:________________。
(2)二氯甲烷_____________同分异构体(填“有”或“没有”)。
(3)请完成一氯甲烷与氯气发生反应的化学方程式:CH3Cl+Cl2![]() ________+HCl,该反应属于反应_________(填有机反应类型)。
________+HCl,该反应属于反应_________(填有机反应类型)。
Ⅱ.(4)写出下列有机物的结构简式:
①2,2﹣二甲基戊烷:_____________
②3﹣甲基﹣1﹣丁烯:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 澄清石灰水与过量碳酸氢钠溶液反应:![]() +Ca2++OH﹣=CaCO3↓+H2O
+Ca2++OH﹣=CaCO3↓+H2O
B. 硫酸氢钠溶液中加入氢氧化钡溶液至中性:H++![]() +Ba2++OH﹣=BaSO4↓+2H2O
+Ba2++OH﹣=BaSO4↓+2H2O
C. 向氢氧化钠溶液中通入足量CO2:2OH﹣+CO2=![]() +H2O
+H2O
D. 向氢氧化钡溶液中加入过量硫酸:2H++![]() +Ba2++2OH﹣=BaSO4↓+2H2O
+Ba2++2OH﹣=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
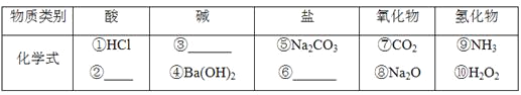
【题目】无机化合物可根据其组成和性质进行分类。
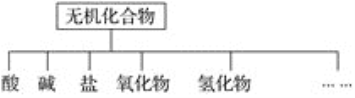
(1)上图所示的物质分类方法名称是________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表中。
___________、______________、_______________
(3)写出⑦转化为⑤的化学方程式:__________________________________________。
(4)实验室制备⑦常用________和________反应,检验该气体的方法是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
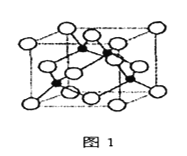
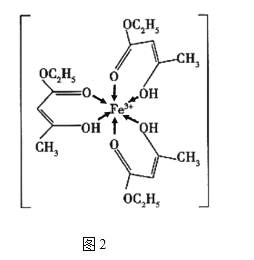
【题目】金属铁、铜及其化合物在科学研究和工业生产中具有重要的用途。下图1表示铜与氯形成化合物A的晶胞(黑球代表铜原子)。图2是Fe3+与乙酰乙酸乙酯形成的配离子B。
回答下列问题
(1)基态Cu原子的核外电子排布式为____________________________。
(2)从原子结构角度分析,第一电离能I1(Fe)与I1(Cu)的关系是:I1(Fe)________I1(Cu)(填“>“<”或“=”)
(3)化合物A的化学式为____________,Cl原子的配位数是____________。
(4)B中碳原子的杂化轨道类型为________,含有的化学键为________(填字母)。
a.离子键 b.金属键 c.极性键 d.非极性键
e.配位键 f.氢键 g.σ键 h.π键
(5)化合物A难溶于水,但易溶于氨水,其原因可能是________________;与NH3互为等电子体的分子有________________(写化学式,一种即可)。NH3的键角大于H2O的键角的主要原因是________________________________________。
(6)已知化合物A晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则该晶体中两个Cu原子之间的最短距离为________________________nm(列出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辛烷(C8H18)是汽油的重要成分,其与O2反应的能量变化如图所示。下列判断正确的是
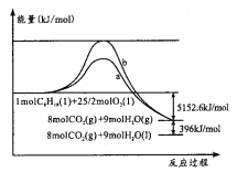
A. 曲线b代表加入催化剂时的能量变化
B. 反应物的总能量小于生成物的总能量
C. 表示辛烷燃烧热的热化学方程式:C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g) ΔH=-5152.6kJ/mol
D. 反应a、b的活化能不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应不属于氧化还原反应的是
A. 2NaOH+H2SO4===Na2SO4+2H2O B. 3CO+Fe2O3![]() 3CO2+2Fe
3CO2+2Fe
C. 2Na+2H2O====2NaOH+H2↑ D. 2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com