
【题目】某同学用KSCN溶液和![]() 溶液探究
溶液探究![]() 的还原性时出现异常现象,实验如下:
的还原性时出现异常现象,实验如下:
|
|
|
|
|
|
溶液变红,大约10秒左右红色褪去,有气体生成 | 溶液变红且不褪色,有气体生成 | 溶液变红且不褪色,滴加盐酸和 |
下列说法不正确的是
A.对比![]() ,可以判定酸性条件下
,可以判定酸性条件下![]() 可以氧化
可以氧化![]()
B.实验![]() 中发生的氧化还原反应有两种
中发生的氧化还原反应有两种
C.![]() 中红色溶液中含有
中红色溶液中含有![]() 胶体
胶体
D.![]() 中发生的氧化还原反应为:
中发生的氧化还原反应为:![]()
【答案】B
【解析】
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,滴入过氧化氢发生氧化还原反应,生成铁离子,形成血红色溶液,大约10秒左右红色褪去,铁离子做催化剂过氧化氢分解有气体生成
,滴入过氧化氢发生氧化还原反应,生成铁离子,形成血红色溶液,大约10秒左右红色褪去,铁离子做催化剂过氧化氢分解有气体生成![]() 经检验为
经检验为![]() ,取褪色后溶液,滴加盐酸和
,取褪色后溶液,滴加盐酸和![]() 溶液,产生白色沉淀为硫酸钡沉淀,证明
溶液,产生白色沉淀为硫酸钡沉淀,证明![]() 离子被氧化为硫酸根离子,
离子被氧化为硫酸根离子,
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,滴入过氧化氢溶液,溶液变红且不褪色,说明亚铁离子被氧化为铁离子,铁离子对过氧化氢起到催化剂作用,有气体生成
,滴入过氧化氢溶液,溶液变红且不褪色,说明亚铁离子被氧化为铁离子,铁离子对过氧化氢起到催化剂作用,有气体生成![]() 经检验为
经检验为![]() ,经检验有丁达尔效应,说明生成了氢氧化铁胶体,
,经检验有丁达尔效应,说明生成了氢氧化铁胶体,
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,通入足量氧气,溶液变红且不褪色,说明氧气氧化亚铁离子生成铁离子,滴加盐酸和
,通入足量氧气,溶液变红且不褪色,说明氧气氧化亚铁离子生成铁离子,滴加盐酸和![]() 溶液,无白色沉淀,经检验无丁达尔效应,无硫酸钡沉淀生成和氢氧化铁胶体形成,排除了氧气氧化
溶液,无白色沉淀,经检验无丁达尔效应,无硫酸钡沉淀生成和氢氧化铁胶体形成,排除了氧气氧化![]() 的可能。
的可能。
A.对比![]() ,实验
,实验![]() 确定了
确定了![]() 离子被氧化为硫酸根离子,实验
离子被氧化为硫酸根离子,实验![]() 排除了氧气氧化
排除了氧气氧化![]() 的可能,可以判定酸性条件下
的可能,可以判定酸性条件下![]() 可以氧化
可以氧化![]() ,故A正确;
,故A正确;
B.实验![]() 中发生的氧化还原反应有亚铁离子被过氧化氢氧化为铁离子,过氧化氢分解生成氧气,氧气氧化亚铁离子,不止两种,故B错误;
中发生的氧化还原反应有亚铁离子被过氧化氢氧化为铁离子,过氧化氢分解生成氧气,氧气氧化亚铁离子,不止两种,故B错误;
C.![]() 中检验有丁达尔效应,说明红色溶液中含有
中检验有丁达尔效应,说明红色溶液中含有![]() 胶体,故C正确;
胶体,故C正确;
D.![]() 中通入足量氧气溶液变红色说明生成了铁离子,发生的氧化还原反应为:
中通入足量氧气溶液变红色说明生成了铁离子,发生的氧化还原反应为:![]() ,故D正确;
,故D正确;
故选:B。


科目:高中化学 来源: 题型:
【题目】一氯甲烷等卤代烃跟苯的反应如图所示,(无机小分子产物略去)。下列说法正确的是

A. 该反应属于化合反应
B. b的二氯代物有6种结构
C. 1mol b加氢生成饱和烃需要6molH2
D. C5H11Cl的结构有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在工业生产和日常生活中有重要用途。
在工业生产和日常生活中有重要用途。
I.工业上用钛矿石![]() ,含FeO、
,含FeO、![]() 、
、![]() 等杂质
等杂质![]() 经过下述反应制得:
经过下述反应制得:

其中,步骤![]() 发生的反应为:
发生的反应为:![]() 。
。
![]() 净化钛矿石时,是否需要除去杂质FeO?答: ______
净化钛矿石时,是否需要除去杂质FeO?答: ______ ![]() 填“需要”或“不需要”
填“需要”或“不需要”![]() 。
。
![]() 净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: ______; ______。
净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: ______; ______。
![]() 可通过下述两种方法制备金属钛:
可通过下述两种方法制备金属钛:
“方法一”是电解![]() 来获得Ti:将处理过的
来获得Ti:将处理过的![]() 作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
![]() 阴极反应的电极反应式为 ______。
阴极反应的电极反应式为 ______。
“方法二”是先将![]() 与
与![]() 、C反应得到
、C反应得到![]() ,再用镁还原得到
,再用镁还原得到![]() 。因下述反应难于发生:
。因下述反应难于发生:
![]() 所以不能直接由
所以不能直接由![]() 和
和![]() 反应
反应![]() 即氯化反应
即氯化反应![]() 来制取
来制取![]() 。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
![]() 已知:
已知:![]()
![]() 。请写出
。请写出![]() 与
与![]() 、C反应制各
、C反应制各![]() 的热化学方程式: ______。
的热化学方程式: ______。
![]() 从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因_______________。
从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图:
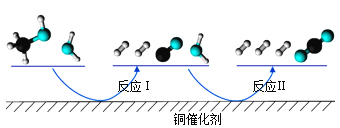

下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量
C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和氯化钠溶液制取氢氧化钠的工艺流程:
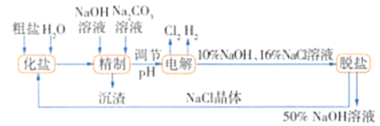
依据图中所给信息,完成下列填空:
(1)电解时发生反应的化学方程式为________________。
(2)粗盐含Ca2+、Mg2+等杂质,加入NaOH溶液、Na2CO3溶液的目的就是除去这些杂质,但如果精制时发现其中SO42-含量也较高,必须添加含钡离子的试剂除去SO42-,该试剂可以是________(填序号)。
a. Ba(OH)2溶液 b.Ba(NO3)2溶液 c.BaCl2溶液
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为________(填序号)。
a.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂
b.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液
c.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住。 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色。 |
下列说法不合理的是
A.烧杯A中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B.红棕色气体消失可能与NO2和烧杯C中的KI发生反应有关
C.烧杯A中溶液变蓝是因为产生了Cu(NO3)2
D.若将铜片换成铁片,则C中的液体不会变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的操作,对应的现象以及结论都正确的是![]()
![]()
选项 | 操作 | 现象 | 结论 |
A | 向 | 产生白色沉淀 |
|
B | 蘸有浓氨水的玻璃捧靠近X | 有白烟产生 | X一定是浓盐酸 |
C | 向澄清石灰水加入某试剂的溶液少许 | 产生白色沉淀 | 该试剂中一定含有 |
D | 炭粉中加入浓硫酸并加热,导出的气体通入 | 有白色沉淀产生 | 有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
A. 在常温常压下,11.2 L N2含有的原子数为NA
B. 32 g O2在标准状况下所占体积约为22.4 L
C. 标准状况下,18 g H2O所占的体积约为22.4 L
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com