
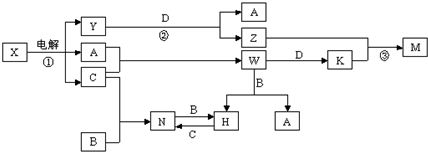
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
| ||
| ||
| ||
| ||


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʵ����ȷ���Ƿ���Cl-��NO3- |
| B����Һ�п϶�����CO32-��SO42-����Ũ�ȷֱ�Ϊ4.00mol/L��2.00mol/L |
| C������ʵ��ȷ����Һ�п϶�������Mg2+��Fe3+��Al3+ |
| D��Ҫȷ���Ƿ���K+��Ӧ��һ������ɫ��Ӧʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
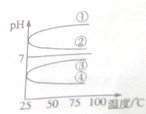 A��B��C��D��E������Һ�ֱ���NaOH��NH3?H2O��CH3COOH��HCl��NH4HSO4�е�һ�֣������½�������ʵ�飺
A��B��C��D��E������Һ�ֱ���NaOH��NH3?H2O��CH3COOH��HCl��NH4HSO4�е�һ�֣������½�������ʵ�飺| c(B) |
| c(OH-) |
| c(OH-) |
| c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�ϡ��0.1 mol/L�İ�ˮ����Һ��c��OH-����c��NH4+����c��H+�����½� |
| B�������£�c��NH4+����ȵĢ٣�NH4��2SO4 �ڣ�NH4��2Fe��SO4��2 ��NH4Cl �ܣ�NH4��2CO3��Һ�У��������ʵ���Ũ�ȴ�С��ϵ�ǣ��ڣ��٣��ܣ��� |
| C��pH=8.3��NaHCO3��Һ��c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
| D������Һ�д��ڵ�����ֻ��Cl-��OH-��NH4+��H+ʱ������Һ������Ũ�ȴ�С��ϵ����Ϊc��Cl-����c��NH4+����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
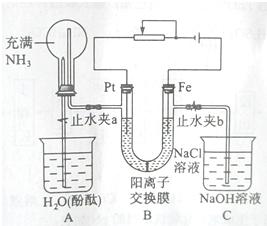
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 5 |
| 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
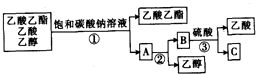
| A�������� �ڹ��� �۷�Һ |
| B���ٷ�Һ ������ ������ |
| C�������� �ڷ�Һ �۷�Һ |
| D���ٷ�Һ ������ �۽ᾧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ��� |
| A����ع���ʱ�������缫��ӦʽΪ��2MnO2+H2O+2e-=Mn2O3+2OH- |
| B����س��ʱ�����Դ���������ĵ缫��ӦΪ��Zn��OH��2+2e-=Zn+2OH- |
| C����ع���ʱ������������ͨ�����·���� |
| D����ع���ʱ�����·��ÿͨ��0.2mol���ӣ�п�����������ϼ�С6.5g |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com