
【题目】下列选项中,对于指定项目的数目前后相等的是 ( )
A.电子数:17gOH—与1mol-OH
B.双键数目:1mol![]() 与4mol C2H4
与4mol C2H4
C.分子数:常温常压下16g氧气与4g氦气
D.阴离子总数:72gCaO2与62g Na2O
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。

(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__________。
(2)装置②中主要玻璃仪器的名称__________、__________、__________。
(3)实验室制备Cl2的离子方程式为____________。
(4)装置③中Cu的作用__________(用化学方程式表示)。
(5)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__________。
(6)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到__________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的 元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______。基态碳原子的核外电子占有______个原子轨道。
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、![]() (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN 中 C 的杂化方式有______。1mol PAN 中含有的σ键数目为______。组成PAN 的元素的电负性大小顺序为______。
②相同压强下,HCOOH 的沸点比 CH3OCH3______(填“高”或“低”),
(3)水溶液中有 H3O+、H5O2+ 、H9O4 + 等微粒的形式。请画出 H5O2 的结构式:______。
(4)硅和碳在同一主族。下图为 SiO2 晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是______nm。
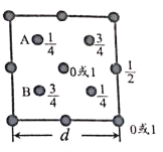 (d 的单位为 nm)
(d 的单位为 nm)
查看答案和解析>>
科目:高中化学 来源: 题型:
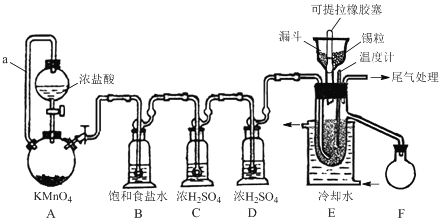
【题目】实验室可用溢流法连续制备无水四氯化锡(SnCl4)。SnCl4易挥发,极易发生水解,Cl2极易溶于SnCl4。制备原理与实验装置图如下:
Sn(s)+2Cl2(g)=SnCl4(l) ΔH = –511kJmol-1
可能用到的有关数据如下:
物质 | Sn | SnCl4 | CuCl2 |
熔点/℃ | 232 | -33 | 620 |
沸点/℃ | 2260 | 114 | 993 |
制备过程中,锡粒逐渐被消耗,须提拉橡胶塞及时向反应器中补加锡粒。当SnCl4液面升至侧口高度时,液态产物经侧管流入接收瓶。回答下列问题:
(1)a管的作用是________。
(2)A中反应的离子方程式是________。
(3)D的作用是________。
(4)E中冷却水的作用是________。
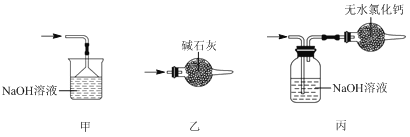
(5)尾气处理时,可选用的装置是________(填序号)。
(6)锡粒中含铜杂质致E中产生CuCl2,但不影响F中产品的纯度,原因是________。
(7)SnCl4粗品中含有Cl2,精制时加入少许锡屑后蒸馏可得纯净的SnCl4。蒸馏过程中不需要用到的仪器有________(填序号)。
A.蒸馏烧瓶 B.温度计 C.接收器 D.冷凝管 E.吸滤瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把10.2g Na2CO3·10H2O和NaHCO3组成的固体混合物溶于水配成100 mL溶液,其中c(Na+)=0.8 mol·L-1。若把等质量的固体混合物加热至恒重,残留固体的质量是( )
A.3.18 gB.2.12 gC.4.24 gD.5.28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列体系中,离子能大量共存的是( )
A.含1.2 mol·L-1 NO3-的溶液:H+、Fe2+、Mg2+、Br-
B.使酚酞变红的溶液:K+、Na+、![]() 、Cl-
、Cl-
C.滴加KSCN显红色的溶液:![]() 、K+、Cl-、I-
、K+、Cl-、I-
D.0.1 mol·L-1 NaHCO3溶液:Na+、Ba2+、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期主族元素,前三种元素在周期表中的位置如图所示:
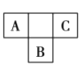
A、B、C三种元素中有两种元素的最高价氧化物对应的水化物是强酸,D元素的原子半径在短周期元素中最大,E是最高正价为![]() 的非金属元素。
的非金属元素。
(1)C在周期表中的位置是______
(2)A、B、C三种元素中两种元素所形成的两种强酸的分子式分别为______;上述五种元素形成的简单离子中,电子层结构相同的离子的半径由大到小的顺序为____________
(3)举例说明C的非金属性比B的非金属性强:____________
(4)D的单质与E所形成的最常见化合物能发生剧烈反应,写出相应的离子方程式:____________;A、E之间形成的最简单化合物(过量)与C的单质混合后可得到一种单质和一种盐,对应的化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有a~g7种短周期主族元素,它们在元素周期表中的相对位置如图所示,请回答下列问题:
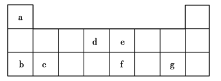
(1)下列选项中,元素的原子间最容易形成离子键的是______(填序号,下同),元素的原子间最容易形成共价键的是______。
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
(2)下列由a~g7种元素原子形成的各种分子中,所有原子最外层都满足8电子稳定结构的是______(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)由题述元素中的3种非金属元素形成的AB型离子化合物的电子式为______。
(4)![]() 与
与![]() 可形成一种化合物
可形成一种化合物![]() ,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。
上述物质有如图转化关系:

下列说法错误的是
A. 四种元素形成的单质中W的氧化性最强
B. 甲、乙、丙中沸点最高的是丙
C. 甲常用作致冷剂
D. 甲、乙分子均只含极性共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com