
【题目】某种元素原子的质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是( )
A. 由已知信息可得NA=![]()
B. W g该原子的物质的量一定是![]() mol
mol
C. 该原子的摩尔质量是aNA g
D. W g该原子中含有![]() 个该原子
个该原子
科目:高中化学 来源: 题型:
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图,下列叙述不正确的是( )

A. 有机物A属于芳香族化合物
B. 有机物A和NaOH的醇溶液共热可发生消去反应
C. 有机物A和浓硫酸混合加热,可以发生消去反应
D. 1molA和足量的NaOH溶液反应,最多可以消耗 3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中的位置如图所示。下列推断正确的是( )

A. 原子半径:Z>Y>X
B. 元素非金属性:Z>Y>X
C. 最高价氧化物对应水化物的酸性:Z>Y>W
D. WH4与Z元素的单质在光照时发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。

(1)步骤1的主要操作是___________。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)__________,固体残渣的成分是(填化学式)________________。
(3)步骤3中涉及的操作是:蒸发浓缩、_____________、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:

请回答下列问题:
(1)Pt(a)电极是电池的________极,电极反应式为__________________;Pt(b)电极发生________(填“氧化”或“还原”)反应,电极反应式为___________。
(2)电池的总反应方程式为____________________。
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应温度 |
A | 0.1mol Mg | 6mol/L硝酸 | 10mL | 30℃ |
B | 0.1mol Mg | 3mol/L盐酸 | 10mL | 60℃ |
C | 0.1mol Fe | 3mol/L盐酸 | 10mL | 60℃ |
D | 0.1mol Mg | 3mol/L盐酸 | 10mL | 30℃ |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知固体Na2SO3受热分解生成两种正盐,实验流程和结果如下:
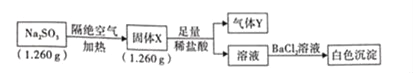
已知:气体Y是一种纯净物,在标准状况下密度为1.518gL﹣1.请回答下列问题:
(1)气体Y的电子式为_____。
(2)实验流程中,Na2SO3受热分解的化学方程式为_____。
(3)另取固体X试样和Na2SO3混合,加适量蒸馏水溶解,再加入稀盐酸,立即有淡黄色沉淀产生。则产生淡黄色沉淀的离子方程式为_____(不考虑空气的影响)。
(4)Na2SO3长期露置在空气中,会被氧化成Na2SO4,检验Na2SO3是否变质的实验操作是_____。
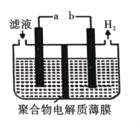
(5)某研究性学习小组通过图所示装置,利用电化学方法处理上述流程中产生的气体Y.基本工艺是将气体Y通入FeCl3,待充分反应后过滤,将所得滤液加入电解槽中进行电解,电解后的滤液可以循环利用。则与a相连的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
温度/℃ | c(NH3·H2O) /(mol·L-1) | 电离常数 | 电离度/% | c(OH-) /(mol·L-1) |
0 | 16.56 | 1.37×10-5 | 9.098 | 1.507×10-2 |
10 | 15.16 | 1.57×10-5 | 10.18 | 1.543×10-2 |
20 | 13.63 | 1.71×10-5 | 11.2 | 1.527×10-2 |
提示:![]()
(1)温度升高,NH3·H2O的电离平衡向________(填“左”或“右”)移动,能支持该结论的表中数据是________(填字母)。
a.电离常数 b.电离度 c.c(OH-) d.c(NH3·H2O)
(2)表中c(OH-)基本不变的原因是__________________________________。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是_______(填字母,下同)。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(4)氨水溶液中,下列做法能使c(NH4+)与c(OH-)比值变大的是________。
A.加入固体氯化铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com