
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示:

现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
硫酸 | 4 mol·L-1 | ρ1 |
2 mol·L-1 | ρ2 | |
氨水 | 4 mol·L-1 | ρ3 |
2 mol·L-1 | ρ4 |
⑴ ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
⑵ 表中2 mol·L-1氨水的质量分数为:________。
⑶ 将4 mol·L-1的氨水与2 mol·L-1的氨水等质量混合,所得氨水的物质的量浓度是_____(填序号)。
A.>3 mol·L-1 B.=3 mol·L-1 C.<3 mol·L-1 D.无法判断
⑷ 将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______(填序号)。
A.>15% B.=15% C.<15% D.无法判断
⑸ 100g浓度为4 mol·L-1的硫酸溶液与_________mL水混合,能使硫酸的物质的量浓度减小到2 mol·L-1。
【答案】 ρ1>ρ2>ρ4>ρ3 (3.4/ρ4) % A A (200ρ2-100ρ1)/ ρ1
【解析】(1)硫酸的密度大于水的密度,氨水的密度小于水的密度,所以ρ1、ρ2>ρ4、ρ3,硫酸的密度大于水的密度,浓度越大,密度越大,ρ1>ρ2,氨水的密度小于水的密度,浓度越大,密度越小,ρ4>ρ3,因此大小顺序为ρ1>ρ2>ρ4>ρ3;(2)表中2molL-1氨水的密度是ρ4,根据公式c=1000ρw/M得出质量分数为:w=3.4/ρ4 %;(3)由图可知,氨水的浓度越大密度越小,将4molL-1的氨水与2molL-1的氨水等质量混合,所得氨水的物质的量浓度要比3molL-1大,答案选A;(4)硫酸的密度大于水的密度,将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数>(20%+10%)/2,即混合后质量分数大于15%,答案选A;(5)100g浓度为4molL-1的硫酸溶液中溶质的物质的量是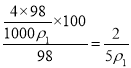 ,设加入水的体积是VmL,能使硫酸的物质的量浓度减小到2molL-1,则
,设加入水的体积是VmL,能使硫酸的物质的量浓度减小到2molL-1,则![]() ,解得V=(200ρ2100ρ1)/ρ1mL。
,解得V=(200ρ2100ρ1)/ρ1mL。


科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料。其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂。A可发生如图所示的一系列化学反应,其中①、②、③属于同种反应类型。请回答下列问题:
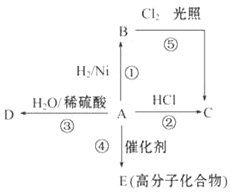
(1)写出A、B、C、D的结构简式:A____________、B___________、C__________、D_________。
(2)写出②、⑤两步反应的化学方程式,并注明反应类型:
② ______________________________________,反应类型:__________________________。
⑤ ______________________________________,反应类型:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,根据上述内容回答下列问题:
①蛋白质在人体内最终的水解产物是_________________。
②属于人体所需微量元素的是____________________。
③属于脂溶性维生素的是_________________。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①硅酸盐产品在生活中使用广泛,下列不是硅酸盐产品的是 _______________。
A、水泥 B、陶瓷 C、玻璃 D、塑料
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为______。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①pH<_________________的雨水称为酸雨;向煤中加入适量的__________________,可以大大减少燃物产物中SO2的量。
②天然水中杂质较多,常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2的作用是
__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验或实验操作和现象,所得结论正确的是
实验或实验操作 | 现象 | 实验结论 | |
A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
C |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
D |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的核磁共振氢谱中出现三组峰的是
A. 2,2,3,3一四甲基丁烷 B. 2,3,4一三甲基戊烷
C. 3,4一二甲基己烷 D. 2,5一二甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.
(1)用CH4催化还原煤燃烧产生的氮氧化物,可以消除污染.
已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol
NO2(g)═![]() N2O4(g) △H=-28.5kJ/mol
N2O4(g) △H=-28.5kJ/mol
写出CH4催化还原N2O4(g)生成CO2、N2和H2O(g)的热化学方程式_____________。
(2)一定条件下,将2mol NO2与4molSO2置于恒温体积为2L的恒容密闭容器中,发生:NO2(g)+SO2(g)═SO3(g)+NO(g),10s时反应达到平衡,测得平衡时c(NO2)=0.25mol/L,则10s内反应的平均速率v(SO2)=____________;达到平衡时NO2转化率=____________;计算该温度下该反应的化学平衡常数K= _____________(填数值)。
(3)将CO2与NH3混合,在一定条件下反应合成尿素,可以保护环境、变废为宝,反应原理为:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H
CO(NH2)2(s)+H2O(g) △H
该反应在一定条件下能自发进行的原因是____________;若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是_____________(填序号)。
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
C.2v(NH3)正=v(H2O)逆 d.容器中混合气体的密度不再改变
(4)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。有人利用如图所示装置(均为惰性电极)从海水中提取CO2(海水中无机碳95%以HCO3-存在),有利于减少环境中温室气体含量。

①a室的电极反应式为___________________。
②b室中提取CO2的反应的离子方程式为 ___________________。
③b室排出的海水(pH <6)不可直接排回大海,需用该装置中产生的物质对b室排出的海水进行处理,合格后才能排回大海。处理的方法是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y均为有刺激性气味的气体,且几种物质间有以下转化关系,部分产物未标出。请回答下列问题。

(1)写出下列各物质的化学式:X 、Y 、C 。
(2)反应①的化学方程式为 ,反应②的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.08mol·L-1。则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.08mol·L-1。则下列判断正确的是
A. c1:c2=3:1 B. 平衡时,Y和Z的生成速率之比为2:3
C. X、Y的转化率不相等 D. C1的取值范围为01<0.14mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com