
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示,由图中数据分析:

(1)该反应的化学方程式 。
(2)反应开始至2min,以Z表示的平均反应速率为 。
(3)反应达平衡此时体系的压强是开始时 倍。
(4)下列叙述能说明上述反应达到化学平衡状态的是 (填字母)
A.混合气体的总物质的量不随时间的变化而变化
B.单位时间内每消耗3mol X,同时生成2mol Z
C.混合气体的密度不随时间的变化而变化
【答案】(1)3X+Y![]() 2Z(不写可逆符号不给分);(2)0.05 mol·L-1·min-1;(3)0.9倍;(4)A。
2Z(不写可逆符号不给分);(2)0.05 mol·L-1·min-1;(3)0.9倍;(4)A。
【解析】
试题分析:(1)X、Y物质的量随反应进行减少,因此属于反应物,Z应是生成物,根据化学反应速率之比等于化学计量数之比,同时间同体积,化学计量数之比等于物质的量变化之比,即(1-0.7):(1-0.9):0.2=3:1:2,化学反应方程式3X+Y![]() 2Z;(2)根据化学反应速率的表达式,v(Z)=0.2/(2×2)mol/(L ·min)=0.05 mol/(L ·min);(3)压强之比等于物质的量之比,反应前的总物质的量为(1+1)mol=2mol,反应后的总物质的量为(0.9+0.7+0.2)mol=1.8mol,两者物质的量之比为2:1.8=1:0.9;(4)A、反应前后气体系数之和不相等,总物质的量随时间的变化而变化,当总物质的量不再改变,说明反应达到平衡,故正确;B、反应方向都是向正反应方向进行,不能作为达到化学平衡的标志,故错误;C、ρ=m/V,恒容状态,体积不变,组分都是气体,气体质量不变,因此密度不能作为达到平衡的标志,故错误。
2Z;(2)根据化学反应速率的表达式,v(Z)=0.2/(2×2)mol/(L ·min)=0.05 mol/(L ·min);(3)压强之比等于物质的量之比,反应前的总物质的量为(1+1)mol=2mol,反应后的总物质的量为(0.9+0.7+0.2)mol=1.8mol,两者物质的量之比为2:1.8=1:0.9;(4)A、反应前后气体系数之和不相等,总物质的量随时间的变化而变化,当总物质的量不再改变,说明反应达到平衡,故正确;B、反应方向都是向正反应方向进行,不能作为达到化学平衡的标志,故错误;C、ρ=m/V,恒容状态,体积不变,组分都是气体,气体质量不变,因此密度不能作为达到平衡的标志,故错误。


科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10﹣2,K2=5.4×10﹣5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解为CO、CO2和H2O。回答下列问题:

(1)写出草酸晶体分解的化学方程式_________________________________。
(2)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。若实验过程中,B中澄清石灰水变浑浊,______(填“能”或“不能”)说明草酸晶体的分解产物中有CO2,原因是______。
(3)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A和如图所示的部分装置(可以重复选用)进行实验。

①乙组同学的实验装置中,依次连接的合理顺序为A →___→____→G→ →____。装置H反应管中盛有的物质是 。
②F装置的作用是___________________________________。
③能证明草酸晶体分解产物中有CO的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
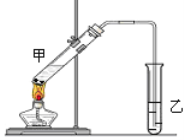
(1)若反应的乙醇中O为18O,用同位素示踪法写出制取乙酸乙酯的化学反应方程式:
。
(2)浓硫酸的作用是:① ;② 。
(3)该装置中有一个明显的错误是 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)某同学将收集到的乙酸乙酯滴入饱和NaHCO3溶液中,观察到有少量气泡产生,可得出的结论是 ,该过程中发生反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是位于短周期的主族元素。已知:①热稳定性:HmD>HmC; ②Cm+、E(m+1)+具有相同的电子层结构;③A与B在同一周期,在该元素所有主族中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子的3倍。
依据上述信息用相应的化学用语回答下列问题:
(1)B元素在周期表的位置_____________;
(2)HmDm的电子式______________;
(3)Cm-的结构示意图______________;
(4)AmDm的化学键类型_________;
(5)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为_________;
(6)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行化学实验时应强化安全意识。下列做法正确的是( )
A. 金属钠着火时使用泡沫灭火器灭火
B. 用试管加热碳酸氢钠固体时使试管口竖直向上
C. 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液沖洗
D. 做蒸馏实验时,如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL{![]() }及阻燃剂四溴双酚A。合成线路如下:
}及阻燃剂四溴双酚A。合成线路如下:

已知:① X的蒸汽密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;C为![]()
![]()
![]()
(1)X的分子式为_______________;B的名称是_________________。
(2)B→C还需要的反应试剂及条件是____________。C→D的反应类型是_______。
(3)写出X→Y的化学方程式:_________________________________。
(4)0.5mol四溴双酚A在一定条件下与足量的NaOH溶液反应,最多消耗_________molNaOH。
(5)符合以下条件的D的同分异构体有_________种(不考虑空间异构)。
①含有两个甲基和两种官能团②能使溴的CCl4溶液褪色③能发生银镜反应
(6)已知由烯烃直接制备不饱和酯的新方法为:
![]()
利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料![]() ,写出合成该涂料的反应流程图:______________________________________________。
,写出合成该涂料的反应流程图:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为《化学与生活(选修1)》选做题。
(1)资源必须要合理使用。
①水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是______(填字母代号)
A.科学合理使用农药
B.任意排放化工厂废水
C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃.根据垃圾分类方法,矿泉水瓶属于_____________(填“可回收物”或“可堆肥垃圾”);
③在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向大气的排放,减小环境污染。在催化转化器中,CO和NO发生反应.请完成该反应的化学主程式_____________。
(2)保护环境、爱护地球已成为人们的共同呼声。
①我们常在公共场所见到下列标志,其中属于回收标志的是__________

②2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是____________。
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO尼古丁和都属于室内空气污染物
(3)化学与生活关系密切。现有下列四种物质:
A.蛋白质 B.亚硝酸盐 C.维生素C D.油脂
①__________是重要的体内能源;
②__________广泛存在于新鲜水果和绿色蔬菜中,有酸性和还原性,又称为抗坏血酸;
(4)材料是人类赖以生存和发展的重要物质基础
①试管、烧杯和烧瓶等化学仪器的主要材质是__________;
A.玻璃 B.陶瓷 C.水泥
②“辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料。生铁和钢成分上的主要差别是_________;
A.碳的含量不同
B.磷、硫的含量不同
C.镍、铬等金属含量不同
③钢铁在潮湿空气中易发生吸氧腐蚀,负极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钠-过氧化氢加合物(xNa2SO4yH2O2zH2O)的组成可通过下列实验测定:
①准确称取1.7700g 样品,配制成100.00mL 溶液A.
②准确量取25.00mL 溶液A,加入盐酸酸化的BaCl2 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825g.
③准确量取25.00mL 溶液A,加适量稀硫酸酸化后,用0.02000molL-1KMnO4 溶液滴定至终点,消耗KMnO4 溶液25.00mL.H2O2 与KMnO4 反应的离子方程式如下:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
(1)步骤②中滴定终点的现象为____________;
(2)步骤②中使用盐酸酸化,而步骤③中改用硫酸酸化的原因是____________;
(3)上述滴定若不加稀硫酸酸化,MnO4-被还原为MnO2,其离子方程式为____________;
(4)通过计算确定样品的组成(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com