
【题目】利用如图装置模拟铁的电化学保护。下列说法正确的是
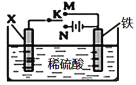
A.若X为锌棒,开关K置于M处,为外加电流阴极保护法
B.若X为碳棒,开关K置于N处,为牺牲阳极阴极保护法
C.若X为锌棒,开关K置于M处,Zn极发生:Zn-2e→Zn2+
D.若X为碳棒,开关K置于N处,X极发生还原反应
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)写出表示含有6个质子、8个中子的原子的化学符号:________,该同位素原子在科学研究中有着重要的用途,该用途是_____________
(2)原子序数为113的元素在元素周期表中的位置________。
(3)在![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中有_______种核素
中有_______种核素
(4)在自然界中许多元素有多种核素,如氧元素存在![]() 、
、![]() 、
、![]() 三种核素,氢元素有
三种核素,氢元素有![]() 、
、 ![]() 、
、![]() 三种核素。
三种核素。
①![]() 、
、![]() 、
、![]() 、
、![]() 四种核数最多可以组成______种水分子
四种核数最多可以组成______种水分子
②请画出![]() 微粒的结构示意图:__________________。
微粒的结构示意图:__________________。
③现有11g由![]() 和
和![]() 组成的水分子,其中含中子数为_____mol,电子数为______个。
组成的水分子,其中含中子数为_____mol,电子数为______个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g)该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如表所示。
H2O(g)+CO(g)该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如表所示。
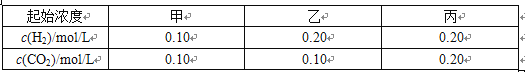
其中甲经2min达平衡时,v(H2O)为0.025mol/(L·min),下列判断错误的是
A.平衡时,乙中CO2的转化率等于50%
B.当反应平衡时,丙中c(CO2)是甲中的2倍
C.温度升至800℃,上述反应平衡常数为![]() ,则正反应为吸热反应
,则正反应为吸热反应
D.其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20mol/L CO2,到达平衡时c(CO)与乙不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当电池工作时,下列说法错误的
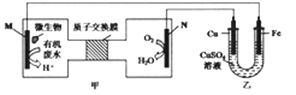
A. 甲池中N极的电极反应式为:O2+4e-+4H+=2H2O
B. 当N极消耗5.6L(标准状况下)O2时,铁极增重32g
C. 电子的流动方向为M→Fe→CuSO4溶液→Cu→N
D. M极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)在化学合成上用作还原剂及催化剂。工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾。
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为________(保留两位小数),50%的硫酸与30%的硫酸等体积混合,混合酸的浓度为_______(填>、<、=)40%。
(2)将111.2g绿矾(FeSO47H2O,式量为278)在高温下加热,充分反应后生成Fe2O3固体和SO2、SO3、水的混合气体,则生成Fe2O3的质量为_______g;SO2为_______mol。实验室可用以下方法制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O,式量为392]。
(3)将4.88g铁屑(含Fe2O3)与25mL 3mol/L H2SO4充分反应后,得到FeSO4和H2SO4的混合溶液,稀释溶液至100mL,测得其pH=1。铁屑中Fe2O3的质量分数是________(保留两位小数)。
(4)向上述100mL溶液中加入与该溶液中FeSO4等物质的量的(NH4)2SO4晶体,待晶体完全溶解后蒸发掉部分水,冷却至t℃,析出摩尔盐晶体12.360g,剩余溶液的质量为82.560g。t℃时,计算(NH4)2SO4·FeSO4·6H2O的溶解度。_______(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如下图所示。下列有关该有机物说法正确的是
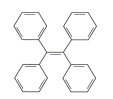
A. 分子式为C26H22 B. 属于苯的同系物
C. 一氯代物有3种 D. 能溶于水和酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】YBa2Cu3Ox(Y为元素钇)是一种重要超导材料,下列关于![]() 的说法错误的是( )
的说法错误的是( )
A.质量数是89B.质子数与中子数之差为50
C.核外电子数是39D.与![]() 互为同位素
互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请写出下列各题中的离子方程式或化学方程式
(1)碳酸钠与硝酸反应的离子方程式:_________。
(2)二氧化硅与氢氧化钠反应的离子方程式:_____________。
(3)写出工业制硅所涉及的化学方程式:a.__________b.__________c.____________。
(4)写出氢氧化镁与盐酸反应的离子方程式:____________。
(5)请写出一个离子方程式证明溴的氧化性大于碘:_________。
(6)写出一个化学方程式其离子反应为CO32-+2H+=CO2+H2O:______。
(7)写出一种酸在常温下能与硅反应的化学方程式:_______________。
(8)写出用HF雕刻玻璃的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是
A.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9NA
B.56g铁在足量氧气中完全燃烧,转移的电子数小于3NA
C.16g O2和14C2H4的混合物中所含中子数为8NA
D.常温下,1 L 0.5 mol/L CH3COONH4溶液的pH=7,则溶液中CH3COO-与NH4+的数目均为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com