
【题目】某学习小组按如下流程探究碘的制取,甲乙两种制取方案如下:
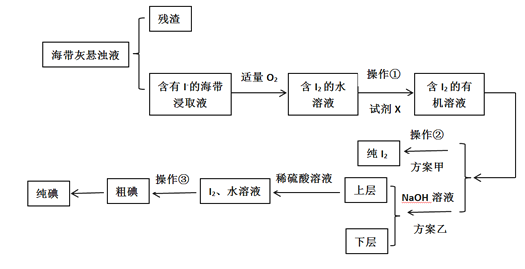
已知:3I2+6OH-=5I-+IO3-+3H2O;5I-+IO3-+6H+=3I2 +3H2O;酸性条件下,I2在水溶液中的溶解度极小。
(1)灼烧海带时,除需要三脚架,泥三角外,还需要用到的实验仪器为___。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①___;②___;③___。
(3)有机试剂X可以是___(填序号)
A.四氯化碳 B.乙醇 C.醋酸
(4)下列关于加入NaOH溶液操作的说法,正确的是___。
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除浸取原液中的杂质 D.NaOH溶液可由乙醇代替
(5)方案甲中采用操作②会导致碘的损失,原因是___。
【答案】CD 萃取分液 蒸馏 过滤 A AB 碘易升华
【解析】
(1)根据蒸干灼烧的操作所需仪器回答;
(2)实验室从海带中提取碘:海带灼烧成灰,浸泡溶解得到海带灰悬浊液,通过过滤,得到不溶的残渣,滤液为含碘离子的溶液,加入酸和氧化剂O2,将碘离子氧化成碘单质,利用有机溶剂苯萃取出碘单质,方案甲是通过蒸馏提取出碘单质,方案乙则是通过碘单质与氢氧化钠反应生成I-与IO3-,两种离子进一步反应生成碘单质的过程,分液后加入稀硫酸,降低碘单质在水中的溶解度,经过过滤制得粗碘,据此分析作答。
(1)灼烧海带时,除需要三脚架,泥三角外,还需要用到的实验仪器坩埚和酒精灯,CD项符合题意,故答案为:CD;
(2)根据上述分析可知,提取碘的过程中有关的实验操作名称分别是①为萃取分液;②为蒸馏;③由于碘单质在酸性溶液的溶解度很小,碘在水溶液中以晶体析出,该操作名称为过滤,故答案为:萃取分液;蒸馏;过滤;
(3)有机试剂X作为萃取剂,必须与水互不相溶,A项符合题意,乙醇与醋酸与水互溶,不符合题意,BC项错误,故答案为:A;
(4)据题中所给信息:3I2+6NaOH=5NaI+NaIO3+3H2O,方案乙的目的在于把碘元素全部由CCl4层转移入水层,NaOH溶液应过量,为了下一步便于提取碘,所加氢氧化钠溶液的体积不能过多,故其浓度不能太小,故选项A、B正确,选项C错误,由于I2在CCl4和乙醇中都易溶解,且CCl4和乙醇互溶,乙醇不能从I2的CCl4溶液中萃取I2,选项D错误;答案选AB;
(5)由于碘易升华,加热碘的四氯化碳溶液时,碘易挥发,会导致碘的损失,故不采用蒸馏方法,故答案为:碘易升华。


科目:高中化学 来源: 题型:
【题目】H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l)△H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法正确的是( )
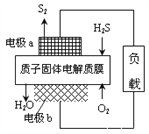
A. 电池在工作时,电流从电极a经过负载流向电极b
B. 电极a上发生的电极反应为: 2H2S - 4e- = S2 + 4 H+
C. 当反应生成64gS2时,电池内部释放632kJ热量
D. 当电路中通过4mol电子时,有4mol H+经质子膜进入负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)147gH2SO4的物质的量是_______;
(2)氧化铜在高温下发生分解反应:4CuO![]() 2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为________mol。
2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为________mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____元素化合价升高,则该元素被_____,_____元素化合价降低;______作还原剂,_____发生还原反应。
(4)钠在空气中燃烧的化学方程式:_____,1mol钠完全燃烧转移电子的个数为______(阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移
B. 100 mL 1 mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
D. 84gNaHCO3固体含有CO32-离子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶澄清的溶液,其中可能含有H+,Mg2+,Na+,Ba2+,Fe3+,Cl﹣,CO32﹣,SO42﹣等离子,取该溶液进行以下实验
a.用PH试纸检验,表明溶液呈强酸性。
b.取部分溶液逐渐滴加入NaOH溶液,使溶液从酸性逐渐变成碱性,整个滴加过程中,溶液均无沉淀生成。
c.取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成。
(1)根据上述事实确定:该溶液中肯定存在的离子有____________;肯定不存在的离子有____________;可能存在的离子有____________。
(2)写出以下反应的离子方程式:
①氧化镁溶于盐酸____________。
②碳酸氢钠溶液与氢氧化钠溶液混合____________。
③氢氧化钡与稀硫酸混合____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铜的提炼多从黄铜矿开始,黄铜矿在焙烧过程中主要反应之一的化学方程式为![]()
![]() 。下列说法正确的是( )
。下列说法正确的是( )
A. 每生成![]() ,有4mol硫被氧化
,有4mol硫被氧化
B. ![]() 只作还原剂,
只作还原剂,![]() 只作氧化剂
只作氧化剂
C. ![]() 既是氧化产物又是还原产物
既是氧化产物又是还原产物
D. 若有![]() 参加反应,则上述反应中共有
参加反应,则上述反应中共有![]() 转移
转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是( )
A. 由Na和Cl形成离子键的过程:![]()
B. NH5的结构与NH4Cl相似,NH5的结构式: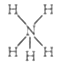
C. 中子数为20的氯原子:![]()
D. 乙烯的分子式:CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分类是学习化学的一种重要方法,科学合理的分类对于提高学习效率、解决问题都有着重要的意义。请回答下列问题:
I. 纯净物根据其组成和性质有如图分类形式

图中所示所属的分类方法为__________________。
II. 有以下13种物质①石墨 ②过氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钠溶液 ⑧纯醋酸 ⑨氯化氢 ⑩硫酸铝 稀硫酸 氯化银 硫酸氢钠
(1)属于电解质的是 _________;属于非电解质的是 _________。
(2)写出下列物质溶于水的电离方程式:⑥__________________;⑩___________________;
(3)写出物质⑥和⑦反应的离子方程式:___________________。
(4)写出物质⑥和在水中发生反应的离子方程式:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com