
【题目】过氧乙酸(CH3COOOH)可用作纺织品漂白剂。过氧乙酸可通过下列方法制备: 向烧瓶中依次加入乙酸、42.5%过氧化氢溶液、浓硫酸。控制反应温度为25 ℃,搅拌4小时,静置15小时,得过氧乙酸溶液。
(1)制备20g38%过氧乙酸溶液至少需要42.5%过氧化氢溶液质量为________g。
(2)过氧乙酸含量测定。准确称取0.4900g过氧乙酸样液,定容于100 mL容量瓶中。取5.00 mL上述溶液于100 mL碘量瓶中,再加入5mL 2 mol·L-11H2SO4,用0.01 mol·L-1KMnO4溶液除去过氧乙酸样品中剩余H2O2,随即加入过量KI溶液,摇匀,用0.01 mol·L-1 Na2S2O3标准液滴定至终点,消耗Na2S2O3的体积为25.00 mL。
已知有关反应的方程式:CH3COOOH+2I-+2H+===I2+CH3COOH+H2O;2S2O32-+I2===2I-+S4O62-。
①加入过量KI溶液前,需KMnO4溶液除去H2O2的化学方程式为:______________________________。
②计算过氧乙酸样液中过氧乙酸的质量分数(给出计算过程并保留小数点后一位)__________。
③用该法测定过氧乙酸含量比实际含量偏高的原因是(不考虑实验操作产生的误差_______________。
【答案】 8 g 2KMnO4+5H2O2+3H2SO4==2MnSO4+K2SO4+5O2↑+8H2O 38.8% I-会被溶液中残留的氧气或空气中氧气氧化为I2等原因
【解析】(1)制备20g38%过氧乙酸溶液至少需要42.5%过氧化氢溶液质量为x,
H2O2+CH3COOH![]() CH3COOOH+H2O
CH3COOOH+H2O
34 76
x×42.5% 20g×38%
![]() =
=![]() ,解得x=8g;
,解得x=8g;
(2)①加入过量KI溶液前,需除去H2O2的原因是过氧化氢也会氧化碘离子,会干扰测定结果,反应的离子方程式为:2I-+H2O2+H+=I2+2H2O;②n(S2O32-)=0.01000mol/L×0.02500L=2.5×10-4mol,CH3COOOH+2I-+2H+═I2+CH3COOH+H2O,2S2O32-+I2═2I-+S4O62-
得关系式为CH3COOOH~I2~2S2O32-,n(CH3COOOH)=![]() n(S2O32-)=
n(S2O32-)=![]() ×2.5×10-4mol=1.25×10-4mol,w%=
×2.5×10-4mol=1.25×10-4mol,w%=![]() ×
×![]() ×100%=38.8%;③取5.00mL上述溶液与100mL碘量瓶中,再加入5.0mL2molL-1H2SO4溶液,用0.01molL-1KMnO4溶液滴定至溶液出现浅红色(以除去过氧乙酸试样中剩余H2O2),过量的高锰酸钾溶液会氧化碘离子生成碘单质导致过氧乙酸含量偏高,或空气中氧气也可以氧化碘离子为碘单质,也可以导致测定结果偏高。
×100%=38.8%;③取5.00mL上述溶液与100mL碘量瓶中,再加入5.0mL2molL-1H2SO4溶液,用0.01molL-1KMnO4溶液滴定至溶液出现浅红色(以除去过氧乙酸试样中剩余H2O2),过量的高锰酸钾溶液会氧化碘离子生成碘单质导致过氧乙酸含量偏高,或空气中氧气也可以氧化碘离子为碘单质,也可以导致测定结果偏高。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图1表示同温度下,pH = 1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且b点溶液的导电性比a点强
B. 图2表示0.1000 mol/L CH3COOH溶液滴定20.00mL0.1000mol/LNaOH溶液所得到的滴定曲线
C. 图3表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D. 据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入2.5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60Ml
B.240mL
C.30mL
D.120mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如下: 
请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8g CO2和3.6g H2O;E的蒸气对氢气的相对密度为30,则E的分子式为 .
(2)A为一取代芳烃,B中含有一个甲基.由B生成C的化学方程式为 .
(3)由B生成D、由C生成D的反应条件分别是、 .
(4)由A生成B、由D生成G的反应类型分别是、 .
(5)F存在于栀子香油中,其结构简式为 .
(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有种,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是(填结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁轨道焊接常用到铝热反应,某学习小组进行铝热反应实验,装置如图所示。
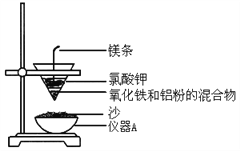
(1)仪器 A 的名称为_______。
(2)写出工业上制取金属镁的化学方程式______。
(3)点燃镁条引发反应,在反应过程中没有涉及到的化学反应类型是_______。
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
(4)写出该铝热反应的化学方程式,并用单线桥表示电子转移的方向和数目_______。
(5)铝热反应中放出大量的热,有黑色熔融物落入沙中。学习小组推测黑色熔融物中除了含有铁和氧化铝,还含有铝和氧化铁,实验验证如下:
Ⅰ. 向冷却后的黑色固体中加入 NaOH 溶液,观察到有气体产生。实验结论:黑色固体中含有铝。写出该反应的离子方程式:________。
Ⅱ. 取少量黑色固体于试管中,加入稀盐酸,固体溶解,有气泡产生。向所得溶液中滴入几滴 0.01 mol·L- 1 KSCN 溶液,溶液不变色。实验结论:黑色固体中不含氧化铁。
你认为实验结论是否合理?____(填“合理”或“不合理”)。理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硅酸的反应为Na2SiO3+2HCl═2NaCl+H2SiO3↓,该反应属于( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修3:物质结构与性质]我国具有悠久的历史,在西汉就有湿法炼铜(Fe+CuSO4=Cu+FeSO4),试回答下列问题。
(1)Cu2+的未成对电子数有______个,H、O、S电负性由大到小的顺序为_______。
(2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。
①[Cu(NH3)4]SO4中化学键类型有_______,[Cu(NH3)4]2+的结构简式为_______,阴离子中心原子杂化类型为______。
②氨的沸点远高于膦(PH3),原因是______________。
(3)铁铜合金晶体类型为_____;铁的第三(I3)和第四(I4)电离能分别为2957kJ/mol、5290kJ/mol,比较数据并分析原因________________。
(4)金铜合金的一种晶体结构为立方晶型,如图所示。

①该合金的化学式为____;
②已知该合金的密度为dg/cm3,阿伏加德罗常数值为NA,两个金原子间最小间隙为apm(1pm=10-10cm)。则铜原子的半径为_______cm(写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。

下列说法正确的是
A. M点所示溶液c(NH4+)+c(NH3·H2O)= c(Cl-)
B. N点所示溶液中:c(NH4+)>c(Cl-)
C. Q点所示消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的离子积相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com