
【题目】某校化学兴趣小组对SO2的性质和回收利用等问题进行探究,对环境保护具有重要意义。SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。
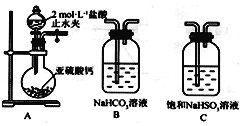
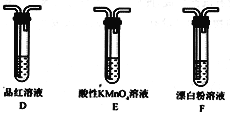
(1)装置A中盛放亚硫酸钙的仪器名称是_________________,其中发生反应的化学方程式为_____________________________________________________;
(2)装置正确的连接顺序为A→____→ → → D → F ,其中装置B的作用是_________。证明亚硫酸的酸性强于次氯酸的现象为________________________________________。
【答案】圆底烧瓶CaSO3+2HCl=CaCl2+SO2↑+H2OC B E制取CO2D中品红溶液不褪色,F中出现白色沉淀
【解析】
(1)装置A中盛放亚硫酸钙的仪器为圆底烧瓶,发生反应的化学方程式为 CaSO3+2HCl=CaCl2+SO2↑+H2O。(2) 次氯酸具有强氧化性,二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸和次氯酸的酸性强弱,应先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比次氯酸酸性强弱进行判断。装置A制备二氧化硫,由于盐酸有挥发性,制备的二氧化硫中含有氯化氢,用饱和的亚硫酸氢钠除去氯化氢,再通过碳酸氢钠溶液,可以验证亚硫酸的酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中 的二氧化硫,用品红溶液检验二氧化碳中的二氧化硫是否除尽,再通入F中。所以仪器的连接顺序为:A、C、B、E、D、F。装置B是用二氧化硫和碳酸氢钠反应制取CO2 。二氧化硫和碳酸氢钠反应生成二氧化碳,二氧化碳和次氯酸钙反应生成碳酸钙白色沉淀,D中品红溶液不褪色,F中出现白色沉淀,证明了碳酸反应生成次氯酸,证明碳酸酸性比次氯酸酸性强,进而证明亚硫酸的酸性比次氯酸的酸性强。


科目:高中化学 来源: 题型:
【题目】通常情况下,苯的化学性质比较稳定,这是因为 ( )
A.苯不能使高锰酸钾酸性溶液褪色B.苯不与溴水发生加成反应
C.苯的分子结构决定的D.苯是芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用下图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是
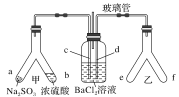
A. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
B. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
C. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
D. e、f两管中的试剂可以分别是浓氨水和NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。常温下0.1mol·L-1 NaHC2O4溶液(pH约为4)中指定微粒的物质的量浓度关系错误的是
A. c(Na+)= c(HC2O![]() )+c(C2O
)+c(C2O![]() )+c(H2C2O4)
)+c(H2C2O4)
B. c(HC2O4-)>c(H2C2O4)>c(C2O![]() )
)
C. c(Na+)+c(H+)=c(HC2O![]() )+ c(C2O
)+ c(C2O![]() )+c(OH-)
)+c(OH-)
D. c(H2C2O4)+c(H+)=c(C2O![]() )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )

A. 6:1 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.72g金属钠、氧化钠和过氧化钠的混合物与足量水反应,在标准状况下得到672mL混合气体,将混合气体电火花点燃,恰好完全反应,则原混合物中钠、氧化钠、过氧化钠的物质的量之比为( )
A. 3:2:1 B. 4:2:1 C. 2:1:1 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是_______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
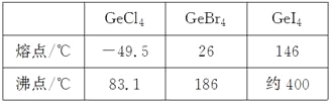
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为____________,微粒之间存在的作用力是________________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为________。

②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为________g·cm-3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com