
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:

请根据以上信息回答下列问题:
Ⅰ.(1)写出N的化学式和B的名称:N________,B________。
(2)写出反应②的化学方程式,并标出其电子转移的方向和数目________________。
(3)写出反应③的离子方程式____________________________________。
Ⅱ.粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液④碳酸钠溶液,以上试剂添加的顺序可以为________。
A.②③④① B.③④②①
C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及的反应类型是________。
A.分解反应 B.化合反应
C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是_____。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有________性。
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?________(填“甲”或“乙”),理由是_________________。
【答案】HCl氢氧化钙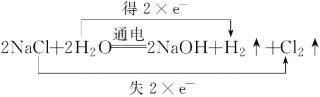 Cl2+2OH-=Cl-+ClO-+H2OADCCD挥发乙若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2(其他合理解释也可)
Cl2+2OH-=Cl-+ClO-+H2OADCCD挥发乙若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2(其他合理解释也可)
【解析】
根据流程图知:反应②为精盐溶液的电解,反应物是氯化钠和水,产物是氯气、氢气、氢氧化钠,C+F→N,N能溶解沉淀,C既能和F反应又能和E反应,所以E为NaOH,F为H2,C为Cl2,N为HCl,贝壳(主要成分为CaCO3)经过高温煅烧可以生成疏松的A为氧化钙,氧化钙可与水反应生成B为氢氧化钙,与母液反应生成氢氧化镁沉淀,氢氧化镁与盐酸反应生成氯化镁,电解熔融的氯化镁可生成氯气和镁,由转化关系可知D为Mg,以此解答该题。
根据以上分析为可知A为氧化钙,B为氢氧化钙,C为Cl2,D为Mg,E为NaOH,F为H2,则
Ⅰ.(1)根据以上分析为可知N的化学式为HCl,B的名称为氢氧化钙;
(2)惰性电极电解食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时生成氢氧化钠,生成1mol氢气转移2mol电子,则电子转移的方向和数目可表示为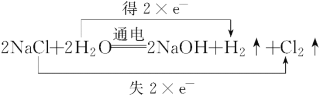 ;
;
(3)反应③是氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;
Ⅱ.Ca2+、Mg2+、SO42-等分别与Na2CO3溶液、NaOH溶液、BaCl2溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液还能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,试剂添加的顺序可以为②③④①或③②④①,答案选AD;
Ⅲ.(1)母液和B反应为海水中的镁离子和氢氧化钙反应生成氢氧化镁沉淀,为复分解反应,制取氯化氢为化合反应,氢氧化镁和盐酸反应得到氯化镁,为复分解反应,氯化镁电解为分解反应,该过程中未涉及的反应为置换反应,答案选C;
(2)提取Br2,反应⑥所用的气态氧化剂为氯气,本厂生产烧碱为电解氯化钠溶液,产物中有氯气,本厂生产镁单质,是电解无水氯化镁,电解氯化镁的产物为镁和氯气,故答案为CD;液溴易挥发,因此流程⑦将溴单质从混合物中分离出来是基于溴单质具有挥发性;
(3)母液用来提取Mg和Br2,若先提取镁,海水中会残留大量Ca(OH)2,Ca(OH)2能和氯气反应生成氯化钙、次氯酸钙和水,再用Cl2提取溴时会消耗大量Cl2,所以乙观点合理。


科目:高中化学 来源: 题型:
【题目】①pH=2的CH3COOH溶液;②pH=2的H2SO4溶液;③pH=12的氨水;④pH=12的NaOH溶液。室温条件下,有关上述溶液的比较中,正确的是( )
A. 水电离的c(H+):①=②=③=④
B. 将②、④溶液混合后,pH=7,消耗溶液的体积:②<④
C. 等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D. 向10 mL上述四溶液中各加入90 mL水后,溶液的pH:③>④>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中常用到化学知识,下列说法不正确的是( )
A. 白色污染、绿色食品中的“白”、“绿”均指相关物质的颜色
B. 用食醋可以除去热水壶中的水垢
C. 聚氯乙烯塑料有毒,不可用于制食品包装袋
D. 新制的Cu(OH)2可以检测糖尿病患者尿液中是否含有葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂(易被氧化),某研究性学习小组为了制备少量Na2S2O5,并探究SO2的某些性质,设计下图所示装置(夹持装置已略去)。请回答下列问题:
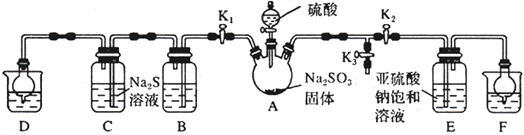
(1)向A中滴加的硫酸最好选用__________________(填字母)。
A.98%的浓硫酸 B.70%的硫酸 C.10%的稀硫酸
(2)打开分液漏斗旋塞,发现其中的液体不能流下,应采取的操作是__________________________。
(3)关闭K1、K3,打开K2。一段时间后E中有Na2S2O5晶体析出,装置E中发生反应的化学方程式为__________________________。
(4)关闭K2、K3,打开K1,若探究SO2的漂白性,装置B应盛有__________溶液;若探究SO2的还原性,B中发生反应的离子方程式可以是_____________________________________;观察到装置C 中发生的现象是__________________________。
(5)装置D和F 的作用为__________________________。
(6)设计实验验证Na2S2O5晶体在空气中已被氧化:__________________________。
(7)请指出该设计的缺陷:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列三个化学反应均能发生:
X2+2W2+![]() 2X-+2W3+
2X-+2W3+
Z2+2X-![]() 2Z-+X2
2Z-+X2
2W3++2Y-![]() 2W2++Y2
2W2++Y2
则在相同条件下,下列三个反应也能发生的是( )
①Y2+2X-![]() 2Y-+X2 ②Z2+2Y-
2Y-+X2 ②Z2+2Y-![]() 2Z-+Y2 ③2W3++2Z-
2Z-+Y2 ③2W3++2Z-![]() 2W2++Z2
2W2++Z2
A. 只有① B. 只有② C. ①和② D. ②和③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如右图所示,其中A、B为多孔材料.下列说法正确的是
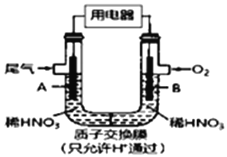
A. 该电池工作时,电子的流向:外电路由B到A
B. 电极B 附近的HNO3浓度增大
C. A电极的反应为:NO2-e-+H2O=NO3-+2H+,NO-3e-+2H2O= NO3-+4H+
D. 该电池工作时,除去含1molNO和NO2的混合尾气,需消耗11.2LO2(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硝酸厂尾气中较高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,流程如下:
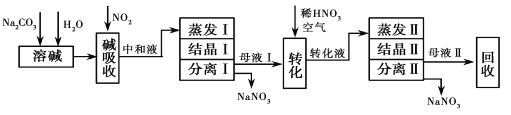
已知:NaOH+NO+NO2═2NaNO2+H2O
(1)写出Na2CO3溶液和NO、NO2反应的化学方程式_______________________________。
(2)中和液所含溶质除NaNO2及少量Na2CO3 外,还有少量___________和___________(填化学式)。
(3)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是____________________;蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的______________(填操作名称)最合理。
(4)母液Ⅱ需 回收利用,下列处理方法合理的是________________________。
a.转入中和液 b.转入结晶Ⅰ操作 c.转入转化液 d.转入结晶Ⅱ操作
(5)NaNO2能与N2H4反应生成NaN3,该反应中NaNO2_____(填“被氧化”或“被还原”)
N2H4 的电子式是____________________,NaN3 中含有的化学键类型是______________________。
(6)若将NaNO2、NaNO3两种产品的物质的量之比设为2∶1,则生产1.38吨NaNO2时,Na2CO3的理论用量为________________吨(假定Na2CO3恰好完全反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯和乙烷的说法中错误的是
A.乙烯是不饱和烃,乙烷是饱和烃
B.乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,乙烷则不能
C.乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键键能的两倍,因此乙烯比乙烷稳定
D.乙烯分子为平面结构,乙烷分子为立体结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com