
【题目】秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
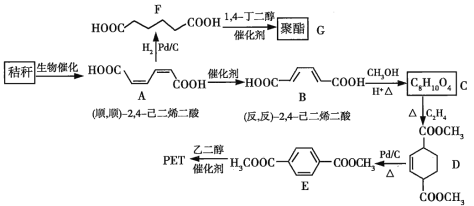
回答下列问题:
(1)下列关于糖类的说法正确的是_________。(填标号)
a 糖类都有甜味,具有![]() 的通式 b 麦芽糖水解生成互为同分异构体的葡萄糖和果糖
的通式 b 麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c 用银镜反应不能判断淀粉水解是否完全 d 淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为___________。
(3)D中的官能团名称为_________,D生成E的反应类型为_________。
(4)F的化学名称是________。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,![]() 与足量碳酸氢钠溶液反应生成
与足量碳酸氢钠溶液反应生成![]() ,W共有_____种(不含立体异构),其中核磁共振氢谱为三组峰的结构简式为______。
,W共有_____种(不含立体异构),其中核磁共振氢谱为三组峰的结构简式为______。
(6)参照上述合成路线,以(反,反)![]() ,
,![]() 已二烯和
已二烯和![]() 为原料(无机试剂任选),设计制备对苯二甲酸的合成路线______。
为原料(无机试剂任选),设计制备对苯二甲酸的合成路线______。
【答案】cd 取代反应(酯化反应) 酯基、碳碳双键 消去反应 己二酸 12 ![]()
【解析】
结合B、D可知B到C为酯化反应,那么C为![]() ,F到G位缩聚反应生成聚酯G,则G为:
,F到G位缩聚反应生成聚酯G,则G为:![]() 。
。
(1)a.糖类不一定具有甜味,如纤维素,不一定符合碳水化合物通式,如脱氧核糖(C5H10O4)就不符合通式,a错误;
b.麦芽糖水解生成葡萄糖,而蔗糖水解生成葡萄糖和果糖,b错误;
c.用碘水检验淀粉是否完全水解,用银氨溶液可以检验淀粉是否水解,c正确;
d.淀粉、纤维素都是多糖类天然高分子化合物,d正确;
故答案为cd;
(2)![]() 发生酯化反应,酯化反应也属于取代反应,故答案为:取代反应(酯化反应);
发生酯化反应,酯化反应也属于取代反应,故答案为:取代反应(酯化反应);
(3)D中官能团名称是酯基、碳碳双键,D生成E,增加两个碳碳双键,说明发生消去反应,故答案为:酯基、碳碳双键;消去反应;
(4)F为二元羧酸,名称为己二酸或1,![]() 己二酸,故答案为:己二酸;
己二酸,故答案为:己二酸;
(5)W具有一种官能团,不是一个官能团,W是二取代芳香化合物,则苯环上有两个取代基,![]() 与足量碳酸氢钠反应生成
与足量碳酸氢钠反应生成![]() ,说明W分子中含有2个羧基。则侧链组合有4种情况:①
,说明W分子中含有2个羧基。则侧链组合有4种情况:①![]() ,
,![]() ;②
;②![]() ,
,![]() ;③
;③![]() ,
,![]() ;④
;④![]() ,
,![]() 。每组取代基在苯环上有邻、间、对三种位置关系,所以W共有12种结构。在核磁共振氢谱上只有三组峰,说明分子是对称结构,结构简式为
。每组取代基在苯环上有邻、间、对三种位置关系,所以W共有12种结构。在核磁共振氢谱上只有三组峰,说明分子是对称结构,结构简式为![]() ,故答案为:12;
,故答案为:12;![]() ;
;
(6)流程图中有两个新信息反应原理:一是C与乙烯反应生成D,是生成六元环的反应;二是![]() ,环烯结构在
,环烯结构在![]() 、加热条件下脱去2分子
、加热条件下脱去2分子![]() 变成苯环,结合这两个反应原理可得出合成路线为:
变成苯环,结合这两个反应原理可得出合成路线为: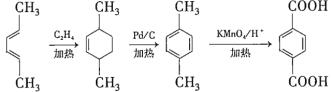 ,故答案为:
,故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】现有淀粉和蛋白质(含苯基)胶体的混合液,要检验其中蛋白质的存在,可取混合液少许,向其中加入![]() _________,加热至沸,溶液呈现明显的__________色,说明有蛋白质存在。要检验其中淀粉的存在,可取混合液少许,加入___________,溶液呈现明显的_________色,说明有淀粉存在。要把蛋白质和淀粉分离开,可进行的操作是___________。
_________,加热至沸,溶液呈现明显的__________色,说明有蛋白质存在。要检验其中淀粉的存在,可取混合液少许,加入___________,溶液呈现明显的_________色,说明有淀粉存在。要把蛋白质和淀粉分离开,可进行的操作是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国对‘可呼吸”的钠-二氧化碳电池的研究取得突破性进展。该电池的总反应式为:4Na+3CO2 ![]() 2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
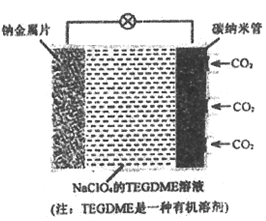
A. 放电时,钠金属片作负极,碳纳米管作正极
B. 充电时,阳极反应为:2Na2CO3+C-4e-=3CO2↑+4Na+
C. 放电时,Na+从负极区向正极区移动
D. 该电池的电解质溶液也可使用NaClO4的水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)卤族元素组成的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识它们。
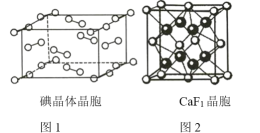
①如图1为碘晶体的晶胞结构。有关说法正确的是_________(填序号)。
a.平均每个晶胞中有4个碘分子
b.平均每个晶胞中有4个碘原子
c.碘晶体为无限延伸的空间结构,是原子晶体
d.碘晶体中存在的相互作用有非极性键和范德华力
②已知CaF2晶胞(图2)的密度为ρ g/cm3,NA表示阿伏加德罗常数的值,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量可表示为_________________。
(2)以MgCl2为原料用电解熔融盐法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外,还有_______________。
(3)有研究表明,化合物X可用于研究模拟酶,当结合 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:

①A中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有_________键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖发酵可制得乳酸,从酸牛奶中也能提取出乳酸,纯净的乳酸为无色黏稠液体,易溶于水。为了研究乳酸的分子组成和结构,进行如下实验:
(1)称取乳酸![]() ,在某种状况下使其完全汽化,若相同状况下等体积氢气的质量为
,在某种状况下使其完全汽化,若相同状况下等体积氢气的质量为![]() ,则乳酸的相对分子质量为_______。
,则乳酸的相对分子质量为_______。
(2)若将上述乳酸蒸气在![]() 中燃烧只生成
中燃烧只生成![]() 和
和![]() ,当气体全部被碱石灰吸收后,碱石灰的质量增加
,当气体全部被碱石灰吸收后,碱石灰的质量增加![]() ;若将此气体通过足量的石灰水,产生
;若将此气体通过足量的石灰水,产生![]() 白色沉淀。则乳酸的分子式为________。
白色沉淀。则乳酸的分子式为________。
(3)乳酸分子能发生自身酯化反应,且其催化氧化产物不能发生银镜反应。若葡萄糖发酵只生成乳酸,试写出该反应的化学方程式:_______(忽略反应条件)。
(4)写出乳酸在催化剂作用下发生反应生成分子式为![]() 的环状酯的结构简式:__。
的环状酯的结构简式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅铬黄是一种颜料,主要成分是铬酸铅PbCrO4。现以CrCl36H2O 和 Pb(NO 3)2等为原料制备该物质,并测定产物纯度。
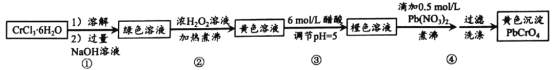
(1)溶解、过滤、洗涤操作时, 均需要用到的以下仪器为______________(填标号)。

(2)第①步所得绿色溶液的主要成分为 NaCrO2,已知 Cr(OH)3 不溶于水,与Al(OH)3类似,具有两性。写①步发生反应的离子方程式_____________________。
(3)第②步中加入H2O2 浓溶液的目的是___________________。溶液逐步变为亮黄色后,仍须持续煮沸溶液一段时间,目的是_____________________。
(4)第③步加入醋酸的目的是,防止pH 较高时,加入 Pb(NO3)2 溶液会产生______(填化学式)沉淀,影响产率。利用pH 试纸,调节 pH 的实验操作是_____________。pH逐步降低时, 溶液中的CrO42-转化为 ____________离子(填化学式)。
(5)由于铬酸铅的溶解度比重铬酸铅的小的多,在第④ 步中逐滴滴加 Pb(NO3)2溶液后,产PbCrO4黄色沉淀, 此时为了提高铅铬黄的产率,可补加少量NaOH溶液,请用化学平衡移动原理加以解释:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结 论 |
A | 含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
B | 用铂丝蘸取少量NaCl溶液进行焰色反应,火焰呈黄色 | 这是钠离子的发射光谱 |
C | NaI溶液 | 酸性条件下H2O2的氧化性比I2强 |
D | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
A. 25% B. 50% C. 75% D. 80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验证明,在![]() 溶液中慢慢加入浓的NaOH溶液,开始有蓝色沉淀产生,但是当加入的浓NaOH溶液过量后,沉淀溶解变成深蓝色溶液,某学生对此作出了推断。下列推断正确的是( )
溶液中慢慢加入浓的NaOH溶液,开始有蓝色沉淀产生,但是当加入的浓NaOH溶液过量后,沉淀溶解变成深蓝色溶液,某学生对此作出了推断。下列推断正确的是( )
A.形成了![]() 配离子
配离子
B.![]() 溶液的颜色被冲淡
溶液的颜色被冲淡
C.形成了![]() 配离子
配离子
D.![]() 存在溶解平衡
存在溶解平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com