
【题目】锌与100 mL 18.5 mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液中氢离子浓度为0.1 mol·L-1。下列叙述不正确的是( )
A.反应中共消耗1.8 mol 硫酸B.气体甲中二氧化硫与氢气的体积比为4∶1
C.反应中共消耗97.5 g 锌D.反应中共转移3 mol电子
【答案】B
【解析】
Zn和浓硫酸先反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,随着反应的进行硫酸浓度降低,发生Zn+H2SO4=ZnSO4+H2↑,然后在具体分析;
A. Zn和浓硫酸先反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,随着反应的进行硫酸浓度降低,发生Zn+H2SO4=ZnSO4+H2↑,反应后溶液稀释至1L,测的溶液中c(H+)=0.1mol·L-1,说明硫酸过量,剩余硫酸的物质的量为 ![]() ×1L×0.1mol·L-1=0.05mol,总硫酸物质的量为100×10-3L×18.5mol·L-1=1.85mol,即反应过程中消耗硫酸的物质的量为(1.85mol-0.05mol)=1.8mol,故A说法正确;
×1L×0.1mol·L-1=0.05mol,总硫酸物质的量为100×10-3L×18.5mol·L-1=1.85mol,即反应过程中消耗硫酸的物质的量为(1.85mol-0.05mol)=1.8mol,故A说法正确;
B. 令生成amolSO2和bmolH2,则有:![]()
![]() 得到2a+b=1.8mol,反应后得到气体物质的量为(a+b)mol=
得到2a+b=1.8mol,反应后得到气体物质的量为(a+b)mol=![]() ,联立解得a=0.3,b=1.2,即相同条件下,气体体积之比等于物质的量之比,SO2和H2的体积之比为0.3:1.2=1:4,故B说法错误;
,联立解得a=0.3,b=1.2,即相同条件下,气体体积之比等于物质的量之比,SO2和H2的体积之比为0.3:1.2=1:4,故B说法错误;
C. 根据选项A的分析,反应后溶液中的溶质为H2SO4和ZnSO4,根据硫酸守恒得出n(H2SO4)+n(ZnSO4)+n(SO2)=n(H2SO4)总,得出n(ZnSO4)=(1.85mol-0.05mol-0.3mol)=1.5mol,消耗Zn的质量为1.5mol×65g·mol-1=97.5g,故C说法正确;
D. 整个反应中Zn失电子,反应中转移电子物质的量为1.5mol×2=3mol,故D说法正确;
故答案为:B。


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
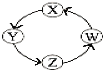
【题目】X、Y、Z、W四种物质间的转化关系如图所示 ,下列转化不能一步实现的是( )
序号 | X | Y | Z | W |
A | N2 | NH3 | NO | NO2 |
B | Na | NaOH | Na2CO3 | NaCl |
C | Cl2 | Ca(OH)2 | HClO | HCl |
D | H2S | S | SO3 | H2SO4 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中进行化学反应CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示

请回答下列问题:
(1)该反应的正反应为______(填“吸热”或“放热”)反应,
(2)某温度下,在2L的密闭容器中,加入 1molCO2和 1mol H2,充分反应达平衡时,CO的平衡浓度为0.25mol/L,试判断此时的反应温度为________
(3)若在(2)所处的温度下,在1L的密闭容器中,加入2moCO2和3 mol H2,则充分反应达平衡时,H2的物质的量______
A.等于1.0mol B.大于1.0mol
C.大于0.5mol,小于1.0mol D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应式:mX(g)+nY(?)![]() pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的
pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的![]() ,c(X)=0.5mol/L,下列说法正确的是( )
,c(X)=0.5mol/L,下列说法正确的是( )
A.反应向逆方向移动B.Y可能是固体或液体
C.系数n>mD.Z的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将几滴KSCN(SCN-是“类似卤离子”)溶液加入到酸性的含有Fe3+的溶液中,溶液变为红色,将该红色溶液分为两份:①向其中—份溶液中加入适量KMnO4溶液,红色褪去;②向另一份溶液中通入SO2,红色也褪去。下列说法中不正确的是
A. ①中红色褪去的原因是KMnO4将SCN-氧化,使Fe(SCN)3消失
B. ②中红色褪色的原因是SO2将Fe3+还原为Fe2+
C. ②中红色裡色的原因是SO2将SCN-还原
D. SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两溶液间的反应,不能用同一离子方程式来表示的是( )
A.Na2CO3+HCl;K2CO3+HNO3
B.Fe+HCl;Fe+H2SO4
C.BaCl2+Na2SO4;Ba(OH)2+H2SO4
D.NaOH+H2SO4;Ba(OH)2+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是

A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,一定体积的的密闭容器中有如下平衡:H2(g)+I2(g)![]() 2HI(g)。已知H2和I2的起始浓度均为0.10mol·L-1,达到平衡时HI的浓度为0.16mol·L-1。若H2和I2的起始浓度均变为0.20 mol·L-1,则平衡时H2的浓度(mol·L-1)是( )
2HI(g)。已知H2和I2的起始浓度均为0.10mol·L-1,达到平衡时HI的浓度为0.16mol·L-1。若H2和I2的起始浓度均变为0.20 mol·L-1,则平衡时H2的浓度(mol·L-1)是( )
A.0.16B.0.08C.0.04D.0.02
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com