
【题目】下列各组中的离子在强酸性水溶液里能大量共存的是
A. Ba2+、Na+、CO32-、NO3- B. K+、 CH3COO-、I-、Fe3+
C. Cu2+、Fe2+、SO42-、Cl- D. K+、Cl-、NO3-、HCO3-
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】![]() (R、R′、R″是各种烃基)如上式烯烃的氧化反应,双键被高锰酸钾酸性溶液氧化而断裂,在断键两端的碳原子都被氧化成为羧基或酮羰基.由氧化所得的产物,可以推测反应物烯烃的结构.今有A、B、C三个含有双键的化合物,它们被上述溶液氧化: 1molA(分子式C8H16),氧化得到2mol酮D.
(R、R′、R″是各种烃基)如上式烯烃的氧化反应,双键被高锰酸钾酸性溶液氧化而断裂,在断键两端的碳原子都被氧化成为羧基或酮羰基.由氧化所得的产物,可以推测反应物烯烃的结构.今有A、B、C三个含有双键的化合物,它们被上述溶液氧化: 1molA(分子式C8H16),氧化得到2mol酮D.
1molB(分子式C8H14),氧化得到2mol酮E和1mol二元羧酸.
1molC(分子式C8H14),氧化只得到一种产物,它是一种没有支链的二元羧酸.
请据此推断B、C、D、E的结构简式为:B、C、D、E .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在图所示的物质转化关系中(反应条件和部分生成物未全部列出),X物质是海水中含量最多的盐,A、B为常见气体单质,B为淡黄绿色气体,I、L为常见的金属单质,H为红褐色物质,Y为常见的无色液体.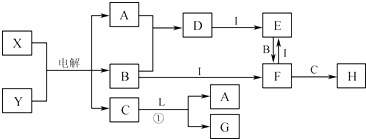
请回答下列问题:
(1)H的化学式为 .
(2)C的电子式为 .
(3)反应①的化学方程式为 .
(4)E转化为F的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用足量CO还原14g铁的氧化物或铁的氧化物的混和物,将生成的CO2通入澄清的石灰水中, 得到25g沉淀,则该物质不可能是
A. FeO、Fe2O3 B. Fe2O3、Fe3O4 C. FeO、Fe3O4 D. Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.17g氨气所含电子数目为10NA
B.32g氧气所含原子数目为NA
C.在25℃,压强为1.01×105Pa时,11.2L氮气所含的原子数目为NA
D.32g氧气与44g二氧化碳的体积一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液(1)汽油和氯化钠溶液;(2)酒精和水的混合溶液;(3)氯化钠和单质溴的溶液;以上混合溶液分离的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计可如图所示的探究原电池的装置.下列有关说法正确的是( )
A.电极材料必须是金属材料
B.若a极为铜条、b极为锌片,c为蔗糖溶液时,灯泡会发亮
C.若a极为铝条、b极为铜片,c为浓硝酸溶液时,铜为负极
D.若a极为铝条、b极为镁片,c为稀硫酸溶液时,铝为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原2.4×10﹣3mol [XO(OH)]2+ 到X元素的低价态时,需消耗30mL 0.2mol·L﹣1的亚硫酸钠(Na2SO3)溶液,则在此反应中X元素的低价态为( )
A. 0价 B. +1价 C. ﹣1价 D. ﹣2价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列原电池对应的电极反应式正确的是( )
A.硫酸铅蓄电池的负极:Pb﹣2e﹣═Pb2+
B.锌银纽扣电池的正极:Ag2O+2e﹣+H2O═2AgOH
C.碱性锌锰电池的负极:Zn﹣2e﹣+2OH﹣═Zn(OH)2
D.氢氧碱性燃料电池的正极:2H2O+4e﹣═O2+4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com