
【题目】(1)49 g H2SO4的物质的量是________;1.5 mol H2SO4的质量是________,其中含有_______mol SO42-,______mol H,含有______g O。
(2)用14.2 g无水硫酸钠配制成500 mL溶液,其物质的量浓度为________mol/L。
(3)若从中取出50 mL,其物质的量浓度为_______ mol/L;溶质的质量为________ g。
【答案】0.5mol 147g 1.5 3 96 0.2 0.2 1.42
【解析】
(1)结合m=nM、N=nNA及分子构成计算;
(2)根据n=![]() 和c=
和c=![]() 来计算;
来计算;
(3)溶液是均一稳定的,取出一部分溶液后,溶液的浓度不变,根据n=cV和m=nM来计算。
(1)49 g H2SO4的物质的量是![]() =0.5mol;1.5 mol H2SO4的质量是1.5mol×98g/mol=147g,其中含有1.5 mol SO42-,含氢原子的物质的量是1.5mol×2=3mol,含有氧原子质量是1.5mol×4×16g/mol=96g;
=0.5mol;1.5 mol H2SO4的质量是1.5mol×98g/mol=147g,其中含有1.5 mol SO42-,含氢原子的物质的量是1.5mol×2=3mol,含有氧原子质量是1.5mol×4×16g/mol=96g;
(2)14.2g无水硫酸钠的物质的量n=![]() =
=![]() =0.1mol,溶液的浓度c=
=0.1mol,溶液的浓度c=![]() =
=![]() =0.2mol/L;
=0.2mol/L;
(2)溶液是均一稳定的,取出一部分溶液后,溶液的浓度不变,故取出50 mL,其物质的量浓度为0.2 mol/L;物质的量n=cV=0.2mol/L×0.05L=0.01mol,溶质的质量m=nM=0.01mol×142g/mol=1.42g。


科目:高中化学 来源: 题型:
【题目】标准状况下,有①6.72LCH4,②3.01×1023个HCl,③13.6gH2S ,④0.2molNH3,则下列四种气体的关系表示正确的是()
A. 体积:④<①<②<③ B. 密度:①<③<④<②
C. 质量:④<①<③<② D. 氢原子数:②<③<④<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TMB由碳氢氮三种元素组成,其相对分子质量为240,是一种新型指纹检测的色原试剂,已在逐步取代强致癌物联苯胺和其他致癌性的联苯胺衍生物应用于临床化验法医检验刑事侦破及环境监测等领域。某研究小组欲利用燃烧法测定TMB的分子式(氮元素转化为N2)实验装置如图所示。回答下列问题:
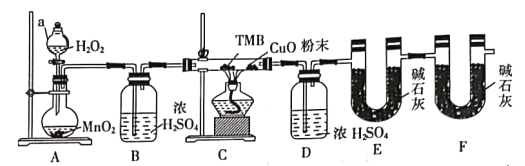
(1)实验装置两处用到装有碱石灰的干燥管,其中F处的目的是______________________。仪器a的名称是___________。
(2)将足量双氧水置于a中,圆底烧瓶中装入MnO2固体,按图连接好装置。
①A中发生反应的化学方程式为______________________。
②待B、D处导管口有均匀气泡时,再点燃C处酒精灯,原因是______________________。
(3)装置C中CuO粉末的作用为_________________________________。
(4)该实验___________(填“需要”或“不需要”)尾气处理,其原因是____________________。
(5)理想状态下,将4.80gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60g,E增加14.08g,则TMB的分子式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的叙述正确的是

A. 向KI溶液中加入淀粉,然后滴入少量稀硫酸,开始无明显现象,片刻后溶液变蓝,则证明氧化性:H2SO4>I2
B. 图甲用于除去乙烯中的SO2
C. 用图乙装置蒸干明矾溶液制KAl(SO4)2·12H2O晶体
D. 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaCN溶液中CN-水解常数![]() 是NaCN溶液的起始浓度]。25℃时,向c0的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[pOH-=-lg c(OH-)]的关系如图。
是NaCN溶液的起始浓度]。25℃时,向c0的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[pOH-=-lg c(OH-)]的关系如图。

下列说法不正确的是
A. 其它条件不变,降低温度,可使b点变到a点
B. 相同温度时,c点对应溶液中的pH大于a点
C. 由图可知,25 ℃时,Kh(CN-)≈10-4.7
D. 向1 L lgc0=0的NaCN溶液中通入0.5 mol HCl气体,所得溶液中c(CN-)<c(HCN)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2==4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,单位都为mol/(Ls),则正确的关系是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.现用物质的量浓度为0.100 0 mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
(1)从下表中选出正确选项______________


(2)某学生的操作步骤如下:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴部分充满溶液;
D.取标准NaOH溶液注入碱式滴定管至“0”刻度以上 2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是____→___→___→___→A→___(用字母序号填写)______________。判断到达滴定终点的实验现象是_____________________________________。
(3)若滴定达终点时,滴定管中的液面如上图所示,正确的读数为__________
A.22.30 mL B.23.65 mL
C.22.35 mL D.23.70 mL
(4)由于错误操作,使得上述所测盐酸溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.酸式滴定管用蒸馏水洗净后立即取用25.00 mL待测酸溶液注入锥形瓶进行滴定
C.碱式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.用酸式滴定管量取待测盐酸时,取液前有气泡,取液后无气泡
(5)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 20.00 | 1.02 | 21.03 |
2 | 20.00 | 2.00 | 21.99 |
3 | 20.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品的浓度是________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在科研和生产中具有广泛用途。回答下列问题:
(l)基态Cu原子的价电子排布图是____。
(2)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是____。
(3)铜晶体中Cu原子的堆积方式如图所示,其堆积方式为____,配位数为____.

(4)NH3中N原子的杂化方式是____;C、N、O元素的第一电离能由大到小的顺序是____(用元素符号表示);SO42-的空间构型是____,与该阴离子互为等电子体的五核微粒有____ (任写1种)。
(5)由铜、钡、钙及铊的氧化物可以制得高温超导体,CaO的熔点比BaO的熔点高,其原因是____。

(6)金铜合金的晶胞如图所示。金铜合金具有储氢功能,储氢后Au原子位于顶点,Cu原子位于面心,H原子填充在由1个Au原子和距Au原子最近的3个Cu原子构成的四面体空隙中,若Cu原子与Au原子的最短距离为a nm,阿伏加德罗常数的值为NA,则该晶体储氢后密度为___________g.cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸(部分反应条件、产物已省略)。
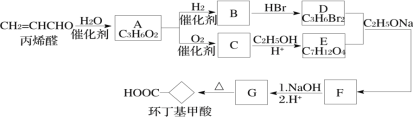
已知:
(1)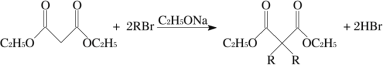
(2)![]()
请回答下列问题:
(1)由丙烯醛生成化合物A的反应类型为____________。
(2)化合物C的结构简式是________________________。
(3)下列说法中正确的是___________(填字母代号)。
A.丙烯醛可以发生银镜反应 B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4 D.1mol化合物B与足量金属钠反应能生成1mol氢气
(4)写出D+E→F的化学方程式:__________________________________________。
(5)符合下列条件的G的同分异构体有____________种,写出其中在1H-NMR谱上显示两组峰且面积比为3∶1的结构简式:______________________。
①能使Br2/CCl4溶液褪色;②1mol G与1mol Na2CO3反应可以生成1mol CO2
(6)以1,3-丁二烯和化合物E为原料可制备![]() ,请选用必要的试剂设计合成路线____________________。
,请选用必要的试剂设计合成路线____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com