
【题目】研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
I.现有反应:①CaCO3=CaO+CO2↑,②Fe +H2SO4=FeSO4+ H2↑。
(1)两反应中属于吸热反应的是____(填序号)。
(2)Fe-Cu 原电池的装置如图所示。
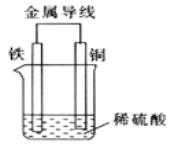
①溶液中H+向______(填“铁”或“铜” )电极方向移动。
②正极的现象是_______,负极的电极反应式为_________。
II.某可逆反应:2A(g)![]() B(g)+D(g)在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:
B(g)+D(g)在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:
 (3)实验1中,在10~20 min内,以物质A表示的平均反应速率为_______mol/(L·min) ,50min时,v(正)______(填“<”“>”或“=”)v(逆)。
(3)实验1中,在10~20 min内,以物质A表示的平均反应速率为_______mol/(L·min) ,50min时,v(正)______(填“<”“>”或“=”)v(逆)。
(4)0~20min内,实验2 比实验1的反应速率______ (填“快”或“慢”),其原因可能是_______。
(5)实验3 比实验1的反应速率快,其原因是_________。
【答案】 ① 铜 有气泡产生 Fe-2e-=Fe2+ 0.013 = 快 实验2中使用了催化剂 实验3中反应温度更高
【解析】(1)碳酸钙分解是吸热反应,铁与稀硫酸发生的置换反应是放热反应;(2)①铁的金属性强于铜,铁负极,铜是正极,正极发生得到电子的还原反应,因此溶液中H+向正极即向铜电极方向移动。②正极上氢离子得到电子生成氢气,则正极的现象是有气泡产生,负极发生铁失去电子的氧化反应,电极反应式为Fe-2e-=Fe2+。(3)实验1中,在10~20min内,A物质的浓度减少了0.80mol/L-0.67mol/L=0.13mol/L,则以物质A表示的平均反应速率为0.13mol/L÷10min=0.013mol/(L·min),50min时反应物浓度不再发生变化,反应达到平衡状态,则v(正)=v(逆)。(4)根据表中数据可知0~20min内,实验2中A的浓度变化量大于实验1中A的浓度变化量,因此实验2中的反应速率快,由于最终平衡时A的浓度仍然相等,即没有改变平衡状态,所以其原因可能是实验2中使用了催化剂。(5)由于实验3中反应温度更高,所以实验3比实验1的反应速率快。


科目:高中化学 来源: 题型:
【题目】N、O、Si、S、Al、Fe、Cu是常见的七种元素.
(1)Si位于元素周期表第周期第族.
(2)Cu原子的价层电子排布图为 .
(3)基态Fe原子有个未成对电子,Fe3+的电子排布式为 . 可用硫氰化钾检验Fe3+ , 形成的配合物的颜色为 .
(4)用“>”或“<”填空:
离子半径 | 电负性 | 熔点 | 酸性 |
O2﹣ Na+ | FO | 金刚石 晶体硅 | H2SO4HClO4 |
(5)氢元素和上述非元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为;分子中既含有极性共价键、又含有非极性共价键的化合物是(填化学式,任写一种).
(6)O和Cu形成的一种离子化合物的晶体结构如图,则铜离子的电荷为 . 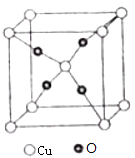
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图1琐事,物质A与物质B之间的反应不再溶液中进行. 
(1)若A为金属单质,C是淡黄色固体,D是一元强碱. ①物质B是(填化学式).
②化合物C的电子式为;化合物D中所含化学键的类型是 .
③在常温下,向pH=a的醋酸溶液中加入等体积pH=b的D溶液,且a+b=14,则充分反应后,所得溶液中各种离子的浓度由大到小的顺序是: .
(2)若A为非金属单质,C是有色气体,D是一元强酸. ①B为(填化学式).
②化合物C与H2O反应化学方程式 , 氧化剂与还原剂的质量比为 .
(3)某同学用图2装置完成有关探究实验. Ⅰ试管中发生反应的离子方程式为 .
Ⅱ试管中观察到的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在污水治理越来越引起人们重视,可以通过 ![]() 膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法正确的是.
膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法正确的是. 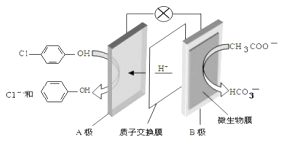
A.电流方向从B极沿导线经小灯泡流向A极
B.A极的电极反应式为 ![]() +e﹣═Cl﹣+
+e﹣═Cl﹣+ ![]()
C.当外电路中有0.2mole﹣转移时,通过质子交换膜的H+的个数为0.1NA
D.B极为电池的正极,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的记录不正确的是
A.纯净的氢气在氯气中安静的燃烧,发出苍白色火焰
B.红热的铜丝在氯气中燃烧,产生绿色的烟
C.红热的铁丝在氯气中燃烧,产生棕褐色的烟
D.将氯气通入硝酸银溶液中,生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A.自然界中的硫都是以化合态存在的
B.硫既具有氧化性,又具有还原性
C.硫化氢气体具有可燃性
D.附着在试管内壁的硫,可以用CS2洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.分散质颗粒直径都在l~100nm 之间 B.能透过半透膜
C.加入浓氢氧化钠溶液都产生红褐色沉淀 D.颜色都呈红褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置.实验时,先断开K2 , 闭合K1 , 两极均有气泡产生;一段时间后,断开K1 , 闭合K2 , 发现电流表指针偏转,下列有关描述正确的是( ) 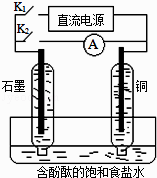
A.断开K2 , 闭合K1时,总反应的离子方程式为:2H++2Cl﹣ ![]() Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2 , 闭合K1时,石墨电极附近溶液变红
C.断开K1 , 闭合K2时,铜电极上的电极反应为:Cl2+2e﹣=2Cl﹣
D.断开K1 , 闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 . ①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15min,用H2表示的平均反应速率为 , 达到平衡时CO的转化率为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com