
【题目】有机物Z是一种天然除草剂,可由X、Y在一定条件下反应制得。下列说法正确的是( )
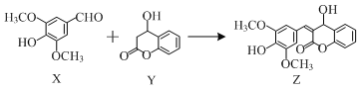
A.有机物X最多可与3molH2发生加成反应
B.可用FeCl3溶液鉴别X和Y
C.Y在Cu作催化剂条件下可被氧化为含醛基的物质
D.X与Y只通过加成反应即可生成Z
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
【题目】有机化合物G可用来制备抗凝血药,可通过下列路线合成。
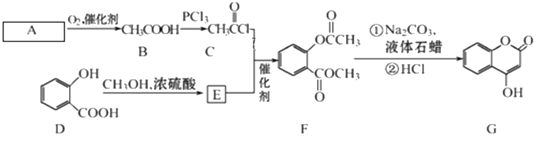
请回答:
(1)A 的结构简式______________________,在A→B的反应中,检验A是否反应完全的试剂为______________________。
(2)C+E→F的反应类型是______________________,F中含有的官能团名称为______________________。
(3)写出G和过量![]() 溶液共热时反应的化学方程式
溶液共热时反应的化学方程式
__________________________________________________________________。
(4)化合物E的同分异构体很多,符合下列条件的结构共有____________种,①含苯环;②苯环上有两个取代基;③能与醇发生酯化反应;④不含-OCO-结构。
(5)已知酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)____________________________________________________________。
)是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或化学用语表达正确的是![]()
A.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
B.p能级的原子轨道呈哑铃形,随着能层的增加,p能级原子轨道也在增多
C.某原子的电子排布式为![]() 属于激发态
属于激发态
D.![]() 的电子排布式为
的电子排布式为![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】薄荷油中含有少量的α非兰烃和β非兰烃,两者互为同分异构体,其相对分子质量为136。根据如下转化,回答相关问题:
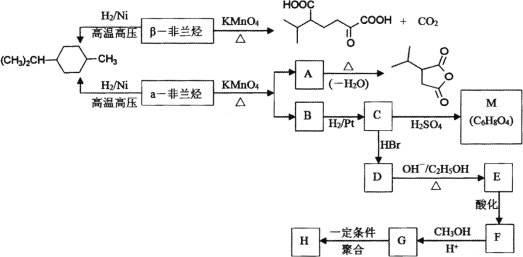
已知:
![]()
![]()
![]() +RCHO
+RCHO
![]()
![]()
![]() +CO2
+CO2
2CH3COOH![]()
![]()
(1) 写出α非兰烃中官能团名称________,β非兰烃的结构简式________。
(2) 下列有关说法正确的是________。
A.α非兰烃与等物质的量的Br2进行加成反应,产物共有3种
B.C→D和E→F反应类型相同
C.聚合物H易溶于水
D.C→M反应过程中有高分子聚合物等副产物产生
(3) 写出F→G的化学方程式________。
(4) 写出符合下列条件的A的同分异构体________。
①含有4个-CH3;②1 mol此同分异构体在碱性条件下水解需2 mol NaOH。
(5) 以甲苯和丙烯为基本原料合成![]() (用流程图表示,其他无机试剂任选)________。
(用流程图表示,其他无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验探究小组进行如下实验,探究化学反应中的能量变化。
实验① | 实验② |
|
|
温度计读数升高 | 温度计读数降低 |
下列判断一定正确的是( )
A.实验①的反应中化学键断裂吸收的能量大于实验②
B.实验①的反应中化学键断裂吸收的能量小于实验②的反应中化学键形成放出的能量
C.实验①说明中和反应放出热量
D.实验②说明所有有氨气生成的反应均吸收热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 用石墨电极电解MgCl2溶液:Mg2++2C1-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑
Mg(OH)2↓+Cl2↑+H2↑
B. 向明矾溶液中滴加碳酸钠溶液:2Al3++3CO32-==Al2(CO3)3↓
C. 向Ca(HCO3)2溶液中滴加少最NaOH溶液:Ca2++2HCO3-+2OH-==CaCO3↓+CO32-+2H2O
D. 向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-==3I2+2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
A.该条件下此反应的化学平衡常数约为0.91(L/mol)3
B.A的平均反应速率为0.3mol/(L![]() s)
s)
C.B的转化率为60%
D.若混合气体的密度不再改变时,该反应不一定达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、R五种元素均位于周期表的前四周期,且原子序数依次增大。元素X的基态原子中电子占据了三种能量不同的原子轨道,且成对电子数是未成对电子数的2倍;元素Y与W同主族,且Y是地壳中含量最多的元素;Z基态原子有12种不同运动状态的电子;元素R基态原子最外层只有1个电子且内层电子全充满。
请回答下列问题:(答题时,X、Y、Z、W、R用所对应的元素符号表示)
(1)基态Y原子的轨道式表示式为![]() ___。
___。
(2)元素Y、W均可形成含18个电子的氢化物,其中Y的氢化物沸点较高,原因是___;
(3)元素Z与同周期相邻两元素第一电离能由高到低的顺序为___。
(4)元素R在周期表中位于___区,R分别与Y、W形成离子化合物R2Y和R2W,其中熔点较高的为___。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)4]2+,在配离子中与R2+形成配位键的原子是___。
(6)X的一种单质(相邻原子间通过共价键形成空间网状结构)、XY2、WY2、ZW对应的晶体熔沸点由高到低的顺序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监测测定水中溶解氧的方法是:①量取25.00mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗VmL。有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O、I2+2S2O32-=2I-+S4O62-
滴定次数 | 待测液的体积/mL | 0.1000mol·L-1 Na2S2O3的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
试回答:
(1)消耗Na2S2O3的体积平均值为___mL,水中溶解氧的量是(以g/L为单位,保留3位有效数字)___。
(2)滴定(I2和S2O32-反应)以淀粉溶液为指示剂,终点时现象为___。
(3)判断下列操作引起的误差(填“偏大”、“偏小” “无影响”或“无法判断”)
①读数:滴定前平视,滴定后俯视___。
②未用标准液润洗滴定管___。
③配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质___。
④待测液的滴定管之前有气泡,取液后无气泡___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com