
【题目】某实验探究小组进行如下实验,探究化学反应中的能量变化。
实验① | 实验② |
|
|
温度计读数升高 | 温度计读数降低 |
下列判断一定正确的是( )
A.实验①的反应中化学键断裂吸收的能量大于实验②
B.实验①的反应中化学键断裂吸收的能量小于实验②的反应中化学键形成放出的能量
C.实验①说明中和反应放出热量
D.实验②说明所有有氨气生成的反应均吸收热量
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,乙烯产品占石化产品的75%以上,在国民经济中占有重要的地位。有如下两个实验都能用来制备乙烯请根据要求回答问题。
Ⅰ.已知使用活性较低的林德拉催化剂[Pd/(PdO、CaCO3)],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化成烷烃。现有一课外活动兴趣小组拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.02mol CaC2的电石和1.600g含杂质18.75 %的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,测得G中收集到的水VmL(收集到的气体已经转化为标准状况下的体积)。
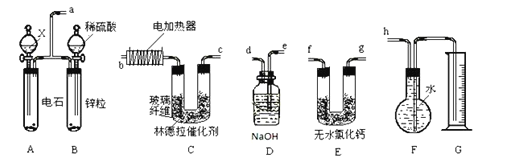
(1)试剂X为:_____。
(2)写出A中所发生反应的化学方程式(有机物写结构简式):_____。
(3)所用装置的连接顺序是_____(填各接口的字母)。
(4)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_____。
Ⅱ.实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成 SO2、CO2、水蒸气等无机物。某研究性学习小组用下图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。
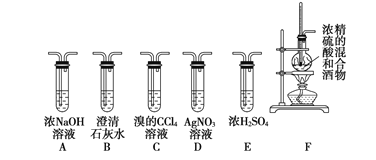
(1)为实现上述实验目的,装置的连接顺序为 F→_____→_____→_____→_____→D。(各装置限用一次),B装置的作用是_____。
(2)当C中观察到_____时,表明单质溴能与乙烯反应;若D中_______,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是_____反应,则D装置中溶液的作用_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关糖类油脂及蛋白质的说法正确的是( )
A.相同质量的这三种物质在人体内被完全氧化时,糖类释放的能量最多
B.油脂中的碳链均为碳碳单键时,主要是低沸点的植物油
C.蛋白质仅由碳、氢、氧三种元素组成
D.淀粉、纤维素及蛋白质均能发生水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为建设美丽浙江,浙江省政府开展“五水共治”。
(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2。工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:_______________。
(2)某地污水中的有机污染物主要成分是三氯乙烯 (C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验探究小组进行如下实验,探究化学反应中的能量变化。
实验① | 实验② |
|
|
温度计读数升高 | 温度计读数降低 |
下列判断一定正确的是( )
A.实验①的反应中化学键断裂吸收的能量大于实验②
B.实验①的反应中化学键断裂吸收的能量小于实验②的反应中化学键形成放出的能量
C.实验①说明中和反应放出热量
D.实验②说明所有有氨气生成的反应均吸收热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物Z是一种天然除草剂,可由X、Y在一定条件下反应制得。下列说法正确的是( )
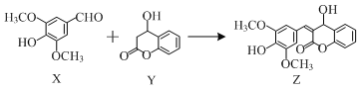
A.有机物X最多可与3molH2发生加成反应
B.可用FeCl3溶液鉴别X和Y
C.Y在Cu作催化剂条件下可被氧化为含醛基的物质
D.X与Y只通过加成反应即可生成Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 晶体的晶胞结构与NaCl晶体的相似
晶体的晶胞结构与NaCl晶体的相似![]() 如图所示
如图所示![]() ,但因为
,但因为![]() 晶体中含有的哑铃形
晶体中含有的哑铃形![]() 的存在,使晶胞沿一个方向拉长。下列关于
的存在,使晶胞沿一个方向拉长。下列关于![]() 晶体的说法中正确的是
晶体的说法中正确的是![]()

A. 1个![]() 周围距离最近且等距离的
周围距离最近且等距离的![]() 数目为4
数目为4
B. 该晶体中的阴离子和O2是等电子体
C. ![]() 克
克![]() 晶体中含阴离子0.2mol
晶体中含阴离子0.2mol
D. 与每个![]() 距离相等且最近的
距离相等且最近的![]() 共有12个
共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
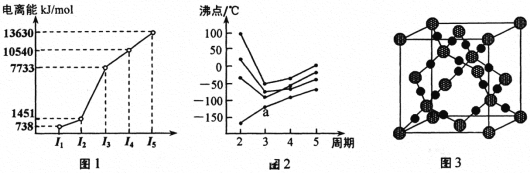
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有_____种不同运动状态的电子。
(2)如图2所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________。判断依据是____________。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_____________晶体。
(4)第一电离能介于Al、P之间的第三周期元素有____种。 GaCl3中中心原子的杂化方式为_________,写出与GaCl3结构相同的一种等电子体(写离子)______________。
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有__________个紧邻分子。 D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是_____________(填字母标号)。
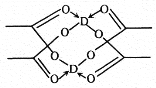
a.极性键 b.非极性键 c.配位键 d.金属键
(6)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A~D图中正确的是_____(填字母标号)。

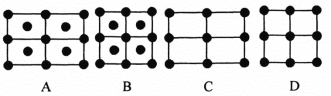
铁原子的配位数是____________,假设铁原子的半径是r cm,该晶体的密度是ρg/cm3 ,则铁的相对原子质量为________________(设阿伏加德罗常数的值为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com