
����Ŀ���� X��Y��Z ����Ԫ�أ���X��Y��Z �ĵ����ڳ����¾�Ϊ���壬��X ���ʿ����� Z �ĵ�����ȼ�գ��� �ɻ����� XZ������ʲ�ɫ����XZ ��������ˮ����ˮ��Һ�е��봦 X+�� Z������ˮ��Һ��ʹ��ɫʯ���� ֽ��죬��ÿ���� X2 ��������һ�� Y2���ӻ��ϳ����� X2Y ���ӣ�X2Y ������ΪҺ�壬��Z �������� X2Y �У����õ���Һ����Ư���ԡ�
��1��д���������ĵ���ʽ��X+_____��Z��______��Y ԭ��_____��
��2��д�� X2Y �Ļ�ѧʽ_____����Ҫ���� X2Y ���Ӿ�����ͬ�����������Ļ�ѧ���ţ�����ԭ�Ӻ� ��������_____��5 ��ԭ�Ӻ˵ķ���_____��
��3��д�� Z �������� X2Y �з�����Ӧ�����ӷ���ʽ��_____��������Һ��ʹ���۵� ������Һ��������Ҫ�����õ�����_____��
��4��ʵ�����Ʊ� XZ �Ļ�ѧ����ʽ��_____����μ��� XZ �Ƿ��ռ���__________��
���𰸡�H+ ![]()
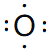 H2O OH�� CH4 Cl2+H2O��H++Cl��+HClO Cl2 NaCl��s��+H2SO4��Ũ��
H2O OH�� CH4 Cl2+H2O��H++Cl��+HClO Cl2 NaCl��s��+H2SO4��Ũ��![]() NaHSO4+HCl�� ��ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ���
NaHSO4+HCl�� ��ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ���
��������
XZ��������ˮ����ˮ��Һ�е����X+��Z����XZ��ˮ��Һ��ʹʯ����Һ��죬��Һ�����ԣ���XΪ��Ԫ�أ�X����ΪH2�����X�ĵ�����Z�ĵ�����ȼ������XZ��ȼ��ʱ����ʲ�ɫ����֪ZΪClԪ�أ�Z�ĵ���ΪCl2����XZΪHCl��X2Y������ΪҺ�壬��X2YΪH2O��˵��YΪOԪ�أ�Cl2����H2O��Ӧ����HCl��HClO��HClO����Ư�����ã��������⣬�����Ϸ������
XZ��������ˮ����ˮ��Һ�е����X+��Z����XZ��ˮ��Һ��ʹʯ����Һ��죬��Һ�����ԣ���XΪ��Ԫ�أ�X����ΪH2�����X�ĵ�����Z�ĵ�����ȼ������XZ��ȼ��ʱ����ʲ�ɫ����֪ZΪClԪ�أ�Z�ĵ���ΪCl2����XZΪHCl��
X2Y������ΪҺ�壬��X2YΪH2O��˵��YΪOԪ�أ�Cl2����H2O��Ӧ����HCl��HClO��HClO����Ư�����ã��������⣻
��1��X+ΪH+�������ʽΪH+��Z��ΪCl���������ʽΪ![]() ��YΪOԪ�أ���ԭ�ӵ���ʽΪ
��YΪOԪ�أ���ԭ�ӵ���ʽΪ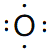 ��
��
�ʴ�Ϊ��H+��![]() ��
��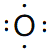 ��
��
��2��X2Y �Ļ�ѧʽΪH2O���� H2O ���Ӿ�����ͬ�����������Ļ�ѧ���ţ�����ԭ�Ӻ� ��������ΪOH����5 ��ԭ�Ӻ˵ķ���ΪCH4��
�ʴ�Ϊ��H2O��OH����CH4��
��3��Z �������� X2Y �з�����Ӧ�����ӷ���ʽ��Cl2+H2O��H++Cl��+HClO��������Һ��ʹ���۵⻯����Һ��������Ҫ�����õ����ǣ�Cl2��
�ʴ�Ϊ��Cl2+H2O��H++Cl��+HClO��Cl2��
��4��ʵ�����Ʊ� HCl �Ļ�ѧ����ʽ��NaCl��s��+H2SO4��Ũ��![]() NaHSO4+HCl�������� HCl �Ƿ��ռ�����������ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ�����
NaHSO4+HCl�������� HCl �Ƿ��ռ�����������ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ�����
�ʴ�Ϊ��NaCl��s��+H2SO4��Ũ��![]() NaHSO4+HCl������ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ�����
NaHSO4+HCl������ʪ�����ɫʯ����ֽ�����ڼ���ƿ�ڣ���ֽ��죬�����ռ���������δ�ռ�����


 �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д� ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ�������ͨ��X��������Ӧ��2X��g��![]() Y��g�����¶�T1��T2��X�����ʵ���Ũ��c��X����ʱ��t�仯��������ͼ��ʾ������������ȷ����
Y��g�����¶�T1��T2��X�����ʵ���Ũ��c��X����ʱ��t�仯��������ͼ��ʾ������������ȷ����

A. T1��T2 ��H �� 0
B. �÷�Ӧ���е�M��ų����������ڽ��е�W��ų�������
C. M�������Ӧ����v����������N����淴Ӧ����v���棩
D. M��ʱ�ټ���һ����X��ƽ���X��ת���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ɱ���ܱ�������ʢ��������N2��H2�Ļ�����壬��һ�������·�����Ӧ��N2��g��+3 H2 ��g��![]() 2NH3��g��,��ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV L,����NH3�������0.1 V L������˵����ȷ����
2NH3��g��,��ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV L,����NH3�������0.1 V L������˵����ȷ����
A. ԭ�����������Ϊ1.2V L B. ��Ӧ��ƽ��ʱN2���ĵ�0.2 V L
C. ԭ�����������Ϊ1.1VL D. ��Ӧ��ƽ��ʱH2���ĵ�0.5 V L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�ˮ����ȡþ���ɰ����²�����У�
�ٰѱ����Ƴ�ʯ���飻
��������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ����
�۽������������ᷴӦ���ᾧ���ˡ���HCl�����Χ�и�����
�ܽ��õ��IJ������ڵ��õ�þ��
����˵������ȷ���ǣ� ��
A. �˷����ŵ�֮һ��ԭ����Դ�ḻB. �٢ڢ۲����Ŀ���ǴӺ�ˮ����ȡþ��
C. �٢ڢ۲����漰���ϡ��ֽ���ֽⷴӦD. �ڢٵ��ڢܲ��ķ�Ӧ����������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������NOx��SO2����������Ҫ�ɷ֡�
��NOx��Ҫ��Դ������β����
��֪��N2��g����O2��g��![]() 2NO��g�� ��H����180.50 kJ��mol��1
2NO��g�� ��H����180.50 kJ��mol��1
2CO��g����O2��g��![]() 2 CO2��g�� ��H����566.00kJ��mol��1
2 CO2��g�� ��H����566.00kJ��mol��1
��1��Ϊ�˼��������Ⱦ���������������β�������ܿڲ��ô�����NO��COת��������Ⱦ����������ѭ����д���÷�Ӧ���Ȼ�ѧ����ʽ_________________��
��2��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У������¶Ⱥ�������䣬��Ӧ���̣�0��15min����NO�����ʵ�����ʱ��仯�Ĺ�ϵ����ͼ��ʾ��


��T��ʱ�û�ѧ��Ӧ��ƽ�ⳣ��K��_______________��ƽ��ʱ�������¶Ȳ��䣬���������г���CO��N2��0.8mol��ƽ�⽫_______�ƶ���������������������������������
��ͼ��a��b�ֱ��ʾ��һ���¶��£�ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n(NO)�ı仯���ߣ����б�ʾ����������ϴ��������__________������a������b������
��15minʱ�����ı���練Ӧ����������n(NO)������ͼ��ʾ�ı仯����ı������������_______��
����SO2��Ҫ��Դ��ú��ȼ�ա�ȼú��������������Ǽ��ٴ����к�������Ⱦ�Ĺؼ���
��3���ô�����Һ����SO2�ɽ���ת��ΪHSO3�����÷�Ӧ�����ӷ���ʽ��___________________��
��4����ͼ���װ�ÿɽ������е�NO��SO2�ֱ�ת��ΪNH4+��SO42��������A�Ļ�ѧʽΪ_____________�������ĵ缫��Ӧʽ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������100mL 1.0 mol/L Na2CO3��Һ����ȷ�ķ�����
�� ��10.6 g Na2CO3 ����100mLˮ��
�� ��28.6g Na2CO3��10H2O����ˮ���100 mL��Һ
�� ��20 ml 5.0 mol/L Na2CO3��Һ��ˮϡ����100 mL
A. �٢ڢ� B. �ڢ� C. ֻ�Т� D. ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ӧ���������仯��ͼ��ʾ������˵����ȷ����

A. ��Ӧ����a�д�������
B. �÷�ӦΪ���ȷ�Ӧ����ЧӦ���ڡ�H
C. �д����������£���Ӧ�Ļ�ܵ���E1+E2
D. �ı�������ɸı�÷�Ӧ�Ļ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ����������ʯī������ʢ�б���NaCl��Һ��U���С����з�����ȷ�ģ���
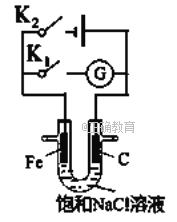
A. K1�պϣ������Ϸ����ķ�ӦΪ2H����2e��=H2��
B. K1�պϣ�ʯī����Χ��Һ������ǿ
C. K2�պϣ��������ᱻ��ʴ��������������������������
D. K2�պϣ���·��ͨ��0.002NA������ʱ������������0.001mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(FexNy)�ڴż�¼�����������Ź㷺��Ӧ��ǰ����ijFexNy���Ʊ���������������ͪ���Ҵ����롣
��1��Fe��̬ԭ�ӽṹʾ��ͼ__________��
��2����ͪ( )�����и�Ԫ�ص縺�ԴӴ�С˳����________��1 mol��ͪ�����к��ЦҼ�����ĿΪ________��
)�����и�Ԫ�ص縺�ԴӴ�С˳����________��1 mol��ͪ�����к��ЦҼ�����ĿΪ________��
��3��ijFexNy�ľ�����ͼ1��ʾ��Cu������ȫ����þ�����aλ��Fe����bλ��Fe���γ�Cu����Ͳ���Fe(x��n)CunNy��FexNyת��Ϊ����Cu����Ͳ���������仯��ͼ2��ʾ�����и��ȶ���Cu����Ͳ���Ļ�ѧʽΪ________��


��4����ѧ���Ƶ���20��̼ԭ����ɵ� ������״����C20������״�ṹ��������������ι��ɣ���ͼ����

��ش�:һ�� C20���ӹ���_______����ߣ��Ʋ�C20�����Ӳ��_______����ϴ���С��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com