
【题目】某化学小组参观制碱厂后,绘制了该厂生产纯碱的工艺流程图如图。据图判断下列说法错误的是( )

A. 流程图Ⅰ是依次向粗盐水中加入Ca(OH)2和Na2CO3,二者加入的顺序可以颠倒
B. 流程Ⅰ后过滤得到的沉淀成分有Mg(OH)2和CaCO3
C. 通入NH3的主要作用是形成碱性溶液,有利于CO2的吸收
D. 碳酸氢钠首先从溶液中结晶析出的原因其溶解度较小
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列反应或过程需要吸收能量的是( )
A.可燃物的燃烧过程B.手机锂电池充电过程
C.Mg+2HCl=MgCl2+H2↑D.H2SO4+2KOH=K2SO4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是( )
A.B、C、N原子最外层电子数依次增多
B.Na、Mg、Al元素最高正价依次升高
C.Be、Mg、Ca的电子层数依次增多
D.Li、Be、B原子半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象能正确反映对应的变化关系的是( )
A. 向一定量的稀硫酸中滴加氢氧化钠

B. 向一定量的H2SO4和MgSO4混合溶液中滴加氢氧化钡溶液

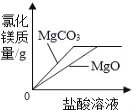
C. 将足量块状MgCO3和MgO粉末分别加入相同质量、相同质量分数的稀盐酸中
D. 在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得诺贝尔化学奖。轮烷是一种分子机器的“轮子”,芳香化合物a、b、c是合成轮烷的三种原料,其结构如下图所示。下列说法不正确的是

A. b、c互为同分异构体
B. a、c分子中所有碳原子均有可能处于同一平面上
C. a、b、c均能发生氧化反应、加成反应、加聚反应和酯化反应
D. a、b、c均能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) △H1=+551kJmol-1
反应Ⅲ:S(g)+O2(g)=SO2(g) △H3=-297kJmol-1
反应Ⅱ的热化学方程式:____________________。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如右图所示,p2______p1(填“>”或“<”),得出该结论的理由是__________。

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下,将ii补充完整
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=______+______+2I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象,(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4molL-1 KI | amolL-1 KI 0.2molL-1H2SO4 | 0.2molL-1H2SO4 | 0.2molL-1 KI 0.0002 molI2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
① B是A的对比实验,则a=______。
②比较A、B、C,可得出的结论是______。
③实验表明,SO2的歧化反应速率D>A.结合i,ii反应速率解释原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
B | 淀粉溶液在硫酸存在下加热一段时间后,再与新制的Cu(OH)2悬浊液混合,加热煮沸 | 无红色沉淀生成 | 淀粉没有水解 |
C | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数:Kh(CH3COO-)<Kh(HCO3-) |
D | 常温时,用两支试管各取5 mL 0.1 mol/L 酸性KMnO4溶液,分别加入0.1 mol/L和0.2 mol/L H2C2O4溶液各2 mL | 两试管溶液均褪色,且加0.2 mol/L H2C2O4溶液的试管中褪色更快 | 其它条件不变,H2C2O4溶液的浓度越大,化学反应速率越大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com