
【题目】利用反应![]() 构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是
构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是![]()
![]()

A.电流从左侧电极经过负载后流向右侧电极
B.电极A极反应式为![]()
C.为使电池持续放电,离子交换膜需选用阴离子交换膜
D.当有![]() 被处理时,转移电子数为
被处理时,转移电子数为![]()
科目:高中化学 来源: 题型:
【题目】医疗上绿矾![]() 是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究:
是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究:
Ⅰ![]() 制备产品
制备产品![]()
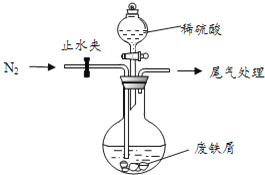
该小组由废铁屑![]() 含少量氧化铜、氧化铁等杂质
含少量氧化铜、氧化铁等杂质![]() ,用如图所示装置制备
,用如图所示装置制备![]() 晶体,步骤如下:
晶体,步骤如下:
![]() 预处理:先将废铁屑加入到饱和
预处理:先将废铁屑加入到饱和![]() 溶液中洗涤,目的是______,然后将废铁屑用水洗涤
溶液中洗涤,目的是______,然后将废铁屑用水洗涤![]() 遍.
遍.
![]() 将洗涤后的废铁屑加入到圆底烧瓶中,并持续通入
将洗涤后的废铁屑加入到圆底烧瓶中,并持续通入![]() ,
,![]() 的作用是______.
的作用是______.
![]() 再加入足量稀硫酸,控制温度
再加入足量稀硫酸,控制温度![]() 之间,充分反应后,圆底烧瓶中剩余的固体为______.
之间,充分反应后,圆底烧瓶中剩余的固体为______.
![]() 获取产品:先向步骤
获取产品:先向步骤![]() 中反应后的混合物中加入少许蒸馏水,趁热过滤,______
中反应后的混合物中加入少许蒸馏水,趁热过滤,______![]() 滤出晶体,用少量冰水洗涤
滤出晶体,用少量冰水洗涤![]() 次,再用滤纸将晶体吸干,密闭保存.
次,再用滤纸将晶体吸干,密闭保存.
Ⅱ![]() 测定
测定![]() 含量
含量![]()
![]() 称取上述样品
称取上述样品![]() ,溶于适量的稀硫酸中,配成100mL溶液,需要的仪器除天平、玻璃棒、烧杯、量筒外,还需要的仪器有
,溶于适量的稀硫酸中,配成100mL溶液,需要的仪器除天平、玻璃棒、烧杯、量筒外,还需要的仪器有![]() 填仪器名称
填仪器名称![]() ______、______.
______、______.
![]() 准确量取25mL该液体于锥形瓶中,用
准确量取25mL该液体于锥形瓶中,用![]()
![]() 标准溶液滴定,则滴定终点的判断方法是______.
标准溶液滴定,则滴定终点的判断方法是______.
![]() 用同样的方法滴定3次,平均消耗
用同样的方法滴定3次,平均消耗![]() 标准液,该样品中
标准液,该样品中![]() 的质量分数为______
的质量分数为______![]()
![]() 若测量结果偏小,则可能是在定容时 ______
若测量结果偏小,则可能是在定容时 ______ ![]() 填“俯视”或“仰视”
填“俯视”或“仰视”![]() 读数.
读数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是A分子的球棍模型和B分子的比例模型,回答下列问题:

(1)A和B的关系是 。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式 。
(3)写出B分子和金属钠反应的化学方程式 。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Glaser反应是指端炔烃在催化剂存在下可发生偶联反应,例如:
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
下面是利用Glaser反应制备化合物E的一种合成路线:
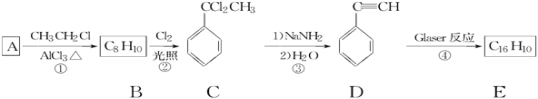
回答下列问题:
(1)B的结构简式为__,D的化学名称为__。
(2)步骤②的反应化学方程式:__。
(3)E的结构简式为__。用1molE合成1,4二苯基丁烷,理论上需要消耗氢气__mol。
(4)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢原子,数目比为3∶1,写出符合条件的两种F的结构简式___、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有化合物:
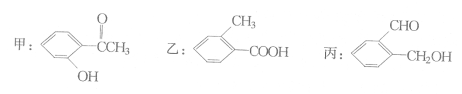
(1)请写出丙中含氧官能团的名称:___________________。
(2)请判别上述哪些有机物互为同分异构体:___________
(3)鉴别乙的方法(指明所选试剂及主要现象即可):__________
(4)请按酸性由强至弱排列甲、乙、丙的顺序:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2X(g)+Y(g)2Z(g),某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定不同时间内X的转化率,得到的数据如表所示,下列判断正确的是( )
t/min | 2 | 4.5 | 5 | 6 |
X的转化率 | 30% | 40% | 70% | 70% |
A.随着反应的进行,混合气体的密度不断增大
B.其他条件不变,将X的物质的量改为10mol,则可得到4molZ
C.6min时,容器中剩余1.4molY
D.反应在5.5min时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A对氢气的相对密度为30,分子中含碳40%,含氢6.6%,其余为氧。
(1)通过计算确定该有机物的分子式;____
(2)按中学常见官能团,写出其可能的结构简式。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡金属在生产生活中的应用十分广泛。
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,由以上实验事实可以判断CrO2Cl2分子是_____________(填“极性”或“非极性”)分子,该分子的立体构型的名称为___________。
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(2)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,先后发生的离子方程式为Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,_______________。
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为__________________________;析出晶体的原因是_______________________________________________________。若将Cu单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________________。
(4)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3____H2O(填“大于”、“等于”或“小于”)。
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。
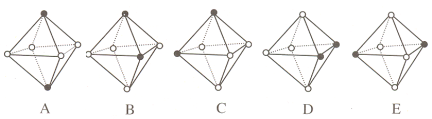
(5)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是_________。(填字母编号,任填一组。图中黑点为NH3,圆圈为CO,Ni略去)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氟气反应生成氟化氢的过程中能量变化如图所示。由图可知

A. 生成1 molHF气体放出的热量为270 kJ
B. H2(g)+ F2(g)→ 2HF(l)+ 270 kJ
C. 反应物的总能量大于生成物的总能量
D. 该反应是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com